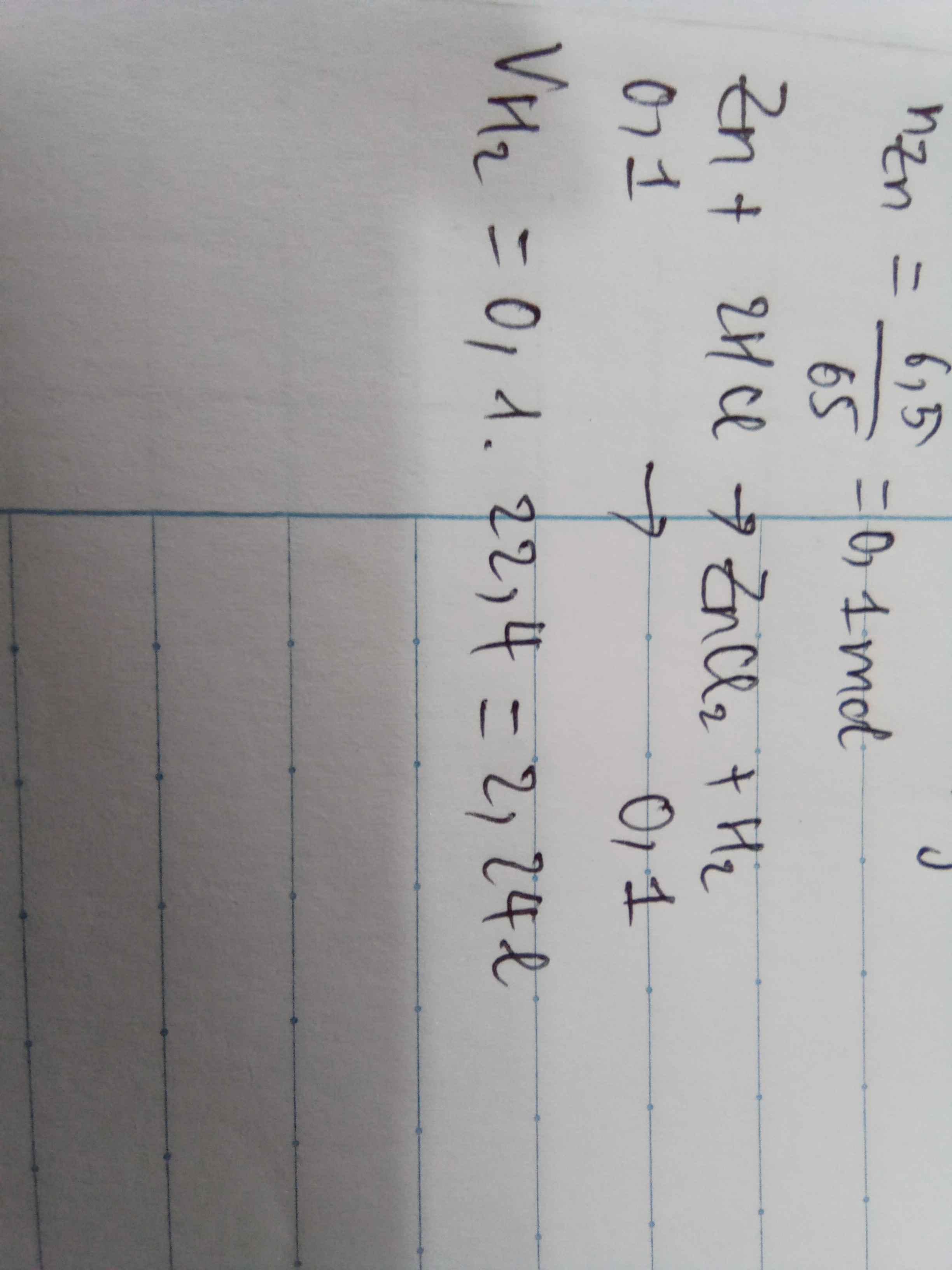Cho 32,5g Zn tác dụng vs dung dịch có chứa 29,2g HCl. Tính thể tích khí H2( đktc) thu được
H24
Những câu hỏi liên quan
cho 32,5g Zn tác dụng vừa đủ với dung dịch HCl 20o/o thu được kẽm clorua (ZnCl2) và khí hidro (H2).
tính thể tích H2 sinh ra ở đktc?
tính khối lượng dung dịch HCl cần dùng?
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Ta có: \(n_{Zn}=\dfrac{32,5}{65}=0,5\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=1\left(mol\right)\\n_{H_2}=0,5\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{ddHCl}=\dfrac{1\cdot36,5}{20\%}=182,5\left(g\right)\\V_{H_2}=0,5\cdot22,4=11,2\left(l\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho 32,5g bột kẽm Zn tác dụng vừa đủ với dung dịch axit Clohiđric theo sơ đồ phản ứng sau : Zn +HCl ---> ZnCl2+H2 Hãy tính : a thể tích khí hiđro thu được ở đktc b khối lượng axit Clohiđric cần dùng
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
+\(n_{Zn}=\dfrac{32,5}{65}=0,5\left(mol\right)\)
+\(nH_2=n_{Zn}=0,5\left(mol\right)\)
+\(n_{HCl}=2n_{Zn}=1\left(mol\right)\)
+\(V_{H2}=0,5.22,4=11,2\left(lit\right)\)
\(m_{HCl}=1.36,5=36,5\left(gam\right)\)
Đúng 2
Bình luận (0)
\(n_{Zn}=\dfrac{m}{M}=\dfrac{32,5}{65}=0,5\left(mol\right)\)
\(Zn\) \(+\) \(2\)\(HCl\) → \(ZnCl_2\) \(+\) \(H_2\)
\(0,5\) \(mol\) → \(1\) \(mol\) → \(0,5\)\(mol\) → \(0,5\) \(mol\)
\(V_{H_2}=n.22,4=0,5.22,4=11,2\left(l\right)\)
\(m_{HCl}=n.M=1.36,5=36,4\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 8,125g Zn tác dụng dung dịch HCL loãng có chứa 18,25g HCL . hãy tính thể tích khí H2 sinh ra ở đktc
\(n_{Zn}=\dfrac{8,125}{65}=0,125mol\)
\(n_{HCl}=\dfrac{18,25}{36,5}=0,5mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Xét: \(\dfrac{0,125}{1}\) < \(\dfrac{0,5}{2}\) ( mol )
0,125 0,125 ( mol )
\(V_{H_2}=0,125.22,4=2,8l\)
Đúng 4
Bình luận (0)
Cho 13g Zn tác dụng dung dịch HCL có chứa 14,6g. hãy tính thể tích khí H2 sinh ra ở đktc
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\); \(n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
Xét tỉ lệ: \(\dfrac{0,2}{1}=\dfrac{0,4}{2}\) => pư vừa đủ
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2----------------->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
Đúng 5
Bình luận (0)
nZn=13/65=0,2mol
nHCl=14,6/36,5=0,4mol
Zn+2HCl→ZnCl2+H2
Xét: 0,2 < 0,4 ( mol )
0,4 0,4 ( mol )
VH2=0,4.22,4=8,96
Đúng 2
Bình luận (0)
Cho 2,4g Zn tác dụng với dung dịch HCl Thu được ZnCl2 và H2, hãy tính: a,thể tích khí H2 thu được (đktc) b, khối lượng của HCl và ZnCl2
Cho 0,65 gam Zn tác dụng với dung dịch HCL
a) Tính khối lượng ZnCl2 tạo thành
b) Thể tích khí H2 thu được (đktc)
nZn = 0.65 / 65 = 0.01 (mol)
Zn + 2HCl => ZnCl2 + H2
0.01..................0.01......0.01
mZnCl2 = 0.01 * 136 = 1.36 (g)
VH2 = 0.01 * 22.4 = 0.224 (l)
Đúng 2
Bình luận (0)
nZn=0,65/65=0,01(mol)
Zn+ 2HCl-------> ZnCl2+ H2
0,01 0,01 0,01 (mol)
a) m ZnCl2=0,01*136=1,36 (gam)
b)V H2(đktc)=0,01*22,4=0,224(lit)
Đúng 0
Bình luận (0)
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).a) Viết phương trình hóa học xảy ra.b) Tính thể tích khí H2 (đktc)
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính thể tích khí H2 (đktc)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
Đúng 2
Bình luận (0)
13/ Cho 16,8g sắt tác dụng với dung dịch HCl dư. Tính thể tích khí H2 thu được ở đktc.
14/ Cho 25g CaCO3 vào dung dịch HCl dư. Tính thể tích khí CO2 thu được (ở đktc).
15/ Cho 16 g hỗn hợp hai kim loại Fe và Mg tác dụng hoàn toàn với dung dịch HCl dư, sinh ra 6,72 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
\(13,n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\\ PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ .....0,3.....0,6......0,3......0,3\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,3\cdot22,4=6,72\left(l\right)\\ 14,n_{CaCO_3}=\dfrac{25}{40+12+16\cdot3}=0,25\left(mol\right)\\ PTHH:CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\\ .....0,25.....0,5......0,25......0,25......0,25\left(mol\right)\\ V_{CO_2\left(đktc\right)}=0,25\cdot22,4=5,6\left(l\right)\)
Đúng 1
Bình luận (0)