Viết PTHH điều chế khí Clo trong công nghiệp và trong phòng thí nghiệm
GG
Những câu hỏi liên quan
Hãy trình bày các phương pháp điều chế khí oxi trong phòng thí nghiệm và trong công nghiệp. Tại sao không áp dụng phương pháp điều chế khí trong phòng thí nghiệm, và ngược lại?
Điều chế oxi:
- Trong phòng thí nghiệm, oxi được điều chế bằng cách phân hủy những hợp chất giàu Oxi và ít bên với nhiệt như KMnO4, KClO3, ...
2KMnO4 → K2MnO4 + MnO2 + O2
2KClO3 → 2KCl + 3O2
- Trong công nghiệp:
a) Từ không khí: Không khí sau khi đã loại bỏ hết hơi nước, khí CO2, được hóa lỏng dưới áp suất 200 atm đồng thời hạ thấp nhiệt độ. Chưng cất phân đoạn không khí lỏng, thu được oxi lỏng. Oxi lỏng được vận chuyển trong những bình thép có thể tích 100 lít dưới áp suất 150atm.
b) Từ nước. Điện phân nước: 2H2O
Người ta không áp dụng phương pháp phòng thí nghiệm cho phòng thí nghiệm vì trong phòng thí nghiệm chỉ điều chế lượng nhỏ oxi, còn công nghiệp cần một lượng lớn giá thảnh rẻ.
Đúng 0
Bình luận (0)
Tính chất vật lí tính chất hóa học điều chế khí oxi trong phòng thí nghiệm và trong công nghiệp
4) Viết phương trình điều chế Cl2 và HCl trong công nghiệp và trong phòng thí nghiệm.
Cái này SGK có nha em!
Đúng 3
Bình luận (0)
Nêu nguyên liệu dùng để điều chế oxi, hidro trong phòng thí nghiệm. Viết pthh minh họa? Nguyên liệu dùng để điều chế oxi trong phòng thí nghiệm phải có đặc điểm gì? Không khí có thành phần như thế nào? Có thể thu khí oxi và hidro bằng những cách nào, tại sao?
Đọc tiếp
Nêu nguyên liệu dùng để điều chế oxi, hidro trong phòng thí nghiệm. Viết pthh minh họa? Nguyên liệu dùng để điều chế oxi trong phòng thí nghiệm phải có đặc điểm gì? Không khí có thành phần như thế nào? Có thể thu khí oxi và hidro bằng những cách nào, tại sao?
Hình vẽ mô tả thí nghiệm điều chế khí clo trong phòng thí nghiệm: Hóa chất trong bình 1 và bình 2 lần lượt là A. dung dịch NaCl bão hòa và dung dịch H2SO4 đặc. B. dung dịch H2SO4 đặc và dung dịch NaCl bão hòa. C. nước cất và dung dịch H2SO4 đặc. D. dung dịch NaCl bão hòa và dung dịch KOH đậm đặc.
Đọc tiếp
Hình vẽ mô tả thí nghiệm điều chế khí clo trong phòng thí nghiệm:
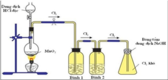
Hóa chất trong bình 1 và bình 2 lần lượt là
A. dung dịch NaCl bão hòa và dung dịch H2SO4 đặc.
B. dung dịch H2SO4 đặc và dung dịch NaCl bão hòa.
C. nước cất và dung dịch H2SO4 đặc.
D. dung dịch NaCl bão hòa và dung dịch KOH đậm đặc.
Chọn A
Khí Cl2 sinh ra bị lẫn tạp chất là khí HCl và hơi nước, bình 1 chứa dung dịch NaCl bão hòa có tác dụng giữ lại HCl còn bình 2 chứa dd H2SO4 đặc có tác dụng giữ lại hơi nước
Đúng 0
Bình luận (0)
nêu phương pháp và vẽ hình thí nghiệm điều chế H2 trong phòng thí ngiệm. Nêu các cách thu khí vào bình và giải thích, Viết PTHH phản ứng ?

Dựa vào tính chất H2 tan rất ít trong nước.
PTHH:
Fe + H2SO4 -> FeSO4 + H2
Fe + 2HCl -> FeCl2 + H2
Zn + H2SO4 -> ZnSO4 + H2
Zn + 2HCl -> ZnCl2 + H2
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
2Al + 6HCl -> 2AlCl3 + 3H2
Đúng 3
Bình luận (0)
Trình bày sự khác nhau về việc điều chế khí oxi trong phòng thí nghiệm và trong công nghiệp về nguyên liệu ,sản lượng và giá thành.
| Phòng thí nghiệm | Công nghiệp | |
| Nguyên liệu | Chất giàu Oxi như : KMnO4 . KClO3 | Không khí , nước |
| Sản lượng | Đủ dùng | sản lượng lớn |
| Giá thành | Cao | Thấp |
Đúng 1
Bình luận (0)
tại sao không áp dụng phương pháp điều chế khí oxi trong phòng thí nghiệm cho công nghiệp và ngược lại ?
Người ta không áp dụng phương pháp trong phòng thí nghiệm cho công nghiệp và ngược lại vì trong phòng thí nghiệm chỉ cần lượng nhỏ oxi, còn trong công nghiệp cần một lượng lớn, giá thành rẻ.
Đúng 0
Bình luận (0)
II-Tự luận
Viết phương trình điều chế: C l 2 trong công nghiệp và HCl trong phòng thí nghiệm (theo phương pháp sunfat)
- Sản xuất clo trong CN:
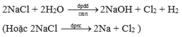
- Điều chế HCl trong PTN theo pp sunfat:
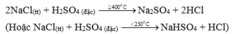
Đúng 0
Bình luận (0)



