Trình bày sự hình thành liên kết cộng hóa trị trong phân tử NH3.
Tuyển Cộng tác viên Hoc24 nhiệm kì 26 tại đây: https://forms.gle/dK3zGK3LHFrgvTkJ6
H24
Những câu hỏi liên quan
trình bày sự hình thành lai hóa sp3 của ngtu C trong phtu CHCl3 và sự hình thành các liên kết trong phân tử này.
Cho hợp chất CaO. Xác định loại liên kết hóa học trong phân tử CaO và trình bày sự hình thành liên kết đó.
Hãy mô tả sự hình thành liên kết cộng hóa trị trong phân tử carbon dioxide, ammonia (gồm một nguyên tử N liên kết với ba nguyên tử H)
`-` Khi hình thành liên kết cộng hóa trị trong phân tử `CO_2`, các nguyên tử đã liên kết với nhau như sau:
Mỗi nguyên tử `C` và `O` lần lượt có `12e` và `16e`. Để hình thành phân tử `CO_2`, nguyên tử `C` đã liên kết với `2` nguyên tử `O` bằng cách nguyên tử `C` góp chung với mỗi nguyên tử `O` là `2e` ở lớp ngoài cùng tạo thành các cặp electron dùng chung.
`NH_3`
Mỗi nguyên tử `N` và `H` lần lượt có `14e` và `1e`. Để hình thành phân tử ammonia, nguyên tử `N` liên kết với nguyên tử `H` bằng cách nguyên tử `N` góp chung với nguyên tử `H` là `1e` ở lớp ngoài cùng tạo thành `3` cặp electron dùng chung.
Đúng 2
Bình luận (0)
Hãy mô tả sự hình thành liên kết cộng hóa trị trong phân tử khí chlorine, khí nitrogen
`Cl_2`
Mỗi nguyên tử `Cl` có `7e` ở lớp ngoài cùng. Để có cấu trúc electron bền vững giống khí hiếm `Ar`, `2` nguyên tử `Cl` đã liên kết với nhau bằng cách mỗi nguyên tử `Cl` góp chung `1e` ở lớp ngoài cùng tạo thành `1` cặp electron dùng chung.
`N_2`
Mỗi nguyên tử `N` có `5e` ở lớp ngoài cùng. Để có cấu trúc electron bền vững giống khí hiếm `Ne`,`2` nguyên tử `N` đã liên kết với nhau bằng cách mỗi nguyên tử `N` góp chung `3e` ở lớp ngoài cùng tạo thành `3` cặp electron dùng chung.
Đúng 2
Bình luận (0)
Sơ đồ sau mô tả sự hình thành liên kết cộng hóa trị trong phân tử HCl:
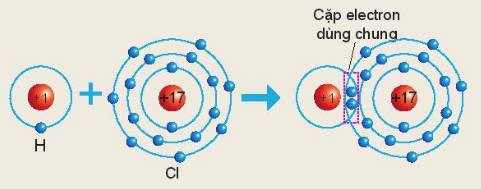
Xác định hóa trị của chlorine trong hợp chất trên
Nguyên tử `Cl` dùng chung `1` cặp electron với nguyên tử `H`
`->` Trong phân tử muối `HCl,` nguyên tử nguyên tố `Cl` sẽ có hóa trị là `I`.
Đúng 1
Bình luận (0)
Hãy vẽ sơ đồ mô tả sự hình thành liên kết cộng hóa trị trong phân tử CH4 giữa 1 nguyên tử C và 4 nguyên tử H.
Cho các phát biểu về NH3 và NH4+ như sau: (1) Trong NH3 và NH4+, nitơ đều có số oxi hóa -3; (2) NH3 có tính bazơ, NH4+ có tính axit; (3) Trong NH3 và NH4+, đều có cộng hóa trị 3; (4) Phân tử NH3 và ion NH4+ đều chứa liên kết cộng hóa trị. Số phát biểu đúng là và NH4+, nitơ đều có số oxi hóa -3; (2) NH3 có tính bazơ, NH4+ có tính axit; (3) Trong NH3 và NH4+, đều có cộng hóa trị 3; (4) Phân tử NH3 và ion NH4+ đều chứa liên kết cộng hóa trị. Số phát biểu đúng là A. 1 B. 2 C. 3 D. 4
Đọc tiếp
Cho các phát biểu về NH3 và NH4+ như sau:
(1) Trong NH3 và NH4+, nitơ đều có số oxi hóa -3;
(2) NH3 có tính bazơ, NH4+ có tính axit;
(3) Trong NH3 và NH4+, đều có cộng hóa trị 3;
(4) Phân tử NH3 và ion NH4+ đều chứa liên kết cộng hóa trị.
Số phát biểu đúng là
và NH4+, nitơ đều có số oxi hóa -3;
(2) NH3 có tính bazơ, NH4+ có tính axit;
(3) Trong NH3 và NH4+, đều có cộng hóa trị 3;
(4) Phân tử NH3 và ion NH4+ đều chứa liên kết cộng hóa trị.
Số phát biểu đúng là
A. 1
B. 2
C. 3
D. 4
Đáp án D
Các phát biểu đúng là: (1), (2), (3), (4)
Đúng 0
Bình luận (0)
1.Phân tử nào có liên kết cộng hóa trị không cực ?A. HCl. B. Cl2. C. NH3. D. H2O.2.Liên kết cộng hóa trị có cực tạo thành giữa hai nguyên tửA. phi kim khác nhau. B. cùng một phi kim điển hình.C. phi kim mạnh và kim loại mạnh. D. kim loại và kim loại.
Đọc tiếp
1.Phân tử nào có liên kết cộng hóa trị không cực ?
A. HCl. B. Cl2. C. NH3. D. H2O.
2.Liên kết cộng hóa trị có cực tạo thành giữa hai nguyên tử
A. phi kim khác nhau. B. cùng một phi kim điển hình.
C. phi kim mạnh và kim loại mạnh. D. kim loại và kim loại.
1.Phân tử nào có liên kết cộng hóa trị không cực ?
A. HCl. B. Cl2. (CHỌN B) C. NH3. D. H2O.
2.Liên kết cộng hóa trị có cực tạo thành giữa hai nguyên tử
A. phi kim khác nhau. B. cùng một phi kim điển hình.
C. phi kim mạnh và kim loại mạnh. (Theo anh nhớ là vậy C á) D. kim loại và kim loại.
Đúng 2
Bình luận (0)
Em hãy mô tả quá trình tạo thành liên kết cộng hóa trị trong phân tử nước.
Khi tạo thành phân tử nước, nguyên tử O góp 2 electron, mỗi nguyên tử H góp 1 electron. Như vậy, giữa nguyên tử O và nguyên tử H có 1 đôi electron dùng chung. Hạt nhân nguyên tử O và H cùng hút đôi electron dùng chung, liên kết với nhau tạo ra phân tử nước.
Đúng 1
Bình luận (0)
Trình bày sự giống và khác nhau của 3 loại liên kết: Liên kết ion, liên kết cộng hóa trị không cực và liên kết cộng hóa trị có cực.
Tham khảo:
| So sánh | Liên kết ion | Liên kết cộng hóa trị không có cực | Liên kết cộng hóa trị có cực |
| Giống nhau | Các nguyên tử kết hợp với nhau để tạo ra cho mỗi nguyên tử lớp electron ngoài cùng bền vững giống cấu trúc khí hiếm (2e hoặc 8e) | ||
| Khác nhau về cách hình thành liên kết | Cho và nhận electron | Dùng chung e, cặp e không bị lệch | Dùng chung e, cặp e bị lệch về phía nguyên tử có độ âm điện mạnh hơn |
| Khác nhau về nguyên tố tạo nên liên kết | Giữa kim loại và phi kim | Giữa các nguyên tử của cùng một nguyên tố phi kim | Giữa phi kim mạnh và yếu khác |
Đúng 2
Bình luận (0)






