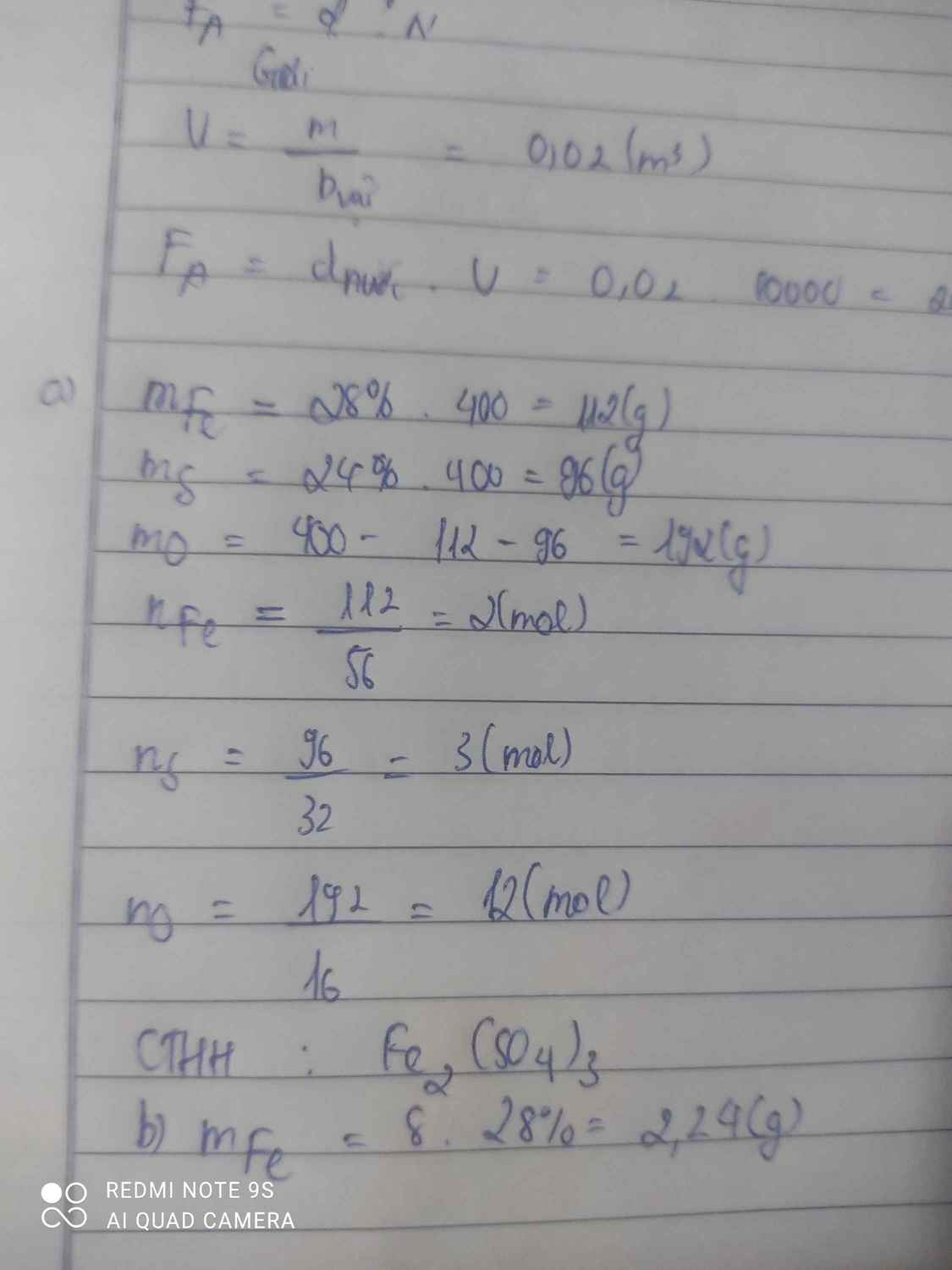Tính thành Phần % theo lượng các nguyên tố trong hợp chất K2 SO4 (K=39,S=32,O=16)
Giúp mik vs
TL
Những câu hỏi liên quan
Tính thành phần phần trăm theo khối lượng của nguyên tố Fe có trong hợp chất Fe203 ( Biết khối lượng của các nguyên tử như sau : K = 39 amu , N = 14 amu , O = 16 amu , Na = 23 amu , S=32 amu , Fe = 56 amu )
Xem chi tiết
klpt : Fe2O3 là : 56.2+16.3=160(amu)
%Fe = \(\dfrac{56.2}{160}\) . 100% = 70%
%O = \(\dfrac{16.3}{160}\) . 100% = 305
Làm ơn tick cho mk
Đúng 0
Bình luận (0)
%Fe = (2×56×100)/(2×56+16×3) = 70%
Đúng 0
Bình luận (0)
Xác định thành phần trăm theo khối lượng của các nguyên tố có trong hợp chất
D. Al2(SO4)3 biết ( Al : 27, S: 32, O : 16)
E. Fe3O4 biết ( Fe: 56, O: 16)
\(\left\{{}\begin{matrix}\%Al=\dfrac{27.2}{342}.100\%=15,79\%\\\%S=\dfrac{32.3}{342}.100\%=28,07\%\\\%O=\dfrac{16.12}{342}.100\%=56,14\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%Fe=\dfrac{56.3}{232}.100\%=72,414\%\\\%O=\dfrac{4.16}{232}.100\%=27,586\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Một hợp chất có công thức hoá học KClO3.Tính thành phần phần trăm theo khối lượng mỗi nguyên tố trong hợp chất(Biết nguyên tử khối của K=39 Cl=35,5 O=16
Ta có CTTH: KClO3
=> Gọi CTTQ là K1Cl1O3
=> \(M_{KClO_3}=122,5\) (g/mol)
\(\%m_K=\dfrac{1
.
39}{122,5}
.
100\%=31,84\%\)
\(\%m_{Cl}=\dfrac{1
.
35,5}{122,5}
.
100\%=28,98\%\)
\(\%m_O=100\%-\left(\%m_K+\%m_{Cl}\right)=100\%-\left(31,84\%+28,98\%\right)=39,18\%\)
Đúng 2
Bình luận (0)
Phần trăm K trong KClO3: \(\%K=\dfrac{39}{39+35,5+16.3}.100=31,84\%\)
Phần trăm Cl trong KClO3: \(\%Cl=\dfrac{35,5}{39+35,5+16.3}.100=28,98\%\)
Phần trăm O trong KClO3: \(\%O=100-31,84-28,98=39,18\%\)
Đúng 1
Bình luận (0)
Tính thành phần phần trăm theo khối lượng các nguyên tố hoá học có trong hợp chất đường mía (C¹² H²² O¹¹) (giúp mình vs ạhh, mik đang cần gấpp)
\(PTK=12.12+1.22+16.11=342< mol>.\)
\(\%C=\dfrac{12.12.100}{342}\approx42,11\%\)
\(\%H=\dfrac{1.22.100}{142}=15,49\%\)
\(\%O=100\%-42,11\%-15,49\%=42,4\%\)
Đúng 3
Bình luận (0)
Cho các CTHH sau: CaCO3; Al2(SO4)3 Hãy tính % khối lượng các nguyên tố có trong mỗi hợp chất (Biết Ca = 40;C= 12; O = 16; Al = 27; S = 32)
Cần gấp ạ
\(M_{CaCO_3}=40+12+16.3=100\left(\dfrac{g}{mol}\right)\\ \%m_{Ca}=\dfrac{40}{100}.100\%=40\%\\ \%m_C=\dfrac{12}{100}.100\%=12\%\\ \%m_O=100\%-\left(12\%+40\%\right)=48\%\\ M_{Al_2\left(SO_4\right)_3}=27.2+\left(32+16.4\right).3=342\left(\dfrac{g}{mol}\right)\\ \%m_{Al}=\dfrac{2.27}{342}.100\%=15,79\%\\ \%m_S=\dfrac{32.3}{342}.100\%=28\%\\ \%m_O=100\%-\left(28\%+15,79\%\right)=56,21\%\)
Đúng 2
Bình luận (0)
(Mg 24; C 12; O 16; Al 27; N 14; H 1; P 31; S 32; Cu 64; Fe 56; )Bài 1: Tính thành phần phần trăm (theo khối lượng) của các nguyên tố hóa học trong các hợp chất sau: 1) MgCO3 2) Al(OH)3 3) (NH4)2HPO4 4) C2H5COOCH3Bài 2: a,Chất nào có phần trăm khối lượng của nguyên tố sắt lớn nhất, nhỏ nhất trong các công thức hóa học sau: FeO; Fe2O3; FeS; FeS2.b,Chất nào sau đây có phần trăm khối lượng oxi lớn nhất, nhỏ nhất: NO2; NO; N2O; N2O3.c,Chất...
Đọc tiếp
(Mg = 24; C = 12; O = 16; Al = 27; N = 14; H = 1; P = 31; S = 32; Cu = 64; Fe = 56; )
Bài 1: Tính thành phần phần trăm (theo khối lượng) của các nguyên tố hóa học trong các hợp chất sau:
1) MgCO3 2) Al(OH)3 3) (NH4)2HPO4 4) C2H5COOCH3
Bài 2:
a,Chất nào có phần trăm khối lượng của nguyên tố sắt lớn nhất, nhỏ nhất trong các công thức hóa học sau: FeO; Fe2O3; FeS; FeS2.
b,Chất nào sau đây có phần trăm khối lượng oxi lớn nhất, nhỏ nhất: NO2; NO; N2O; N2O3.
c,Chất nào có phần trăm khối lượng của nguyên tố sắt lớn nhất, nhỏ nhất trong các công thức hóa học sau: AlCl3; Al2O3; AlBr3; Al2S3.
Bài 1:
\(1,M_{MgCO_3}=84(g/mol)\\ \begin{cases} \%_{Mg}=\dfrac{24}{84}.100\%=28,57\%\\ \%_{C}=\dfrac{12}{84}.100\%=14,29\%\\ \%_{O}=100\%-28,57\%-14,29\%=57,14\% \end{cases}\)
\(2,M_{Al(OH)_3}=78(g/mol)\\ \begin{cases} \%_{Al}=\dfrac{27}{78}.100\%=31,62\%\\ \%_{H}=\dfrac{3}{78}.100\%=3,85\%\\ \%_{O}=100\%-31,62\%-3,85\%=64,53\% \end{cases}\)
\(3,M_{(NH_4)_2HPO_4}=132(g/mol)\\ \begin{cases} \%_{N}=\dfrac{28}{132}.100\%=21,21\%\\ \%_{H}=\dfrac{9}{132}.100\%=6,82\%\\ \%_{P}=\dfrac{31}{132}.100\%=23,48\%\\ \%_{O}=100\%-23,48\%-6,82\%-21,21\%48,49\% \end{cases}\)
\(4,M_{C_2H_5COOCH_3}=88(g/mol)\\ \begin{cases} \%_{C}=\dfrac{48}{88}.100\%=54,55\%\\ \%_{H}=\dfrac{8}{88}.100\%=9,09\%\\ \%_{O}=100\%-9,09\%-54,55\%=36,36\% \end{cases}\)
Đúng 3
Bình luận (0)
Bài 2:
\(c,\%_{Al(AlCl_3)}=\dfrac{27}{27+35,5.3}.100\%=20,22\%\\ \%_{Al(Al_2O_3)}=\dfrac{27.2}{27.2+16.3}.100\%=52,94\%\\ \%_{Al(AlBr_3)}=\dfrac{27}{27+80.3}.100\%=10,11\%\\ \%_{Al(Al_2S_3)}=\dfrac{27.2}{27.2+32.3}.100\%=36\%\)
Vậy \(Al_2O_3\) có \(\%Al\) cao nhất và \(AlBr_3\) có \(\%Al\) nhỏ nhất
Đúng 3
Bình luận (0)
Bài 2:
\(a,\%_{Fe(FeO)}=\dfrac{56}{56+16}.100\%=77,78\%\\ \%_{Fe(Fe_2O_3)}=\dfrac{56.2}{56.2+16.3}.100\%=70\%\\ \%_{Fe(FeS)}=\dfrac{56}{56+32}.100\%=63,64\%\\ \%_{Fe(FeS_2)}=\dfrac{56}{56+32.2}=46,67\%\)
Vậy \(FeO\) có \(\%Fe\) lớn nhất và \(FeS_2\) có \(\%Fe\) thấp nhất
\(b,\%_{O(NO_2)}=\dfrac{16}{16.2+14}.100\%=69,57\%\\ \%_{O(NO)}=\dfrac{16}{16+14}.100\%=53,33\%\\ \%_{O(N_2O)}=\dfrac{16}{14.2+16}.100\%=36,36\%\\ \%_{O(N_2O_3)}=\dfrac{16.3}{14.2+16.3}.100\%=63,16\%\)
Vậy \(NO_2\) có \(\%O\) lớn nhất và \(N_2O\) có \(\%O\) nhỏ nhất
Đúng 1
Bình luận (0)
1/ a. Một loại phân đạm có công thức (NH4)2SO4 em hãy tính phần trăm theo khối lượng của các nguyên tố trong hợp chất ?b/ Tính khối lượng nguyên tố dinh dưỡng N có trong 20kg phân đạm trên? (N 14; H1; S32; O16)
Đọc tiếp
1/ a. Một loại phân đạm có công thức (NH4)2SO4 em hãy tính phần trăm theo khối lượng của các nguyên tố trong hợp chất ?
b/ Tính khối lượng nguyên tố dinh dưỡng N có trong 20kg phân đạm trên? (N= 14; H=1; S=32; O=16)
\(a.\%m_N=\dfrac{14.2}{\left(14+4.1\right).2+32+4.16}.100\approx21,212\%\\ \%m_H=\dfrac{4.2}{\left(14+4.1\right).2+32+4.16}.100\approx6,061\%\\ \%m_S=\dfrac{32}{\left(14+4.1\right).2+32+4.16}.100\approx24,242\%\\ \%m_O=\dfrac{4.16}{\left(14+4.1\right).2+32+4.16}.100\approx48,485\%\)
\(b.m_{N\left(20kg\right)}=20.\dfrac{2.14}{\left(14+4.1\right).2+32+4.16}.100\%\approx4,2424\left(kg\right)\)
Đúng 2
Bình luận (0)
Biết phân tử khối của hợp chất A là 400 đvC và A có thành phần theo khối lượng các nguyên tố như sau: 28% Fe, 24% S, còn lại là O. a. Xác định công thức phân tử của hợp chất A? biết trong hợp chất xuất hiện nhóm SO4 b. Tính lượng sắt có trong 8 gam X?
Câu 2: Tính thành phần % về khối lượng các nguyên tố trong hợp chất: SO3, K2
Câu 3: Viết công thức hóa học của hợp chất gồm:
a) Zinc (kẽm) và chlorine (clo)
b) Barium (bari) và nhóm (NO3)
c) Aluminium (nhôm) và nhóm (SO4)
Câu 2:
\(a,\%S=\dfrac{m_S}{M_{SO_2}}=\dfrac{32}{80}=40\%\\ \%O=100\%-\%S=100\%-40\%=60\%\)
\(b,\%K=\dfrac{m_K}{M_{K_2}}=\dfrac{78}{78}=100\%\) (mik cũng thấy lạ là sao K là kim loại mà CTHH là K2 nhỉ ((: )
Câu 3:
\(a,CTHH.chung:Zn_xCl_y\\ Theo.quy.tắc.hóa.trị,ta.có:x.II=y.I\\ Chuyển.thành.tỉ.lệ:\dfrac{x}{y}=\dfrac{1}{2}\Rightarrow\left\{{}\begin{matrix}x=1\\y=2\end{matrix}\right.\\ CTHH:ZnCl_2\)
\(b,CTHH.chung:Ba_x\left(SO_4\right)_y\\ Theo.quy,tắc.hóa.trị,ta.có:x.II=y.II\\ Chuyển.thành.tỉ.lệ:\dfrac{x}{y}=\dfrac{2}{2}=\dfrac{1}{1}\Rightarrow\left\{{}\begin{matrix}x=1\\y=1\end{matrix}\right.\\ CTHH:BaSO_4\)
\(c,CTHH.chung:Al_x\left(SO_4\right)_y\\ Theo.quy.tắc.hóa.trị,ta.có:x.III=y.II\\ Chuyển.thành.tỉ.lệ:\dfrac{x}{y}=\dfrac{2}{3}\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\\ CTHH:Al_2\left(SO_4\right)_3\)
Đúng 1
Bình luận (4)
Tìm CTHH của các hợp chất
a) Trong hợp chất A cứ 24 phần C kết hợp với 32 phần O theo khối lượng
b) Trong hợp chất B cứ 46 phần Na kết hợp với 16 phần O theo khối lượng
c) Trong hợp chất C cứ 32 phần Cu kết hợp với 16 phần S và 32 phần O theo khối lượng (k )
\(a)\)
\(n_C=\frac{24}{12}=2mol\)
\(n_O=\frac{32}{16}=2mol\)
\(\frac{n_C}{n_O}=\frac{2}{2}=\frac{1}{1}\)
\(\rightarrow CTHH:CO\)
\(b)\)
\(n_{Na}=\frac{46}{23}=2\)
\(n_O=\frac{16}{16}=1\)
\(n_{Na}:n_O=2:1\)
\(\rightarrow CTHH:Na_2O\)
\(c)\)
\(n_{Cu}=\frac{32}{64}=0,5mol\)
\(n_S=\frac{16}{32}=0,5mol\)
\(n_O=\frac{32}{16}=2mol\)
\(n_{Cu}:n_S:n_O=0,5:0,5:2=1:1:4\)
\(\rightarrow CTHH:CuSO_4\)