Ở nhiệt độ cao, khí hiđro không phản ứng được với *
nước
khí oxi
sắt (II) oxit
đồng (II) oxit
nZn = 65/65 = 1 (mol)
Zn + 2HCl => ZnCl2 + H2
1__________________1
VH2 = 1 * 22.4 = 22.4 (l)
CuO + H2 -to-> Cu + H2O
______1_______1
mCu = 1*64 = 64 (g)
Cho 32,5 gam kẽm tác dụng hết với dung dịch axit clohidric HCl. a) Tính thể tích khí hiđro sinh ra (đktc). b) Tính khối lượng lượng muối kẽm clorua tạo thành ? c) Tính khối lượng lượng dd HCl 3,65% tham gia phản ứng ?d)Dùng toàn bộ lượng khí hidro thu được ở trên khử đồng (II) oxit , tính khối lượng kim loại đồng thu được.
Trong phòng thí nghiệm người ta dùng khí hidro để khử đồng (II) oxit ở nhiệt độ cao và thu được 12,8g kim loại đồng. a. Hãy lập phương trình phản ứng trên b. Tính thể tích khí hiđro đã dùng (đktc)? c. Tính khối lượng đồng (II) oxit đã tham gia phản ứng?
a) nCu=0,2(mol)
PTHH: CuO + H2 -to-> Cu + H2O
b) nH2=nCuO=nCu=0,2(mol)
=>V(H2,đktc)=0,2.22,4=4,48(l)
c) mCuO=0,2.80=16(g)
Cho 12,8 gam Đồng tác dụng vừa đủ với khí Oxi ở nhiệt độ cao, thu được Đồng (II) oxit.
a. Tính thể tích khí Oxi tham gia phản ứng (ở đktc)?
b. Tính khối lượng Đồng (II) oxit được tạo thành?
a) \(n_{Cu}=\dfrac{12,8}{64}=0,2\left(mol\right)\)
PTHH: 2Cu + O2 --to--> 2CuO
0,2-->0,1------->0,2
=> VO2 = 0,1.22,4 = 2,24 (l)
b) mCuO = 0,2.80 = 16 (g)
) Cho luồng khí Hiđro đi qua ống thuỷ tinh chứa 10 gam bột Đồng(II)oxit nung nóng ở nhiệt độ 400oC. Sau khi phản ứng kết thúc thu được 8,4 gam chất rắn. a. Nêu hiện tượng xảy ra? b.Tính hiệu suất phản ứng? c.Tính thể tích khí hiđro tham gia phản ứng ở đktc?
Hiện tượng: Chất rắn màu đen(CuO) dần chuyển sang màu nâu đỏ(Cu)
CuO+H2->Cu+H2O
Gọi a là số mol H2
Ta có
10-80a+64a=8,4
=>a=0,1 mol
=>VH2=0,1x22,4=2,24 l
a) Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp?.
b) Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
c) Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,8g sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxit và sắt (III) oxit là bao nhiêu?
a) Phương trình hóa học của các phản ứng:
H2 + CuO → Cu + H2O (1).
3H2 + Fe2O3 → 2Fe + 3H2O (2).
b) Trong phản ứng (1), (2) chất khử H2 vì chiếm oxi của chất khác, chất oxi hóa là CuO và Fe2O3 vì nhường oxi cho chất khác.
c) Khối lượng đồng thu được từ 6g hỗn hợp 2 kim loại thu được:
mCu = 6g - 2,8g = 3,2g, nCu = 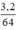 = 0,05 mol
= 0,05 mol
nFe = 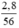 = 0,05 (mol)
= 0,05 (mol)
nH2 (1) = nCu = 0,05 mol ⇒ VH2(1) = 22,4 . 0,05 = 1,12 lít
nH2 (2) = 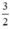 . nFe =
. nFe = 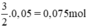 ⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
VH2 = VH2(1) + VH2(2) = 1,12 + 1,68 = 2,8(l)
Khử hết 4 gam đồng (II) oxit bằng khí hiđro ở nhiệt độ cao. Thể tích khí hiđro (ở đktc) cần dùng là
PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
Ta có: \(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)=n_{H_2}\) \(\Rightarrow V_{H_2}=0,05\cdot22,4=1,12\left(l\right)\)
Cho luồng khí hiđro đi qua ống thuỷ tinh chứa 20 g bột đồng (II) oxit ở 4000C. Sau phản ứng thu được 16,8 g chất rắn.
a) Nêu hiện tượng phản ứng xảy ra.
b) Tính hiệu suất phản ứng.
c) Tính số lít khí hiđro đã tham gia khử đồng (II) oxit trên ở đktc.
Hãy viết phương trình hóa học của các phản ứng giữa khí hidro với hỗn hợp đồng II oxit và sắt III oxit ở nhiệt độ cao Nếu thu được 6g hỗn hợp 2 kim loại trong đó có 2,8g sắt thì thể tích đktc khí hidro vửa đủ cần dùng để khử đồng II oxit và sắt III oxit là bao nhiêu ?
\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\)
\(\Rightarrow m_{Cu}=6-2,8=3,2g\)\(\Rightarrow n_{Cu}=0,05mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,05 0,05
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,075 0,05
\(\Rightarrow\Sigma n_{H_2}=0,075+0,05=0,125mol\)
\(\Rightarrow V=0,125\cdot22,4=2,8l\)
Dùng khí hiđro để khử toàn bộ hỗn hợp gồm 24,0 gam đồng(II)oxit và 16,0 gam sắt(III)oxit ở nhiệt độ cao. Thể tích khí hiđro (ở đktc) dùng để khử hết hỗn hợp oxit trên là
`CuO+ H_2 -> Cu+ H_2O`
`0,03 ----0,03` mol
`Fe_2O_3+ 3H_2 ->2Fe + 3H_2O`
`0,1-------0,3` mol
`n_(CuO) = 2,4/80 =0,03` mol
`n_(Fe_2O_3)=16/160 =0,1` mol
`=> V_(H_2)=(0,3+0,03).22,4=7,392 l`