công thức hóa học của oxit sắt biết tỉ lệ khối lượng của 2 nguyên tố sắt và oxi là 7:3
Một oxit được tạo bởi 2 nguyên tố là sắt và oxi, trong đó tỉ lệ khối lượng giữa sắt và oxi là 7/3. Công thức hoá học của oxit sắt là:
A. FeO
B. F e 2 O 3
C. F e 3 O 4
D. Fe O 2
Chọn B
Tỉ lệ khối lượng giữa Fe và O là 7/3
=> Đặt khối lượng của Fe là 7 thì khối lượng của O là 3

1.Tỷ lệ khối lượng của nitơ và oxi trong một oxit là 7 : 20. Công thức của oxit là? (Đáp án là N2O5)
2.Một loại sắt oxit có tỉ lệ khối lượng mFe : mO = 7 : 2. Công thức hóa học của oxit là
3.Cho oxit của nguyên tố R hóa trị IV, trong đó R chiếm 46,7% theo khối lượng. Công thức của oxit đó là
(Nhờ các bạn, thầy, cô hướng dẫn)
1. Gọi CTHH của oxit là NxOy.
Ta có: \(\dfrac{m_N}{m_O}=\dfrac{7}{20}\Rightarrow\dfrac{n_N}{n_O}=\dfrac{7}{20}:\dfrac{14}{16}=\dfrac{2}{5}\)
⇒ x:y = 2:5
→ N2O5
2. Gọi CTHH cần tìm là FexOy.
\(\Rightarrow\dfrac{m_{Fe}}{m_O}=\dfrac{7}{2}\Rightarrow\dfrac{n_{Fe}}{n_O}=\dfrac{7}{2}:\dfrac{56}{16}=1\)
⇒ x:y = 1
→ FeO
3. CTHH cần tìm: RO2
Mà: %R = 46,7%
\(\Rightarrow\dfrac{M_R}{M_R+16.2}.100\%=46,7\%\)
⇒ MR = 28 (g/mol)
→ SiO2
Một oxit được tạo bởi 2 nguyên tố sắt và oxi trong đó tỉ lệ khối lượng giữa sắt và oxi là 7/3. Tìm công thức phân tử của oxit đó.
Gọi công thức hóa học của oxit sắt là: F e x O y :
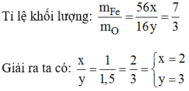
Công thức hóa học: F e 2 O 3 .
Bài 14: Một oxit được tạo bởi 2 nguyên tố sắt và oxi trong đó tỉ lệ khối lượng của hai nguyên tố sắt và oxi bằng 7 : 3. Tìm công thức phân tử của oxit đó.
CTPT: FexOy
Có: \(\dfrac{m_{Fe}}{m_O}=\dfrac{56x}{16y}=\dfrac{7}{3}\)
=> \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTPT: Fe2O3
Gọi CTHH là \(Fe_xO_y\)
\(x:y=\dfrac{m_{Fe}}{56}:\dfrac{m_O}{16}=\dfrac{7}{56}:\dfrac{3}{16}=\dfrac{1}{8}:\dfrac{3}{16}=1:\dfrac{3}{2}=2:3\)
\(\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\Rightarrow Fe_2O_3\)
CTHH: FexOy
\(\dfrac{m_{Fe}}{m_O}=\dfrac{7}{3}\Leftrightarrow\dfrac{56x}{16y}=\dfrac{7}{3}\Leftrightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
CTHH Fe2O3
1) xác định công thức hóa học của nhôm oxit, biết tỉ lệ khối lượng của 2 nguyên tố nhôm và oxit bằng 9 : 8.
2) Một oxít của lưu huỳnh trong đó có oxi chiếm 60 phần trăm về khối lượng. Tìm công thức phân tử của oxit đó?
3) Cho 11,2 gam sắt vào 200 ml dung dịch H2SO4 2M. Hãy:
a) Tính lượng khí H2 tạo ra ở đktc ?
b) Chất nào còn dư sau phản ứng và lượng dư là bao nhiêu ?
c) Tính nồng độ của các chất sau phản ứng ?
1.\(\dfrac{m_{Al}}{m_O}=\dfrac{9}{8}\)
\(Al_xO_y\)
\(x:y=\dfrac{9}{27}:\dfrac{8}{16}=\dfrac{1}{3}:\dfrac{1}{2}=2:3\)
Vậy CTHH là \(Al_2O_3\)
2.\(\rightarrow\%S=100-60=40\%\)
\(S_xO_y\)
\(x:y=\dfrac{40}{32}:\dfrac{60}{16}=1,25:3,75=1:3\)
Vậy CTHH là \(SO_3\)
3.
a.b.
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(n_{H_2SO_4}=2.0,2=0,4mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 < 0,4 ( mol )
0,2 0,2 0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
Chất dư là H2SO4
\(m_{H_2SO_4\left(dư\right)}=\left(0,4-0,2\right).98=19,6g\)
c.Nồng độ gì bạn nhỉ?
Câu 9: (3,0 điểm)
a. Viết phương trình hóa học biểu diễn sự cháy của các chất sau trong khí oxi: đồng,
nhôm, lưu huỳnh, butan (C4H10)
b. Một oxit được tạo bởi 2 nguyên tố sắt và oxi trong đó tỉ lệ khối lượng giữa sắt và
oxi là 7:3. Tìm công thức phân tử của oxit đó.
a)\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(C_4H_{10}+\dfrac{13}{2}O_2\underrightarrow{t^o}4CO_2+5H_2O\)
b)Gọi CTHH là \(Fe_xO_y\)
\(x:y=\dfrac{m_{Fe}}{56}:\dfrac{m_O}{16}=\dfrac{7}{56}:\dfrac{3}{16}=0,125:0,1875=2:3\)
\(\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\Rightarrow Fe_2O_3\)
Tỉ lệ khối lượng của sắt và oxi trong một oxit của sắt là 7:3 . Công thức của oxit là
\(\dfrac{m_{Fe}}{m_{O_2}}=\dfrac{7}{3}\)
\(CTĐG:Fe_xO_y\)
\(\Rightarrow x:y=\dfrac{7}{56}:\dfrac{3}{16}\)
\(=0,125:0,1875\)
\(=2:3\)
Vậy CTHH là: \(Fe_2O_3\)
CTHH: FexOy
mFe/mO = 7/3
=> 56x/16y = 7/3
=> x/y = 7/3 . 16/56 = 2/3
CTHH: Fe2O3
Trong 1 hợp chất có 2 thành phần gồm 2 nguyên tố là sắt và oxi.Trong đó sắt chiếm 70% về khối lượng của hợp chất.Tìm tỉ lệ số nguyên tử sắt và oxi trong hợp chất.Từ đó ,viết công thức hóa học của hợp chất.
Gọi CTHH của oxit sắt : \(Fe_xO_y\)
Ta có :
\(\dfrac{56x}{70} = \dfrac{16y}{30}\\ \Rightarrow \dfrac{x}{y} = \dfrac{2}{3}\)
Tỉ lệ số nguyên tử sắt : số nguyên tử O là 2 : 3
Với x = 2 ; y = 3 thì thỏa mãn
Vậy CTHH của hợp chất cần tìm : Fe2O3
7. Xác định công thức hóa học của nhôm oxit, biết tỉ lệ khối lượng của 2 nguyên tố nhôm và oxi bằng 9 : 8.
Ta có; \(n_{Al}:n_O=\dfrac{9}{27}:\dfrac{8}{16}=2:3\)
\(\Rightarrow\) CTHH là Al2O3
7.
gọi CTHH của nhôm oxi là \(Al_xD_8\)
có :\(\dfrac{27x}{16y}=\dfrac{9}{8}\)
\(\dfrac{x}{y}=\dfrac{2}{3}\)
\(\rightarrow Al_2O_3\)
Ta có; =2:3nAl:nO=927:816=2:3
=> CTHH là Al2O3