Cho hóa học a gồm fe và cu vào 200ml dd hóa chất 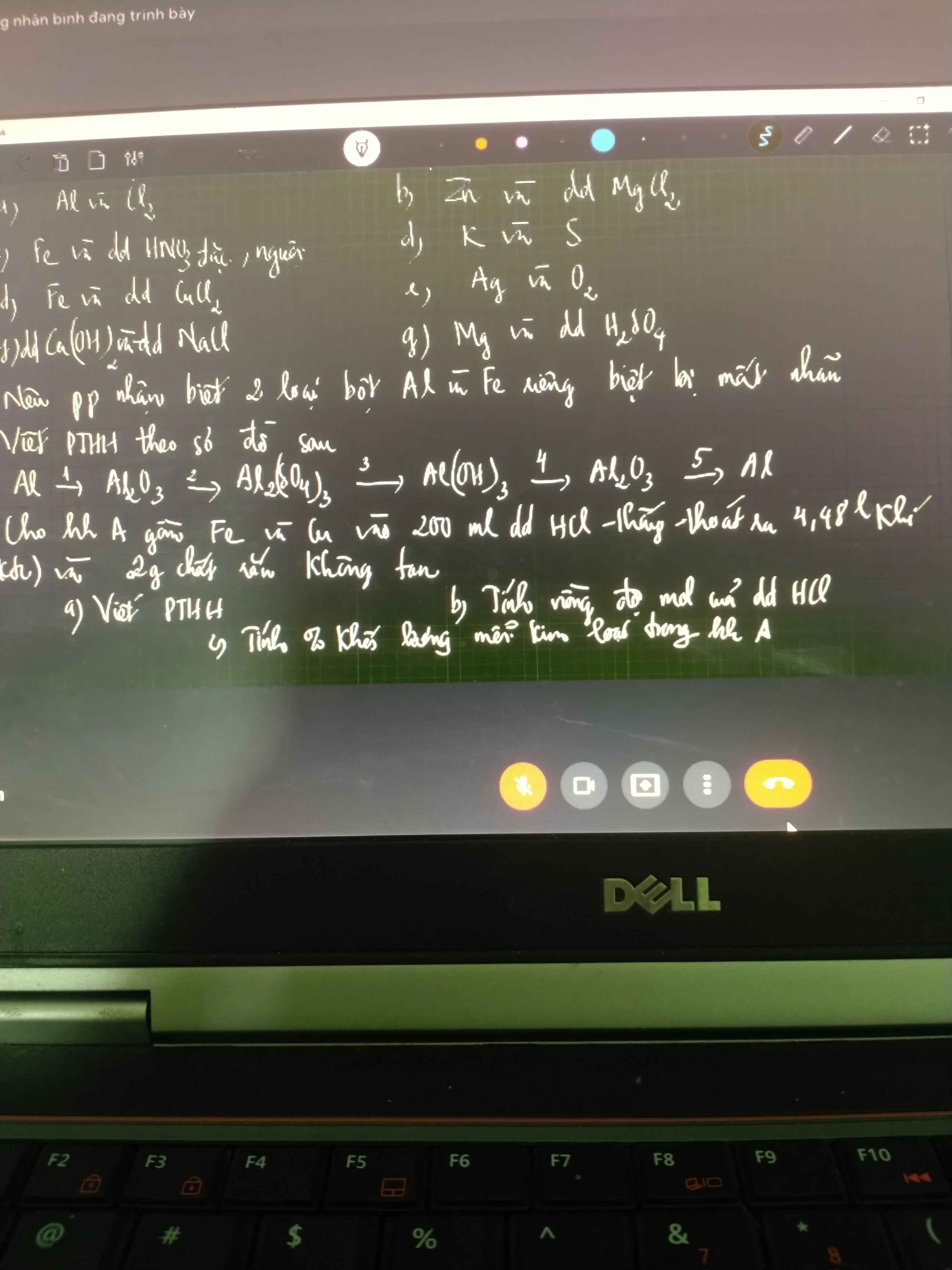
NT
Những câu hỏi liên quan
Cho 12g hỗn hợp x gồm Fe và Cu vào 200ml dd HNO3 2M, thu được 1 chất khi(sản phẩm khử duy nhất)không màu, hóa nâu trong không khí, dd Y và còn lại 2,8g một chất rắn.Cô cạn Y rồi nung nóng chất rắn còn lại trong bình kín đến khối lượng ko đổi thì thu được m g chất rắn.giá trị của m là
Còn 2,8g cran → Cu dư =2,8g → Fe và Cu pư với HNO3 hết 9,2g
Vì NO là sản phẩm khử duy nhất → mol H+=4mol NO →mol NO= 0,1,
Áp dụng bt KL và bt E cho pư Fe,Cu ta có :\(\begin{cases}56x+64y=9,2\\2x+2y=0,3\end{cases}\)→mol Fe: 0,05 và mol Cu pư=0,1
Cr thu đk sau khi nung :FeO và CuO tính đk mg=11,6
Đúng 0
Bình luận (0)
Cho m gam hỗn hợp gồm Fe và Al ở dạng bột vào 200ml dd CuSO4 0,525M. Khuấy kỹ hỗn hợp để các phản ứng hóa học xảy ra hoàn toàn. Sau phản ứng thu được 7,84g chất rắn A gồm 2 kim loại và dung dịch B. Để hòa tan hoàn toàn chất rắn A cần dùng ít nhất bao nhiêu ml dd HNO3 2M, biết rằng phản ứng sinh ra sản phẩm khử duy nhất là NO? A. 211,12 ml B. 221,13 ml C. 166,67 ml D. 233,33 ml
Đọc tiếp
Cho m gam hỗn hợp gồm Fe và Al ở dạng bột vào 200ml dd CuSO4 0,525M. Khuấy kỹ hỗn hợp để các phản ứng hóa học xảy ra hoàn toàn. Sau phản ứng thu được 7,84g chất rắn A gồm 2 kim loại và dung dịch B. Để hòa tan hoàn toàn chất rắn A cần dùng ít nhất bao nhiêu ml dd HNO3 2M, biết rằng phản ứng sinh ra sản phẩm khử duy nhất là NO?
A. 211,12 ml
B. 221,13 ml
C. 166,67 ml
D. 233,33 ml
Đáp án C.
Chất rắn sau phản ứng gồm 2 kim loại → 2 kim loại đó là Cu và Fe , Al đã phản ứng hết → CuSO4 không dư → nCu = 0,105 mol => m= 6,72 gam → còn 1,12 gam là của Fe .
Phản ứng : Fe + 4HNO3 → Fe(NO3)3 + NO +2H2O
nFe = 0,02 mol → nHNO3= 0,08 mol .
n F e 3 + = 0,02 mol
chú ý phản ứng: Cu + 2Fe3+ → Cu2+ + 2Fe2+
⇒ 0,01 mol Cu + 0,02 mol Fe3+ → 0,01 mol Cu2+ và 0,02 mol Fe2+ )
Để HNO3 cần dùng là tối thiểu thì cần dùng 1 lượng hòa tan vừa đủ 0,105 – 0,01 = 0,095 mol Cu
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Từ đây tính được nHNO3= 0,095. 8 3 = 0,253 mol
→ tổng nHNO3 đã dùng là 0,253 + 0,08 = 0,333 mol
→ = 0,16667 lít = 166,67 ml
Đúng 0
Bình luận (0)
a. Tính hóa trị của Cu, Fe, N, S, trong các hợp chất sau: Cu2O, Fe2O3, Fe(NO3)3, N2O, SO3. b. Vận dụng quy tắc hóa trị hãy lập công thức hóa học của các hợp chất sau: * Lưu huỳnh oxit (gồm crom có hóa trị VI và oxi) * Canxi sunfat (gồm Ca và nhóm SO4)
a, Hóa trị của Cu trong hc Cu2O là I
Hóa trị của Fe trong hc Fe2O3 là III
Hóa trị của Fe trong hc Fe(NO3)3 là III
Hóa trị của N trong hc N2O là IV
Hóa trị của S trong hc SO3 là VI
b, CTHH: SO3
CTHH: CaSO4
Đúng 1
Bình luận (0)
hòa tan 12gam hỗn hợp A gồm Mg, MgO và Cu bằng 200ml dd H2SO4 loãng vừa đủ thì có 4,48 lít khí hidro ( đktc) thoát ra, thu được đ B và 3,2 gam chất rắn ko tan.a) Viết các phtrinh hóa học xảy ra b) Tính klg các chất trong hỗn hợp Ac) tính nồng độ mol của dd axit H2SO4 dđđãđã ddudundungdùngdùngd) tính nồg độ mol của muối sunfat thu đc , biết dd sau phản ứng có thể tích ko đổi giúppp mikk vs plsss
Đọc tiếp
hòa tan 12gam hỗn hợp A gồm Mg, MgO và Cu bằng 200ml dd H2SO4 loãng vừa đủ thì có 4,48 lít khí hidro ( đktc) thoát ra, thu được đ B và 3,2 gam chất rắn ko tan.
a) Viết các phtrinh hóa học xảy ra
b) Tính klg các chất trong hỗn hợp A
c) tính nồng độ mol của dd axit H2SO4 dđđãđã ddudundungdùngdùng
d) tính nồg độ mol của muối sunfat thu đc , biết dd sau phản ứng có thể tích ko đổi
giúppp mikk vs plsss
B1: Thực hiện chuyển đổi hóa học theo sơ đồ:
a) Cu -> CuO -> CuCl2 -> Cu(OH)2 -> CuSO4
b) Mg -> MgCl2 -> Mg(NO3)2 -> MgSO4 -> MgCO3 -> MgO
B2: Bằng phương pháp hóa học, hãy phân biệt các dd mất nhãn sau: NaOH, Na2SO4, HCl, H2SO4, Ba(OH)2, NaCl.
B3: Cho 9,1gam hỗn hợp MgO và Al2O3 tác dụng vừa đủ với 200ml dd HCl nồng độ 2,5M
a) Viết PTHH
b) Tính khối lượng của mỗi chất trong hỗn hợp ban đầu.
Xem chi tiết
gvvvvvvvvvvvvvvvvvvvvvvvvvvft
Cho m gam hỗn hợp A gồm Fe và Mg tác dụng với dd HCl dư thu được 3,808 lít H2(đktc). Mặt khác nếu cho m gam hỗn hợp A vào 200ml dd chứa AgNO3 0,5M và Cu(NO3)2 0,8M; phản ứng xong, lọc bỏ phần chất rắn thu được dd B chứa ba muối. Khi thêm dd NaOH dư vào dd B rồi lọc bỏ kết tủa trong không khí đến khối lượng không đổi thu được 10,4g chất rắn. Tính giá trị của m và khối lượng mỗi muối trong dd B.
Đọc tiếp
Cho m gam hỗn hợp A gồm Fe và Mg tác dụng với dd HCl dư thu được 3,808 lít H2(đktc). Mặt khác nếu cho m gam hỗn hợp A vào 200ml dd chứa AgNO3 0,5M và Cu(NO3)2 0,8M; phản ứng xong, lọc bỏ phần chất rắn thu được dd B chứa ba muối. Khi thêm dd NaOH dư vào dd B rồi lọc bỏ kết tủa trong không khí đến khối lượng không đổi thu được 10,4g chất rắn. Tính giá trị của m và khối lượng mỗi muối trong dd B.
QT cho electron:
Fe → Fe2+ + 2e
Mg → Mg2+ + 2e
QT nhận electron:
Ag+ + 1e → Ag
Cu2+ + 2e → Cu
Ta có: nAgNO3= 0,1 mol; nCu(NO3)2= 0,16 mol; nH2= 0,17 mol
Nhìn chung qua quá trình phản ứng thì 3 muối còn lại sẽ là: Cu(NO3)2dư, Fe(NO3)2; Mg(NO3)2 và các kim loại Mg, Fe đều phản ứng hết.
Sơ đồ phản ứng tiếp theo:
⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩Mg(NO3)2 xFe(NO3)2 yCu(NO3)2NaOH−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩Mg(OH)2Fe(OH)2Cu(OH)2O2,to−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩MgO x1/2Fe2O3 y/2CuO
Ta có các PT: nH2 = x + y = 0,17
mchất rắn = 40x + 80y + 80z = 10,4 g
Bảo toàn số mol nguyên tử N trong các muối:
nN-AgNO3 + nN-Cu(NO3)2 = nN-Fe(NO3)2 + nN-Mg(MO3)2
Þ 0,1.1 + (0,16 – z).2 = 2x + 2y
Từ đó giải ra x = 0,16; y = 0,01; z = 0,04
=> m = 0,16.24 + 0,01.56 = 4,4 gam.
Khối lượng các muối là: 23,68g; 1,8g; 7,52 g
Muối có phân tử khối lớn nhất trong B là Cu(NO3)2 0,04 mol có khối lượng là 7,52 gam
Đúng 0
Bình luận (2)
Có các thí nghiệm sau: -TN1: Cho hơi nước đi qua ống đựng bột sắt nung nóng. -TN2: Cho đinh sắt nguyên chất vào dd H2SO4 loăng có nhỏ thêm vài giọt dd CuSO4. -TN3: Để thanh thép trong không khí ẩm -TN4: Nhúng lá kẽm nguyên chất vào dd CuSO4. -TN5: Thanh Fe có quấn dây Cu và để ngoài không khí ẩm. -TN6: Hợp kim Ag-Cu nhúng vào dd HCl -TN7: Hợp kim Zn-Cu nhúng vào dd NaOH -TN8: Sắt mạ thiếc nhúng vào dd HCl Số trường hợp xảy ra ăn mòn điện hóa học là A. 6 B. 3 C. 4 D. 5
Đọc tiếp
Có các thí nghiệm sau:
-TN1: Cho hơi nước đi qua ống đựng bột sắt nung nóng.
-TN2: Cho đinh sắt nguyên chất vào dd H2SO4 loăng có nhỏ thêm vài giọt dd CuSO4.
-TN3: Để thanh thép trong không khí ẩm
-TN4: Nhúng lá kẽm nguyên chất vào dd CuSO4.
-TN5: Thanh Fe có quấn dây Cu và để ngoài không khí ẩm.
-TN6: Hợp kim Ag-Cu nhúng vào dd HCl
-TN7: Hợp kim Zn-Cu nhúng vào dd NaOH
-TN8: Sắt mạ thiếc nhúng vào dd HCl
Số trường hợp xảy ra ăn mòn điện hóa học là
A. 6
B. 3
C. 4
D. 5
Cho hh X 11,2g gồm Fe và oxit MO( hóa trị M không đổi) td vs 200ml dd HCl 2M ( vừa đủ ) . Tìm M
Ta có: \(n_{HCl}=2.\dfrac{200}{1000}=0,4\left(mol\right)\)
PTHH:
\(Fe+2HCl--->FeCl_2+H_2\uparrow\left(1\right)\)
\(MO+2HCl--->MCl_2+H_2O\left(2\right)\)
Gọi x, y lần lượt là số mol của Fe và MO
Theo PT(1): \(n_{HCl}=2.n_{Fe}=2x\left(mol\right)\)
Theo PT(2): \(n_{HCl}=2.n_{MO}=2y\left(mol\right)\)
\(\Rightarrow2x+2y=0,4\) (*)
Theo đề, ta có: \(56x+My+16y=11,2\) (**)
Từ (*) và (**), ta có:
\(\left\{{}\begin{matrix}2x+2y=0,4\\56x+16y+My=11,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}16x+16y=3,2\\56x+16y+My=11,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}40x+My=8\\2x+2y=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}40x+My=8\\40x+40y=8\end{matrix}\right.\Leftrightarrow M=40\)
Vậy M là nguyên tử canxi (Ca)
Đúng 1
Bình luận (0)
1.Hòa tan 100g dd K2SO3 nồng độ 21,6% vào 200ml dd H2SO4(D=1,04g/ml)
a)Tính khối lượng chất dư sau phản ứng
b)Tính nồng độ % các chất tan sau phản ứng
2.Hóa tan hoàn toàn 11g hỗn hợp gồm Fe và Al bằng 1 lượng dd H2SO4 2M(vừa đủ) người ta thu được 8,96 lít khi ở đktc





