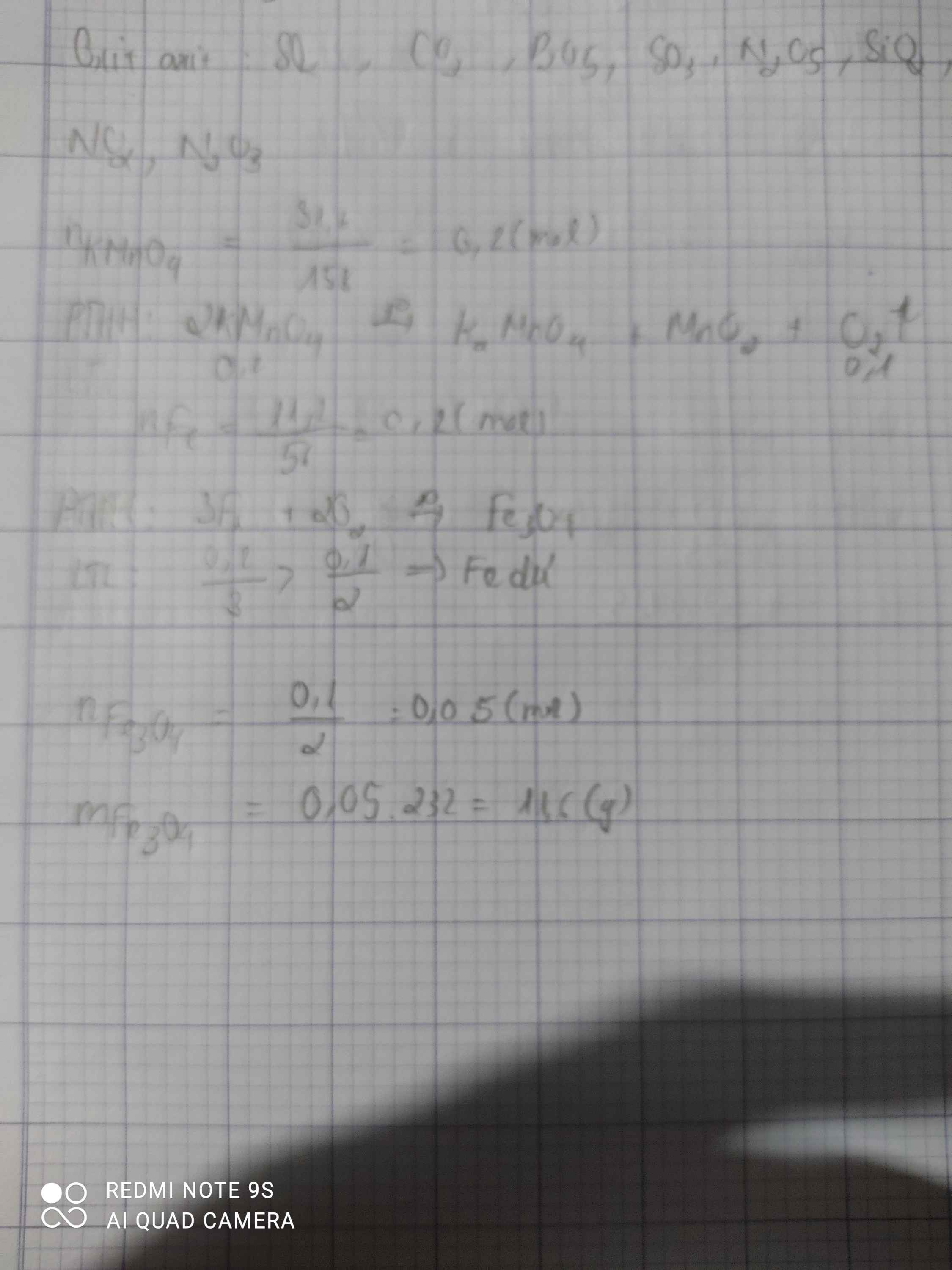Nhiệt phân 15,8g K M n O 4 thu được lượng khí O 2 , đốt cháy 5,6g Fe trong lượng khí O 2 vừa thu được thì sản phẩm sau phản ứng có bị cục nam châm hút không? Hãy giải thích
NN
Những câu hỏi liên quan
1- Nhiệt phân 12,25g KCLO₃ thu đc khí O₂.a) Viết PTHH.b) Tính thể tích khí oxi thu đc ở điều kiện tiêu chuẩn(đktc), biết hiệu suất phản ứng là 90%.c) Người ta tiến hành đốt cháy 5,6g Fe trong lượng khí O₂ vừa thu đc ở trên thì thu đc bao nhiêu gam oxit?2- Hòa tan A gam kim loại Zn trong dung dịch H₂SO₄ loãng, dư thu đc 0,448 lít khí (đktc). Tính A nếu biết hiệu suất phản ứng đạt 95%?
Đọc tiếp
1- Nhiệt phân 12,25g KCLO₃ thu đc khí O₂.
a) Viết PTHH.
b) Tính thể tích khí oxi thu đc ở điều kiện tiêu chuẩn(đktc), biết hiệu suất phản ứng là 90%.
c) Người ta tiến hành đốt cháy 5,6g Fe trong lượng khí O₂ vừa thu đc ở trên thì thu đc bao nhiêu gam oxit?
2- Hòa tan A gam kim loại Zn trong dung dịch H₂SO₄ loãng, dư thu đc 0,448 lít khí (đktc). Tính A nếu biết hiệu suất phản ứng đạt 95%?
1. a) PTHH: \(2KClO_3=2KCl+3O_2\)
b) Khối lượng \(KClO_3\) thực tế phản ứng:
\(H=\dfrac{m_{tt}}{m_{lt}}.100\%\Rightarrow m_{tt}=\dfrac{m_{lt}.H}{100\%}=11,025\left(g\right)\)
\(n_{KClO_3}=\dfrac{m_{KClO_3}}{M_{KClO_3}}=\dfrac{11,025}{122,5}=0,09\left(mol\right)\)
Theo PTHH: \(n_{O_2}=\dfrac{0,09.3}{2}=0,135\left(mol\right)\)
\(\Rightarrow V_{O_2}=n_{O_2}.22,4=0,135.22,4=3,024\left(l\right)\)
c) \(4Fe+3O_2\xrightarrow[t^o]{}2Fe_2O_3\)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Theo PTHH: \(n_{Fe_2O_3}=\dfrac{0,1.2}{4}=0,05\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=n_{Fe_2O_3}.M_{Fe_2O_3}=0,05.160=8\left(g\right)\)
Đúng 3
Bình luận (0)
a)Ta có PTHH: 2KClO3 --t---> 2KCl + 3O2 (1)
b) Biết mKClO3 =12,25g => nKClO3 = mKClO3/MKClO3
=12,25/122,5=0,1 (mol)
Theo PT (1) ta có:
no2 =3/2 nKCLO3 =3/2 . 0,1= 0,15(mol)
Vậy VO2 = n . 22,4 = 0,15 . 22,4= 3,36 (L)
c) Ta có PTHH: 4Fe + 3O2 -----> 2Fe2O3 (2)
Biết mFe = 5,6 g => nFe = m/M= 5,6/56=0,1 (mol)
Theo PT (2) ta có :
nFe2O3 = 2/4 nFe = 2/4 .0,1=0,05 (mol)
Vậy mFe2O3 = n . M = 0,05 . 160= 8 (g)
Đúng 1
Bình luận (0)
Nhiệt phân 15,8gam KMnO₄ thu được lượng khí oxi, đốt cháy 5,6g sắt trong lượng khí oxi vừa thu được thì sản phẩm sau phản ứng có bin nam châm hút hay không ? Hãy giải thích?
nKMnO4=15,8/158=0,1 mol
2KMnO4 --> K2MnO4 + MnO2 + O2
0,1 0,05
nFe=5,6/56=0,1
3Fe + 2O2 -to--> Fe3O4
0,1 0,05 mol
ta thấy nFe/3=0,1/3 > nO2/2=0,05/2=0,025
=> Fe dư ,O2 hết => bin nam châm vẫn hút được hỗn hợp sau phản ứng
Đúng 0
Bình luận (0)
nhiệt phân 15,8 gam KMnO4 thu được lượng khí õi, đốt cháy 5,6g sắt trong lượng khí oxi vừa thu được thì sản phẩm sau phản ứng có bị nam châm hút hay không ? hãy giả thích ?
2KMnO4 \(\xrightarrow[]{t^o}\) K2MnO4 + MnO2 + O2(1)
3Fe + 2O2 \(\xrightarrow[]{t^o}\) Fe3O4(2)
nKMnO4 = 15,8 : 158 = 0,1 mol
nFe = 5,6 : 56 = 0,1 mol
Theo pt 1 nO2 = \(\dfrac{1}{2}nKMnO_4=0,05mol\)
Lập tỉ lệ phương trình (2)
nFe : nO2 = \(\dfrac{0,1}{3}:\dfrac{0,05}{2}\)
Do 0,1/3 > 0,05/2 => Fe dư
Vậy sản phẩm thu được có Fe dư => bị nam châm hút
Đúng 1
Bình luận (0)
Nhiệt phân hoàn toàn 31,6g KMnO4 để điều chế khí oxi trong phòng thí nghiệm
a. Tính thể tích khí oxi thu được ở đktc?
b. Đốt cháy 11,2g Fe với lượng khí O2 thu được ở trên. Tính khối lượng Fe từ oxi thu được sau phản ứng
a.\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{31,6}{158}=0,2mol\)
\(PTHH:2KMnO_4\underrightarrow{np}K_2MnO_4+MnO_2+O_2\)
2 1 1 1 ( mol )
0,2 0,1
\(V_{O_2}=n.22,4=0,1.22,4=2,24l\)
b.\(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
3 2 1 ( mol )
0,2 0,1
0,1 0,1 0,05 ( mol )
\(m_{Fe_3O_4}=n.M=0,05.232=11,6g\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 16,8gam sắt Fe trong không khí thu được oxit sắt từ (Fe₃O₄)
A) tính khối lượng oxit sắt từ( Fe₃O₄) thu được?
B) tính thể tích khí O₂ tham gia phản ứng ( ở Đktc)
C) hiếu đốt 16,8gam sắt Fe vào trong lọ đựng 3,36 lít khí O₂ ( ở đktc) thì số gam oxit sắt từ (Fe₃O₄) thu được là bao nhiêu
D) biếu tiếp tục dẫn oxit sắt từ Fe₃O₄ thu được đi qua 7,84 lít khí H₂ ( đktc) rồi đun nóng, thì chất dư và số gam chất khí dư là bao nhiêu
cho biết : Fe56 ; 016
Đọc tiếp
Đốt cháy hoàn toàn 16,8gam sắt Fe trong không khí thu được oxit sắt từ (Fe₃O₄) A) tính khối lượng oxit sắt từ( Fe₃O₄) thu được? B) tính thể tích khí O₂ tham gia phản ứng ( ở Đktc) C) hiếu đốt 16,8gam sắt Fe vào trong lọ đựng 3,36 lít khí O₂ ( ở đktc) thì số gam oxit sắt từ (Fe₃O₄) thu được là bao nhiêu D) biếu tiếp tục dẫn oxit sắt từ Fe₃O₄ thu được đi qua 7,84 lít khí H₂ ( đktc) rồi đun nóng, thì chất dư và số gam chất khí dư là bao nhiêu " cho biết : Fe=56 ; 0=16"
a.b.\(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,3 0,2 0,1 ( mol )
\(m_{Fe_3O_4}=0,1.232=23,2\left(g\right)\)
\(V_{O_2}=0,2.22,4=4,48\left(l\right)\)
c. \(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,3 > 0,15 ( mol )
0,225 0,15 0,075 ( mol )
\(m_{Fe_3O_4}=0,075.232=17,4\left(g\right)\)
d. \(n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
\(Fe_3O_4+4H_2\rightarrow\left(t^o\right)3Fe+4H_2O\)
0,075 < 0,35 ( mol )
0,075 0,3 ( mol )
Chất dư là H2
\(m_{H_2\left(dư\right)}=\left(0,35-0,3\right).2=0,1\left(g\right)\)
Đúng 1
Bình luận (0)
Đốt cháy 5,6g Fe trong bình chưa khí O2 thu được Fe3O4. a)Viết PTPỨ. b) Tính khối lượng KClO3 cần dùng.c)Tính thể tích khí O2 ở đktc đã phản ứng.
Xem chi tiết
nFe =0,1(mol)
a) PTHH: 3 Fe +2 O2 -to-> Fe3O4
0,1__________1/15____1/30(mol)
b) KClO3 cần dùng là sao?
Đúng 0
Bình luận (0)
Bài 10: Đốt cháy 16,8 g Fe trong khí Oxi vừa đủ thì thu được Fe 2 O 3. Cho toàn bộ lượng
Fe 2 O 3 tạo thành sau phản ứng này tác dụng với m (g) H 2 SO 4 .
a) Tìm thể tích khí Oxi để đốt cháy lượng sắt trên
b) Tìm m
Lưu ý: Có tóm tắt,có lời giải,giải chi tiết giúp mị .-.
a) PTHH: \(4Fe+3O_2\underrightarrow{t^o}2Fe_2O_3\)
Ta có: \(n_{Fe}=\dfrac{m}{M}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
PTPƯ: 4Fe + 3O2 \(\underrightarrow{t^o}\) 2Fe2O3
4 3 2
0,3 0,225 0,15
\(\Rightarrow V_{O_2}=n.24,79=0,225.24,79=5,57775\left(l\right)\)
Đúng 2
Bình luận (5)
TT:mFe=16.8g
a/Tìm VO2?
b/Tìm mH2SO4?
Giải:a/
PTHH: 4Fe+3O2__t°_>2Fe2O3
nFe=mFe/M=16.8/56=0,3mol
Theo PTHH:4molFe-->3molO2
0,3molFe-->nO2=0,3molFe.3/4=0,225mol
4molFE-->2molFe2O3
0,3molFe-->nFe2O3=0,3molFe.2/4=0,15mol
VO2=nO2.22,4=0,225.22,4=5,04l
b/PTHH:Fe2O3+3H2SO4->Fe2(SO4)3+3H2O
Theo PTHH:1molFe2O3-->3molH2SO4
0,15molFe2O3-->nH2SO4=0,15.3/1=0,45mol
mH2SO4=nH2SO4.M
=0,45.(2+32+16.4)
=44,1g
Giải vậy đc chưa bạn:)
Đúng 0
Bình luận (2)
Mong các bạn giúp đỡ!!Câu 13. Hãy so sánh nguyên tử Oxygen nặng, nhẹ hay bằng bao nhiêu lần nguyên tử He.(O16, He4).Câu 14. Đốt cháy hoàn toàn 5,6g Iron - Fe trong khí Chlorine –Cl2, sau phản ứng thu được 16,25g Iron (III) chloride. Tính khối lượng khí Cl2 đã dùngCâu 15. Điền chất còn thiếu vào chỗ trốnga. O2 + _____ à CuOb. Mg + CuSO4 à MgSO4 + _______Câu 16. Cho phương trình hóa học sau: Al2O3 + H2SO4 à Alx(SO4)y + H2OHãy xác định chỉ số x, yCâu 17. Tính khối lượng mol của của chất X. Biết rằn...
Đọc tiếp
Mong các bạn giúp đỡ!!
Câu 13. Hãy so sánh nguyên tử Oxygen nặng, nhẹ hay bằng bao nhiêu lần nguyên tử He.
(O=16, He=4).
Câu 14. Đốt cháy hoàn toàn 5,6g Iron - Fe trong khí Chlorine –Cl2, sau phản ứng thu được 16,25g Iron (III) chloride. Tính khối lượng khí Cl2 đã dùng
Câu 15. Điền chất còn thiếu vào chỗ trống
a. O2 + _____ à CuO
b. Mg + CuSO4 à MgSO4 + _______
Câu 16. Cho phương trình hóa học sau: Al2O3 + H2SO4 à Alx(SO4)y + H2O
Hãy xác định chỉ số x, y
Câu 17. Tính khối lượng mol của của chất X. Biết rằng 0,25 mol chất X nặng 40g.
Câu 18. Hãy so sánh khí CH4 nặng, nhẹ hay bằng không khí bao nhiêu lần.
(C=12, H=1).
Câu 19. Hãy tính số mol của 6,1975 lít khí CO2 ở đkc. (C=12, O=16)
Câu 20. Hãy tính thể tích của 12,6g khí N2 ở đkc. (N=14)
Mong các bạn giúp đỡ!!
Câu 13. Hãy so sánh nguyên tử Oxygen nặng, nhẹ hay bằng bao nhiêu lần nguyên tử He.
(O=16, He=4).
Câu 14. Đốt cháy hoàn toàn 5,6g Iron - Fe trong khí Chlorine –Cl2, sau phản ứng thu được 16,25g Iron (III) chloride. Tính khối lượng khí Cl2 đã dùng
Câu 15. Điền chất còn thiếu vào chỗ trống
a. O2 + _____ à CuO
b. Mg + CuSO4 à MgSO4 + _______
Câu 16. Cho phương trình hóa học sau: Al2O3 + H2SO4 à Alx(SO4)y + H2O
Hãy xác định chỉ số x, y
Đúng 0
Bình luận (1)
Xem thêm câu trả lời
1) Đốt cháy sắt thu được 0,3 mol Fe3O4.Tính thể tích khí oxi (ở đktc) đã dùng2) Đốt cháy sắt thu được 0,2 mol Fe3O4. Thể tích khí oxi (ở đktc ) đã dùng là bao nhiêu ?3) Trong x gam quặng sắt hematit có chứa 5,6g Fe. Khối lượng Fe2O3 có trong quặng đó là:4) Muốn điều chế được 3,36 lít oxi (đktc) thì khối lượngKMnO4 cần nhiệt phân là bao nhiêu, viết phương trình điều chế.5) Trong oxit, kim loại có hóa trị III và chiếm 70 phần trăm về khối lượng là:6) Cho 28,4g điphotpho pentaoxit P2O5 vào cốc chứa...
Đọc tiếp
1) Đốt cháy sắt thu được 0,3 mol Fe3O4.Tính thể tích khí oxi (ở đktc) đã dùng
2) Đốt cháy sắt thu được 0,2 mol Fe3O4. Thể tích khí oxi (ở đktc ) đã dùng là bao nhiêu ?
3) Trong x gam quặng sắt hematit có chứa 5,6g Fe. Khối lượng Fe2O3 có trong quặng đó là:
4) Muốn điều chế được 3,36 lít oxi (đktc) thì khối lượngKMnO4 cần nhiệt phân là bao nhiêu, viết phương trình điều chế.
5) Trong oxit, kim loại có hóa trị III và chiếm 70 phần trăm về khối lượng là:
6) Cho 28,4g điphotpho pentaoxit P2O5 vào cốc chứa 90g nước để tạo thành axit photphoric. Tính khới lượng axit H3PO4 được tạo thành ?
3Fe+2O2-to>Fe3O4
0,9-----0,6--------------0,3
=>VO2=0,6.22,4=13,44l
2
3Fe+2O2-to>Fe3O4
0,4--------0,2
=>VO2=0,4.22,4=8,96l
Đúng 3
Bình luận (0)