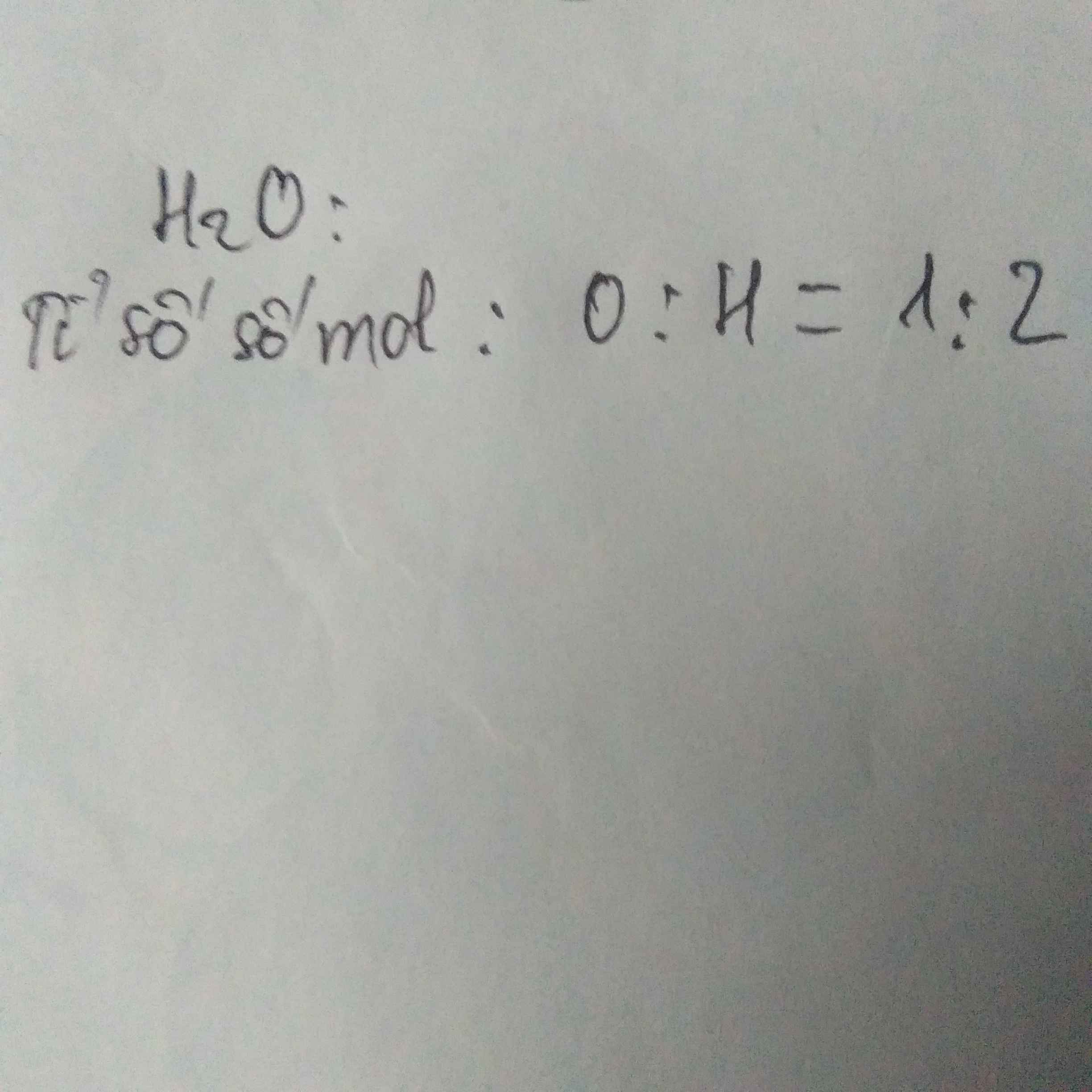Chứng minh CTHH của nước là H2O
PH
Những câu hỏi liên quan
nicotin là hợp chất gây nghiện có trong thuốc lá có hại cho sức khỏe đốt cháy 3,24g nicotin cần 6,048 l khí õi ở đktc thì thu đc 0,56 l khí nitow , khí co2,h2o biết nco2=10/7 n h2o
a, tính m nước vá co2 ở đktc
b, lập cthh của nicotin biết 203>M>122
Từ kết quả thực nghiệm: Khi điện phân nước thu được thể tích khí hiđro gấp 2 lần thể tích khí oxi(cùng điều kiện nhiệt độ, áp suất). Hãy chứng minh CTHH của nước.
khi điện phân nước chỉ thu được 2 sản phẩm là H2 và O2 chứng tỏ trong nước chỉ chứa 2 nguyên tố H và O
mặt khác khi điện phân nước, thể tích H2 thu được gấp 2 lần thể tích O2 thu được chứng tỏ một số mol nước điện phân sẽ thu được số mol H2 bằng 2 lần số mol O2 \(\Rightarrow\) số mol H trong 1 phân tử nước bằng 2 lần số mol O trong 1 phẩn tử nước
gọi CTTQ của nước là HxOy
x: y= nH: nO
= 2: 1
\(\Rightarrow\) CTHH: H2O
Đúng 0
Bình luận (0)
Chuotconbebong2004, Hoàng Nhất Thiên, Thảo Phương , Nguyễn Trương, buithianhtho, Toshiro Kiyoshi, muốn đặt tên nhưng chưa nghĩ ra bạn nào tốt nghĩ giùm mk, Nguyễn Thị Ngọc Ánh, Nguyen, Nguyễn Ngọc Lan, trần hữu tuyển, Hoàng Tuấn Đăng, Nguyễn Trần Thành Đạt, Phùng Hà Châu, Nguyễn Thị Minh Thương , Nguyễn Thị Kiều, Nguyễn Anh Thư, Võ Đông Anh Tuấn, Gia Hân Ngô, Hung nguyen,...
Đúng 0
Bình luận (0)
Trong CTHH H2O .Tỉ lệ số nguyên tử O và H lần lượt là:
Trong số các CTHH sau: Al2O3, O2, CuO, CO, Fe, H2O. Số hợp chất là
Hợp chất:CO2;Al 2(SO4)3; CuO;CuCl 2; H2O;Ca(NO3)2;Na2SO3; H3PO4; HCl; NaOH, Mg(OH)2.
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 12g một hợp chất hữu cơ X thu được 35,2g CO2 và 21,6g H2O a) xác định CTPT của X biết Mx= 30g b) viết CTCT của X và cho biết X có thể có CTHH nào? viết PTHH minh hoạ
X + O2 -- (t^o) -- > CO2 và H2O
X gồm có C và H
nCO2 = 35,2 : 44 = 0,8 (mol)
-- > nC= 0,8(mol)
nH2O = 21,6 : 18 = 1,2(mol)
--> nH = 1,2 . 2 = 2,4 (mol)
mC= 0,8 . 12 = 9,6(g)
mH = 2,4 . 1 = 2,4(g)
h/c X = mC + mH = 12g = m hh
--> h/c X không có nguyên tử Oxi
Gọi CTHH đơn giản của X là CxHy
ta có : nC : nH = 0,8 : 2,4 = 1 : 3
=> CTĐG giản X là CH3
ta có : (CH3)n = 30
15.n=30
=> n= 2
Vậy CTHH của X là C2H6
CTCT của X là: CH3 - CH3
Đúng 5
Bình luận (0)
Cho 18,8g oxit của kl(I) tác dụng vs H2O tạo ra 22,4g một hợp chất Bazơ tan
A, xác định CTHH của oxit
B, chứng tỏ rằng trong dung dịch có chất Bazơ tan
n K2O = = 0,2 mol
a) Khi cho K2O xảy ra phản ứng, tạo thành phản ứng dung dịch có chất tan là NaOH.
K2O + H2O → 2KOH
0,2 mol → 0,4 (mol)
Cm NaOH = 0,4/0,5 = 0,8M.
b) Phản ứng trung hòa dung dịch:
H2SO4 + 2KOH → K2SO4 + 2H2O
0,4 mol → 0,2 mol 0,4 (mol)
m H2SO4 = 0,25×98 = 24,5 g
M H2SO4 = 2+32+64 = 98g
Vdd = 85,96 ml
Đúng 0
Bình luận (0)
Đốt cháy 0,88g hợp chất Y thu được 1,76g CO2; 0,72g H2O. Biết Y nặng hơn không khí xấp xĩ là 3,04 lần.( Mkhông khí=29). Tìm CTHH của Y
\(n_{CO_2}=\dfrac{1.76}{44}=0.04\left(mol\right)\Rightarrow n_C=0.04\left(mol\right)\)
\(n_{H_2O}=\dfrac{0.72}{18}=0.04\left(mol\right)\Rightarrow n_H=0.04\cdot2=0.08\left(mol\right)\)
\(m_O=0.88-0.04\cdot12-0.08=0.32\left(g\right)\)
\(n_O=\dfrac{0.32}{16}=0.02\left(mol\right)\)
\(TC:\)
\(n_C:n_H:n_O=0.04:0.08:0.02=2:4:1\)
\(CT:\left(C_2H_4O\right)_n\)
\(M_Y=3.04\cdot29=88\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow44n=88\)
\(\Leftrightarrow n=2\)
\(CT:C_4H_8O_2\)
Đúng 3
Bình luận (0)
cho CTHH: CxHy +\(\left(x+\dfrac{y}{4}\right)\) O2 --------> xCO2 + \(\dfrac{y}{2}\) H2O
Biết tổng số mol CO2 và H2O là 5 vầ tích số mol của CxHy và O2 là 0,35
Tìm CxHy
Ta có :
\(x + \dfrac{y}{2} = 5\\ \Rightarrow y = (5-x).2 = 10-2x\\ 1(x + \dfrac{y}{4}) = 0,35\\ \Leftrightarrow x + \dfrac{10-2x}{4} = 0,35\\ \Leftrightarrow x = -4,3 \)
(Sai đề)
Đúng 3
Bình luận (0)
Đốt cháy 3.4 g hợp chất Y trong oxi thì thu được sản phẩm gồm 4.48 lít khí No2 và 5.4 g H2O .Xác định CTHH của y biết cthh của y trùng với CTHH đơn giản nhất
nNO2=4,48/22,4=0,2(mol)
=>nN=0,2.1=0,2
=>mN=0,2.14=2,8(g)
nH2O=5,4/18=0,3(mol)
=>nH=0,3.2=0,6(mol)
=>mH=0,6.1=0,6(g)
=>mN+mH=2,8+0,6=3,4=mY
Vậy trong Y có 2 ntố N,H
=>nN:nH=0,2:0,6=1:3
=>CTHH đơn giản là NH3
Đúng 0
Bình luận (2)