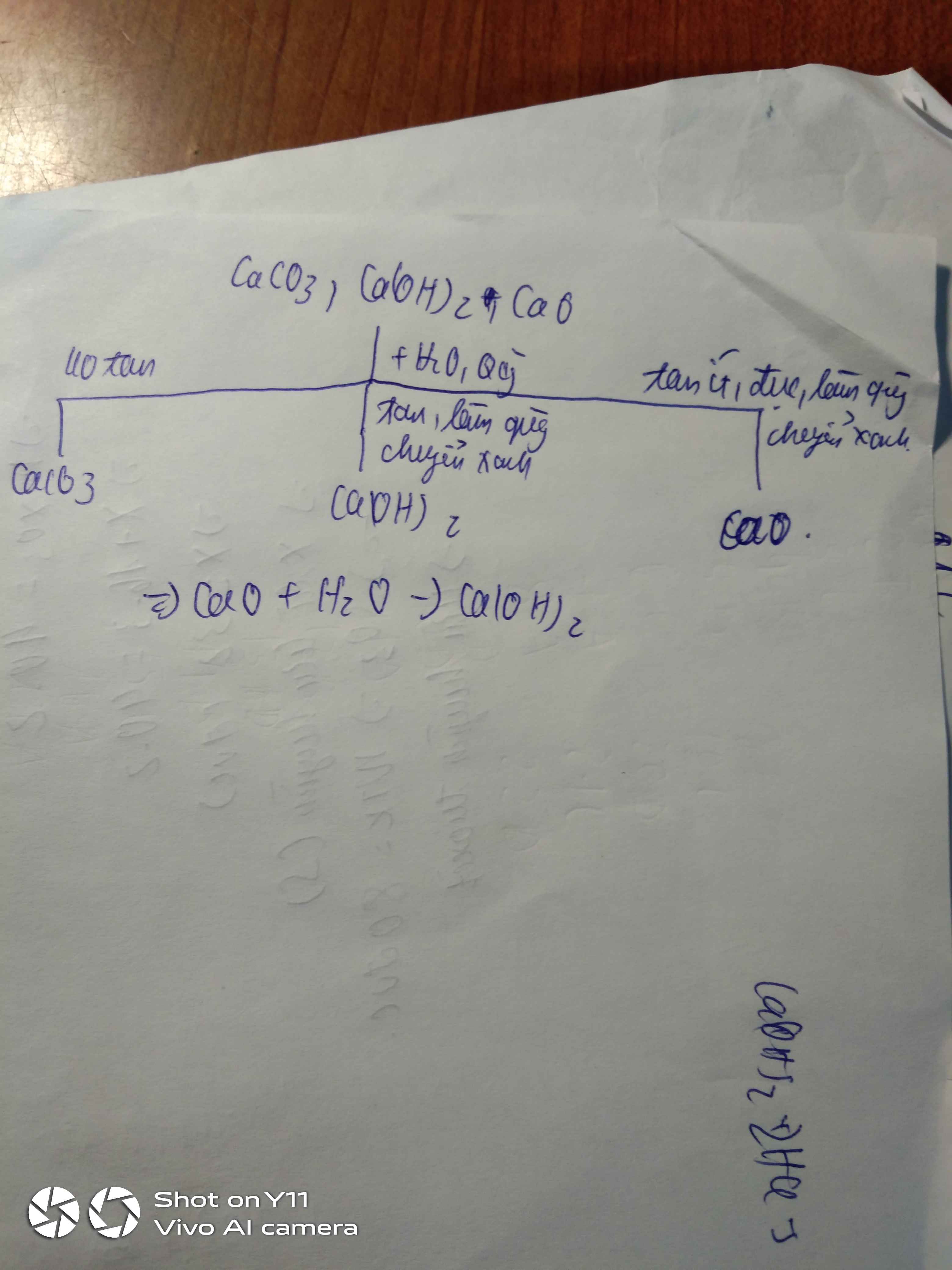
Câu 2. Bằng phương pháp hóa học, hãy nhận biết các hóa chất mắt nhãn sau: Cao và CaCO3
LB
Những câu hỏi liên quan
Câu 2: Bằng phương pháp hóa học, hãy nhận biết các hóa chất mất nhãn sau: CaO và CaCO3.Câu 3: Dẫn 2,24 lít khí CO2 (ở điều kiện tiêu chuẩn) vào 100ml dung dịch KOH.a. Viết phương trình hóa học xảy ra.b. Tính nồng độ mol dung dịch KOH.c. Tính khối lượng muối tạo thành.Câu 4: Lấy 6,4gam oxit của một kim loại hóa trị (III) cần dùng vừa đủ 240 ml dung dịch HCl 1M để hòa tan.a. Viết phương trình hóa học xảy ra.b. Xác định công thức hóa học của oxit.Câu 5: Có những chất sau: a. H2O, b...
Đọc tiếp
Câu 2: Bằng phương pháp hóa học, hãy nhận biết các hóa chất mất nhãn sau: CaO và CaCO3.
Câu 3: Dẫn 2,24 lít khí CO2 (ở điều kiện tiêu chuẩn) vào 100ml dung dịch KOH.
a. Viết phương trình hóa học xảy ra.
b. Tính nồng độ mol dung dịch KOH.
c. Tính khối lượng muối tạo thành.
Câu 4: Lấy 6,4gam oxit của một kim loại hóa trị (III) cần dùng vừa đủ 240 ml dung dịch HCl 1M để hòa tan.
a. Viết phương trình hóa học xảy ra.
b. Xác định công thức hóa học của oxit.
Câu 5: Có những chất sau:
a. H2O, b. KOH, c. K2O, d. CO2.
Hãy cho biết những cặp chất có thể tác dụng với nhau.
2.
- Trích mẫu thử và đánh số thứ tự:
- Cho nước vào từng mẫu thử
+ Mẫu thử không tan trong nước CMddKOH=0,20,1=2MCMddKOH=0,20,1=2M
c, mK2CO3=0,1.138=13,8(g)
4.
Gọi CTHH của oxit là X2O3
X2O3 + 6HCl -> 2XCl3 + 3H2O
nHCl=0,24.1=0,24(mol)
Theo PTHH ta có:
6,40,04=1606,40,04=160
=>MX=5.H2O + K2O -----> 2KOH
H2O + CO2 -----> H2CO3 (axit yếu nên vừa tạo ra bị phân hủy ngay thành CO2 và H2O)
2KOH + CO2 ------> K2CO3 + H2O ( nKOH/ nCO2 >=2)
KOH + CO2 ------> KHCO3 (nKOH/ nCO2 <= 1) </span>
K2O + CO2 ------> K2CO3
Đúng 1
Bình luận (2)
2.
- Trích mẫu thử:
- Cho nước vào các mẫu thử:
+ Nếu có phản ứng là CaO
CaO + H2O ---> Ca(OH)2
+ Không có phản ứng là CaCO3
3. Ta có: \(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
a. PTHH: CO2 + 2KOH ---> K2CO3 + H2O
b. Theo PT: \(n_{KOH}=2.n_{CO_2}=2.0,1=0,2\left(mol\right)\)
Đổi 100ml = 0,1 lít
=> \(C_{M_{KOH}}=\dfrac{0,2}{0,1}=2M\)
c. Theo PT: \(n_{K_2CO_3}=n_{CO_2}=0,1\left(mol\right)\)
=> \(m_{K_2CO_3}=0,1.138=13,8\left(g\right)\)
4. Gọi CTHH của oxit kim loại là: R2O3
a. PTHH: R2O3 + 6HCl ---> 2RCl3 + 3H2O
Đổi 240ml = 0,24 lít
Ta có: \(C_{M_{HCl}}=\dfrac{n_{HCl}}{0,24}=1M\)
=> nHCl = 0,24(mol)
Theo PT: \(n_{R_2O_3}=\dfrac{1}{6}.n_{HCl}=\dfrac{1}{6}.0,24=0,04\left(mol\right)\)
=> \(M_{R_2O_3}=\dfrac{6,4}{0,04}=160\left(g\right)\)
Ta có: \(M_{R_2O_3}=NTK_R.2+16.3=160\left(g\right)\)
=> NTKR = 56(g)
=> CTHH của oxit kim loại là Fe2O3
5. Các chất tác dụng được với nhau là:
a và c; b và d; c và d; a và d
Đúng 2
Bình luận (0)
Câu 5: Nhận biết 3 chất rắn sau bằng phương pháp hóa học: CaO, MgO, P2O5Câu 6: Nhận biết 3 chất rắn sau bằng phương pháp hóa học: CaCO3, CaO, Ca(OH)2Câu 7: Nhận biết 3 chất lỏng sau bằng phương pháp hóa học: H2SO4, NaOH, H2OCâu 8: Nhận biết các dung dịch sau bằng phương pháp hóa họca) Na2SO4, HCl, NaNO3 b) NaOH, Ba(OH)2, NaClc) Na2CO3, AgNO3, NaCl d) HCl, H2SO4, HNO3Câu 9: Nhận biế...
Đọc tiếp
Câu 5: Nhận biết 3 chất rắn sau bằng phương pháp hóa học: CaO, MgO, P2O5
Câu 6: Nhận biết 3 chất rắn sau bằng phương pháp hóa học: CaCO3, CaO, Ca(OH)2
Câu 7: Nhận biết 3 chất lỏng sau bằng phương pháp hóa học: H2SO4, NaOH, H2O
Câu 8: Nhận biết các dung dịch sau bằng phương pháp hóa học
a) Na2SO4, HCl, NaNO3 b) NaOH, Ba(OH)2, NaCl
c) Na2CO3, AgNO3, NaCl d) HCl, H2SO4, HNO3
Câu 9: Nhận biết 4 dung dịch sau đây bằng phương pháp hóa học: NaCl, Ba(OH)2, NaOH, Na2SO4
Câu 10: Nhận biết 4 dung dịch sau đây bằng phương pháp hóa học: HCl, H2SO4, BaCl2, Na2CO3
Câu 11: Nhận biết 4 dung dịch sau đây bằng phương pháp hóa học: HCl, Na2SO4, KCl, Ba(OH)2
Câu 5:
- Thử với lượng nhỏ mỗi chất.
- Cho nước vào các chất rắn, quan sát sau đó cho thêm quỳ tím:
+ Không tan -> MgO
+ Tan, tạo thành dung dịch làm quỳ tím hóa đỏ -> P2O5
P2O5 + 3 H2O -> 2 H3PO4
+ Tan, tạo thành dung dịch làm quỳ tím hóa xanh -> CaO
CaO + H2O -> Ca(OH)2
Đúng 1
Bình luận (0)
Câu 9:
- Đầu tiên dùng quỳ tím cho vào các dung dịch:
+ Qùy tím hóa xanh -> dd NaOH , dd Ba(OH)2 (Nhóm I)
+ Qùy tím không đổi màu -> dd Na2SO4, dd NaCl (nhóm II)
- Sau đó, ta tiếp tục nhỏ vài giọt dung dịch Na2SO4 vào 2 dung dịch nhóm I, quan sát:
+ Có kết tủa trắng BaSO4 -> Nhận biết dung dịch Ba(OH)2
+ Không có kết tủa trắng -> dd NaOH
- Nhỏ vài giọt dung dịch Ba(OH)2 vào nhóm dung dịch II, quan sát:
+ Có kết tủa trắng BaSO4 -> Nhận biết dd Na2SO4
+ Không có kết tủa trắng -> Nhận biết dung dịch NaCl.
PTHH: Ba(OH)2 + Na2SO4 -> BaSO4(kt trắng) + 2 NaOH
Đúng 1
Bình luận (0)
Câu 7: Nhận biết 3 chất lỏng sau bằng phương pháp hóa học: H2SO4, NaOH, H2O
---
- Dùng quỳ tím cho vào các chất lỏng, quan sát:
+ Qùy tím hóa đỏ -> dd H2SO4
+ Qùy tím hóa xanh -> dd NaOH
+ Qùy tím không đổi màu -> H2O
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Có ba lọ không nhãn, mỗi lọ đựng một trong ba chất rắn màu trắng sau: CaCO3, Ca(OH)2, CaO. Hãy nhận biết chất đựng trong mỗi lọ bằng phương pháp hóa học. Viết phương trình hóa học.
Bài 5: Bằng phương pháp hóa học hãy nhận biết các chất rắn sau: a) CaO, MgO b) CaO; CaCO3 c) Na2O; P205 Bài 6: Bằng phương pháp hóa học hãy nhận biết các chất khí sau : CO2, O2
Bài 5 :
a, Cho nước vào từng chất rắn vào quậy đều.
Tan: CaO
Không tan : MgO
b, Sục khí CO2 vào từng chất rắn trên( pha với nước )
Tạo kết tủa trắng : CaO
Chất rắn tan dần : CaCO3
c, Pha với nước vào cho giấy quỳ tím vào từng lọ :
Màu xanh : Na2O
Màu đỏ : P2O5
Bài 6 :
Sục vào dd nước vôi trong .
Tạo kết tủa trắng : CO2
Không hiện tượng : O2
Đúng 1
Bình luận (0)
Bài 2:
Bằng phương pháp hóa học hãy nhận biết các lọ hóa chất bị mất nhãn gồm: CaCO3, NaCl; SO3; MgO và Na2O đều là chất bột màu trắng ?
- Trích một ít các chất làm mẫu thử, đánh số thứ tự lần lượt
- Hòa tan các chất vào nước dư, cho giấy quỳ tím tác dụng với dd thu được:
+ Chất rắn không tan: CaCO3, MgO (I)
+ dd tạo thành đổi màu QT thành màu đỏ: SO3
SO3 + H2O --> H2SO4
+ dd tạo thành đổi màu QT thành màu xanh: Na2O
Na2O + H2O --> 2NaOH
+ dd tạo thành không đổi màu QT: NaCl
- Cho các chất rắn ở (I) tác dụng với dd HCl dư
+ Chất rắn tan dần, sủi bọt khí: CaCO3
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2\uparrow+H_2O\)
+ Chất rắn tan dần, không hiện tượng khác: MgO
MgO + 2HCl --> MgCl2 + H2O
Đúng 4
Bình luận (0)
Câu 1 1.Bằng phương pháp hóa học hãy nhận biết các lọ hóa chất bị mất nhãn gồm: CaCO3, NaCl; SO3; MgO và Na2O đều là chất bột màu trắng ? 2.Cho các axit sau: H3PO4, H2SO4, H2SO3, HNO3.a. Hãy viết công thức và gọi tên các oxit axit tương ứng với các axit trên?b. Hãy lập công thức và gọi tên muối tạo bởi các gốc axit trên với kim loại Na?
Đọc tiếp
Câu 1
1.
Bằng phương pháp hóa học hãy nhận biết các lọ hóa chất bị mất nhãn gồm: CaCO3, NaCl; SO3; MgO và Na2O đều là chất bột màu trắng ?
2.
Cho các axit sau: H3PO4, H2SO4, H2SO3, HNO3.
a. Hãy viết công thức và gọi tên các oxit axit tương ứng với các axit trên?
b. Hãy lập công thức và gọi tên muối tạo bởi các gốc axit trên với kim loại Na?
2 bài này mình giúp bn rồi nhé, bn kiểm tra lại ha :D
Đúng 0
Bình luận (1)
bằng phương pháp hóa học hãy nhận biết 3 chất rắn màu trắng trong 3 lọ mất nhãn gồm các lọ sau : NaCl, Na2SO4 và CaCO3
- Trích một ít các chất làm mẫu thử:
- Hòa tan các chất vào nước dư:
+ Chất rắn tan: NaCl, Na2SO4 (1)
+ Chất rắn không tan: CaCO3
- Cho các chất ở (1) tác dụng với dd BaCl2
+ Không hiện tượng: NaCl
+ Kết tủa trắng: Na2SO4
\(Na_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2NaCl\)
Đúng 4
Bình luận (0)
có 5 lọ mất nhãn mỗi lọ đựng 1 chất màu trắng CaSO4, CaCO3, CaCl2, Ca(NO3)2 ,CaO. hãy nhận biết từng chất bằng phương pháp hóa học
Trích mẫu thử hòa tan mỗi mẫu thử vào nước, mẫu thử tỏa ra nhiệt là CaO. Mẫu thử không tan trong nước là CaCO3, các mẫu còn lại tan trong nước tạo dung dịch (vì CaSO4 ít tan nên ta có thể chọn là nó tan hoặc không tan, ở đây là tan) Hòa tan dung dịch gồm CaSO4 CaCl2 Ca(NO3)2 vào BaCl2 thấy kết tủa trắng , đó là phản ứng giữa BaCl2 và CaSO4 tạo kết tủa BaSO4 , 2 dung dịch còn lại không có hiện tượng gì. Tiếp tục hòa tan vào bạc nitrat(AgNO3) thấy xuất hiện kết tủa trắng là của AgCl từ phản ứng giữa CaCl2 và AgNO3. Chất còn lại chính là Ca(NO3)2
Đúng 1
Bình luận (0)
- Trích mẫu thử, đánh số thứ tự
- Hòa tan 5 mẫu thử trên vào nước
+ Mẫu thử nào tan, tỏa nhiệt là CaO
+ Mẫu thử nào không tan là CaCO3
+ Mẫu thử nào tan ít là CaSO4
+ Còn lại 2 mẫu thử { CaCl2; Ca(NO3)2} bị hòa tan
- Cho 2 dung dịch thu được tác dụng với dung dịch AgNO3
+ Dung dịch nào xuất hiện kết tủa --- CaCl2
+ Dung dịch nào không có hiện tượng --------Ca(NO3)3
Các PTPỨ: CaO + H2O ---- Ca(OH)2
2AgNO3 + CaCl2 -----2AgCl + Ca(NO3)2
- Kết luận : Vậy ta đã nhận biết được 5 chất rắn màu trắng
Đúng 1
Bình luận (0)
Dạng 2: Bằng phương pháp hóa học nhận biết chất khí.VD1: Bằng phương pháp hóa học hãy nhận biết các chất khí không màu đựng trong các lọ riêng biệt sau không ghi nhãn sau: oxi, hiđro,cacbonic .(viết phương trình phản ứng nếu có).VD2: Bằng phương pháp hóa học hãy nhận biết các chất khí không màu đựng trong các lọ riêng biệt sau không ghi nhãn sau: oxi, hiđro,nitơ. (viết phương trình phản ứng nếu có).VD3: Bằng phương pháp hóa học hãy nhận biết các chất khí không màu đựng trong các lọ riêng biệt sa...
Đọc tiếp
Dạng 2: Bằng phương pháp hóa học nhận biết chất khí.VD1: Bằng phương pháp hóa học hãy nhận biết các chất khí không màu đựng trong các lọ riêng biệt sau không ghi nhãn sau: oxi, hiđro,cacbonic .(viết phương trình phản ứng nếu có).VD2: Bằng phương pháp hóa học hãy nhận biết các chất khí không màu đựng trong các lọ riêng biệt sau không ghi nhãn sau: oxi, hiđro,nitơ. (viết phương trình phản ứng nếu có).VD3: Bằng phương pháp hóa học hãy nhận biết các chất khí không màu đựng trong các lọ riêng biệt sau không ghi nhãn sau: oxi, hiđro,không khí. (viết phương trình phản ứng nếu có).Dạng 3: Tính theo phương trình hóa học.VD1:Khử 48 gam sắt (III) oxit bằng khí hiđro. Hãy tính(a) số gam sắt kim loại thu được? (b) thể tích khí hiđro (đktc) cần dùng?(c) thể tích khí oxi (đktc) cần dùng khi tác dụng với hiđro để tạo ra lượng nước gấp đôi lượng nước trong phản ứng trên.VD2:Đốt cháy hoàn toàn 8,1 gam nhôm (Al) trong bình chứa khí O2.(a) Viết phương trình hóa học của phản ứng xảy ra.(b) Tính thể tích khí O2 (ở đktc) đã tham gia phản ứng.(c) Tính khối lượng KClO3 cần dùng để khi phân hủy thì thu được một thể tích khí O2 (ở đktc) bằng với thể tích khí O2 đã tham gia phản ứng ở trên.VD3: Hòa tan 8,4 gam Fe bằng một lượng vừa đủ dung dịch HCl⦁ Viết phương trình hóa học xãy ra . ⦁ tính thể tích khí hiđro (đktc) thu được.⦁ Tính thể tích không khí đề đốt cháy hết lượng khí hiđro ở trên? Biết thể tích khí oxi chiếm 20% thể tích không khí.