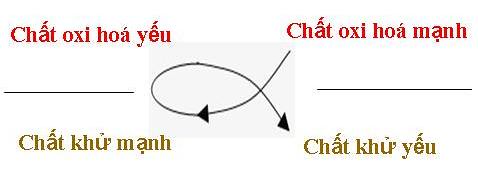
Tại sao FeCl3 lại PƯ với Cu để tạo ra 2 muối
NG
Những câu hỏi liên quan
cho fe pư với dung dịch hcl thấy thoát ra 2.24 lít khí h2
a, viết pt pư sảy ra
b, tính khối lượng fe đã pư
c,tính khối lượng muối đã tạo thành sao pư
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ pthh:Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1 0,1
=> \(m_{Fe}=0,1.56=5,6\left(g\right)\\
m_{FeCl_2}=0,1.127=12,7\left(G\right)\)
Đúng 2
Bình luận (0)
nH2 = 2,24/22,4= 0,1 mol
PTHH : Fe + HCl => FeCl2 + H2
theo pt => nFe = nH2 = 0,1 mol
mFe = 0,1 x56 = 5,6 g
theo pt => nH2 = nFeCl2 = 0,1 mol
mFeCl2 = 0,1 x 127 = 12,7 g
Đúng 0
Bình luận (0)
`a)` PTHH : $Fe + 2HCl \to FeCl_2 + H_2 \\ b)n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol) \\$ Theo pt : $n_{Fe} = n_{H_2} = 0,1(mol) \\ \rightarrow m_{Fe} = 0,1.56 = 5,6(gam) \\ c) n_{FeCl_2} = n_{H_2} = 0,1(mol) \\ \rightarrow m_{FeCl_2} = 0,1.127 = 12,7(gam)$
Đúng 0
Bình luận (0)
Tại sao FeCl3 tác dụng được với Cu, trong khi FeCl2 lại không?
Hỗn hợp X gồm Ag, Fe, Cu. Ngâm X trong dd chỉ chứa một chất tan Y, khuấy kỹ để pư xảy ra hoàn toàn, thấy còn lại một kim loại có khối lượng không đổi so với ban đầu. Biết Y tạo kết tủa với dd BaCl2. Chất Y là A. AgNO3. B. Fe2(SO4)3. C. HCl. D. H2SO4.
Đọc tiếp
Hỗn hợp X gồm Ag, Fe, Cu. Ngâm X trong dd chỉ chứa một chất tan Y, khuấy kỹ để pư xảy ra hoàn toàn, thấy còn lại một kim loại có khối lượng không đổi so với ban đầu. Biết Y tạo kết tủa với dd BaCl2. Chất Y là
A. AgNO3.
B. Fe2(SO4)3.
C. HCl.
D. H2SO4.
Đáp án B
Nếu Y là AgNO3 thì thu được kim loại Ag sẽ có khối lượng lớn hơn khối lượng ban đầu
Nếu là Fe2( SO4)3 thì Fe, Cu tan, còn Ag không tan, có khối lượng không đổi
Nếu là HCl, H2SO4 thì cả Cu và Ag đều không tan nên sẽ thu được 2 kim loại
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Ag, Fe, Cu. Ngâm X trong dd chỉ chứa một chất tan Y, khuấy kỹ để pư xảy ra hoàn toàn, thấy còn lại một kim loại có khối lượng không đổi so với ban đầu. Biết Y tạo kết tủa với dd BaCl2. Chất Y là: A. AgNO3 B. Fe2(SO4)3 C. HCl D. H2SO4
Đọc tiếp
Hỗn hợp X gồm Ag, Fe, Cu. Ngâm X trong dd chỉ chứa một chất tan Y, khuấy kỹ để pư xảy ra hoàn toàn, thấy còn lại một kim loại có khối lượng không đổi so với ban đầu. Biết Y tạo kết tủa với dd BaCl2. Chất Y là:
A. AgNO3
B. Fe2(SO4)3
C. HCl
D. H2SO4
Đáp án B
Nếu Y là AgNO3 thì thu được kim loại Ag sẽ có khối lượng lớn hơn khối lượng ban đầu
Nếu là Fe2(SO4)3 thì Fe, Cu tan, còn Ag không tan, có khối lượng không đổi
Nếu là HCl, H2SO4 thì cả Cu và Ag đều không tan nên sẽ thu được 2 kim loại
Đúng 0
Bình luận (0)
Tại sao khi cho Mg và Cu vào Fe+3 đều tạo ra Fe+2 nhưng người ta lại dùng Cu?Mọi người giải đáp cho em với! (Em mới lớp 10 nhưng cô đã ôn cái này rồi)
Nếu dùng Mg thì Mg sẽ đẩy cả Fe2+ ra nên không được
Đúng 1
Bình luận (0)
Tại sao có trường hợp NaOH tác dụng với khí SO2 lại tạo ra 2 muối là Na2SO3 và NaHSO3
Ta có nếu SO2 phản ứng hết thì có PT:
PTHH: SO2 + 2NaOH -> Na2SO3 + H2O
Nhưng nếu SO2 dư sẽ có phản ứng sau:
SO2 + Na2SO3 + H2O -> 2NaHSO3
Giải thích cho cơ sở này như sau:
Khi lên cấp 3, khi học về ion ta sẽ thấy:
Muối Na2SO3 sẽ được cấu tạo từ ion Na+ và ion SO3-
Lại có: Bazơ NaOH là 1 bazơ mạnh => ion Na+ có tính của bazơ mạnh
Axit H2SO3 là 1 axit rất yếu => ion SO3- có tính của axit yếu
=> Muối Na2SO3 có tính bazơ
Hỗn hợp SO2 + H2O chính là H2SO3 bị phân hủy thành nên hỗn hợp SO2 + H2O mang tính axit
axit luôn có thể tác dụng với bazơ nên có xảy ra phản ứng
SO2 + H2O + Na2SO3 -> 2NaHSO3
Đúng 0
Bình luận (0)
Bazo nào sau đây khó bị nhiệt phân tạo axit tương ứng
Cu(oh)2. Al(oh)3. Fe(oh)3. Naoh
2/ vì sao khi cho ba vào dd na2so4 lại tạo ra khí không màu
3/ vì sao cho na vào dd fecl3 lại tạo khí không màu
Viết các pthh để tạo ra: a, oxit axit. b, oxit bazơ. c,bazơ. d,muối Yêu cầu: mỗi trường hợp lấy 2 ví dụ,một ví dụ là pư hóa hợp , một ví dụ ko phải là pư hóa hợp
a)\(4P+5O_2\underrightarrow{t^o}2P_2O_5\) phản ứng hóa hợp
\(CaCO_3\underrightarrow{t^o}CaO+CO_2\) phân ứng phân hủy
b)\(2Na+O_2\underrightarrow{t^o}2NaO\) phản ứng hóa hợp
\(CaCO_3\underrightarrow{t^o}CaO+CO_2\) phản ứng phân hủy
c)\(Na_2O+H_2O\rightarrow2NaOH\) phản ứng hóa hợp
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
d)\(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\) phản ứng hóa hợp
\(AgNO_3+NaCl\rightarrow AgCl\downarrow+NaNO_3\) phản ứng thế
Đúng 3
Bình luận (1)
cho 100ml dd Ba(OH)2 x(M).tính x trong mỗi trường hợp sau:-TH1:dd A PƯ vừa hết với 200ml dd HCl 3.6%-TH2:dd A PƯ vừa hết với 200g dd H2SO4 4.9%-TH3:dd A PƯ vừa hết với4.48 lít CO2(ĐKTC) tạo ra muối trung hòa -TH4:dd A PƯ vừa hết với 200 dd MgCl2 9.5%. Lọc tách kết tủa sauPƯ đem muối đến m không đổi thu được Z(g)chất rắn .tính m
Đọc tiếp
cho 100ml dd Ba(OH)2 x(M).tính x trong mỗi trường hợp sau:
-TH1:dd A PƯ vừa hết với 200ml dd HCl 3.6%
-TH2:dd A PƯ vừa hết với 200g dd H2SO4 4.9%
-TH3:dd A PƯ vừa hết với4.48 lít CO2(ĐKTC) tạo ra muối trung hòa
-TH4:dd A PƯ vừa hết với 200 dd MgCl2 9.5%. Lọc tách kết tủa sauPƯ đem muối đến m không đổi thu được Z(g)chất rắn .tính m