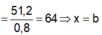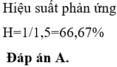cho 80g SO2 tác dụng với 16g O2 tạo ra 48g SO3. TÍnh hiệu suất phản ứng.
Tuyển Cộng tác viên Hoc24 nhiệm kì 26 tại đây: https://forms.gle/dK3zGK3LHFrgvTkJ6
HY
Những câu hỏi liên quan
Cho 4,48 lít khí SO2 tác dụng với 2,24 lít khí O2. Thêm xúc tác và nung nóng cho phản ứng xảy ra. Sau khi phản ứng kết thúc, ta thu được 5,6 lít hỗn hợp khí gồm SO2, O2, SO3. Tính thể tích mỗi khí có trong hỗn hợp sau phản ứng và tính hiệu suất của phản ứng. Biết các khí đo ở đktc
Gọi hiệu suất phản ứng là a
$2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3$
Ta thấy :
V SO2 / 2 = V O2 nên hiệu suất tính theo số mol của SO2 hoặc O2
V SO2 phản ứng = 4,48a(lít)
V O2 phản ứng = 2,24a(lít)
V SO3 = V SO2 pư = 4,48a(lít)
Sau phản ứng, khí gồm :
SO2 : 4,48 - 4,48a(lít)
O2 : 2,24 - 2,24a(lít)
SO3 : 4,48a(lít)
Suy ra :
4,48 - 4,48a + 2,24 - 2,24a + 4,48a = 5,6
=> a = 0,5 = 50%
Hỗn hợp khí gồm :
SO2 : 4,48 -4,48.0,5 = 2,24 lít
O2 : 2,24 - 2,24.0,5 = 1,12 lít
SO3 : 4,48.0,5 = 2,24 lít
Đúng 1
Bình luận (3)
Câu V. 1. Cho 4,48l khí SO2 tác dụng với 2,24l khí O2 theo phương trình hoá học SO2 + O2 SO3 Sau khi phản ứng kết thúc ta thu được 5,6ℓ hỗn hợp khí gồm SO2, O2, SO3.a. Tính thể tích mỗi khí có trong hỗn hợp sau phản ứngb. Tính hiệu suất của phản ứng2. Cho 7,2g Mg tác dụng với 2,24l khí O2 sau phản ứng kết thúc thu được hỗn hợp chất rắn A. Hoà tan A bằng 100g dung dịch HCl 29,2% thì thu được dung dịch B và khí C.a. Viết các phương trình hoá học xảy rab. Tính thể tích khí Cc. Tính C% của các ch...
Đọc tiếp
Câu V.
1. Cho 4,48l khí SO2 tác dụng với 2,24l khí O2 theo phương trình hoá học
SO2 + O2![]() SO3
SO3
Sau khi phản ứng kết thúc ta thu được 5,6ℓ hỗn hợp khí gồm SO2, O2, SO3.
a. Tính thể tích mỗi khí có trong hỗn hợp sau phản ứng
b. Tính hiệu suất của phản ứng
2. Cho 7,2g Mg tác dụng với 2,24l khí O2 sau phản ứng kết thúc thu được hỗn hợp chất rắn A. Hoà tan A bằng 100g dung dịch HCl 29,2% thì thu được dung dịch B và khí C.
a. Viết các phương trình hoá học xảy ra
b. Tính thể tích khí C
c. Tính C% của các chất có trong dung dịch B.
Các khí đều được đo ở điều kiện tiêu chuẩn
Cho 4,48l khí SO2 tác dụng với 2,24l khí O2 theo phương trình hoá học
SO2 + O2 --V2O5->,tO SO3
Sau khi phản ứng kết thúc ta thu được 5,6ℓ hỗn hợp khí gồm SO2, O2, SO3.
a. Tính thể tích mỗi khí có trong hỗn hợp sau phản ứng
b. Tính hiệu suất của phản ứng
\(n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{hh}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Gọi \(n_{SO_3}=a\left(mol\right)\)
PTHH: 2SO2 + O2 --to--> 2SO3
a <----- 0,5a <--- a
\(\rightarrow0,2-a+0,1-a+a=0,25\Leftrightarrow a=0,05\left(mol\right)\)
\(\rightarrow\left\{{}\begin{matrix}V_{O_2}=\left(0,1-0,05\right).22,4=1,12\left(l\right)\\V_{SO_2}=\left(0,2-0,05\right).22,4=3,36\left(l\right)\\V_{SO_3}=0,05.22,4=1,12\left(l\right)\end{matrix}\right.\)
\(H=\dfrac{0,05}{0,2}=25\%\)
Đúng 1
Bình luận (0)
Cho 6,72 lít (đktc) hỗn hợp khí gồm O2 và SO2 có tỉ lệ thể tích 1 : 2.
Đun nóng hỗn hợp trên với xúc tác thích hợp tạo ra SO3.Sau khi dừng phản ứng thu được 4,928 lít hỗn hợp khí.
a.Tính thể tích SO3(đktc).
b.Tính hiệu suất phản ứng.
Trong một bình kín chứa 2 mol O2, 3 mol SO2 và một ít bột xúc tác V2O5. Nung nóng bình một thời gian thu được hỗn hợp khí B.SO2 + O2 -----V2O5,to-----SO31. Nếu hiệu suất phản ứng oxi hóa SO2 thành SO3 là 75% thì có bao nhiêu mol SO3 tạo thành?2. Nếu tổng số mol các khí trong B là 4,25. Hãy tính hiệu suất phản ứng oxi hóa SO2 thành SO3
Đọc tiếp
Trong một bình kín chứa 2 mol O2, 3 mol SO2 và một ít bột xúc tác V2O5. Nung nóng bình một thời gian thu được hỗn hợp khí B.
SO2 + O2 -----V2O5,to----->SO3
1. Nếu hiệu suất phản ứng oxi hóa SO2 thành SO3 là 75% thì có bao nhiêu mol SO3 tạo thành?
2. Nếu tổng số mol các khí trong B là 4,25. Hãy tính hiệu suất phản ứng oxi hóa SO2 thành SO3
1)
Xét tỉ lệ: \(\dfrac{3}{2}< \dfrac{2}{1}\) => Hiệu suất tính theo SO2
\(n_{SO_2\left(pư\right)}=\dfrac{3.75}{100}=2,25\left(mol\right)\)
PTHH: 2SO2 + O2 -----V2O5,to-----> 2SO3
2,25--------------------->2,25
=> nSO3 = 2,25 (mol)
2) Gọi số mol SO2 pư là a (mol)
PTHH: 2SO2 + O2 -----V2O5,to-----> 2SO3
Trc pư: 3 2 0
Pư: a-->0,5a-------------------->a
Sau pư: (3-a) (2-0,5a) a
=> (3-a) + (2-0,5a) + a = 4,25
=> a = 1,5 (mol)
=> \(H=\dfrac{1,5}{3}.100\%=50\%\)
Đúng 2
Bình luận (0)
Nung một hỗn hợp X gồm SO2 và O2 có tỉ khối so với O2 là 1,6 với xúc tác V2O5 thu được hỗn hợp Y. Biết tỉ khối của X so với Y là 0,8. Tính hiệu suất của phản ứng tổng hợp SO3 ? A. 66,7%. B. 50%. C. 75%. D. 80%
Đọc tiếp
Nung một hỗn hợp X gồm SO2 và O2 có tỉ khối so với O2 là 1,6 với xúc tác V2O5 thu được hỗn hợp Y. Biết tỉ khối của X so với Y là 0,8. Tính hiệu suất của phản ứng tổng hợp SO3 ?
A. 66,7%.
B. 50%.
C. 75%.
D. 80%
lấy 6 mol so2 trộn với 8 mol o2 trong điều kiện thích hợ, thu đc 3 mol so3. Tính hiệu suất phản ứng của so2
ta có PTHH: 2SO2 + O2 \(\rightarrow\) 2SO3
theo GT 6(mol) 8(mol) 3(mol)
theo P/Ư: nSO2=nSO3=3(mol)
Hiệu suất= 3/6*100%=50%
Đúng 0
Bình luận (0)
ptpư: 2SO2 + O2 ---> 2SO3
(mol) 1 -> 0,5
(mol) 6 -> 8
Theo pt thấy O2 hết, SO2 dư => tính theo O2
Theo pt thấy nSO4pư =2nO2=2.8=16(mol)
=> H=\(\dfrac{6}{16}\).100%=37,5%
Đúng 0
Bình luận (0)
16 gam là khối lượng SO3 thu được SO3 từ việc cho 19,2 gam khí SO2 tác dụng với 5,6 lít O2 đkc. Tính H của phản ứng tổng hợp khí SO3 này.
\(n_{SO_3}=\dfrac{16}{80}=0,2\left(mol\right)\)
\(n_{SO_2}=\dfrac{19,2}{64}=0,3\left(mol\right)\)
\(n_{O_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2SO2 + O2 --to,V2O5--> 2SO3
Xét tỉ lệ: \(\dfrac{0,3}{2}< \dfrac{0,25}{1}\) => Hiệu suất tính theo SO2
PTHH: 2SO2 + O2 --to,V2O5--> 2SO3
0,2<-------------------0,2
=> \(H=\dfrac{0,2}{0,3}.100\%=66,67\%\)
Đúng 1
Bình luận (0)
Bài 2:1, Cho 4,48 lít khí SO2 tác dụng với 2,24 l O2 theo phương trình SO2 + O2 -- SO3 sau phản ứng thu đc 5,6 lít hỗn hợp gồm SO2; O2; SO3 a, Tính thể tích mỗi khí sau phản ứngb, Tính hiệu xuất 2, Cho 7,2 g Mg td với 2,24 l O2 sau phản ứng thu đc hỗn hợp chất rắn A. Hòa tan A bằng HCl thu thu dc dd B và khí Ca, Viết PTHH. Xác định khối lượng các chất trong A
Đọc tiếp
Bài 2:
1, Cho 4,48 lít khí SO2 tác dụng với 2,24 l O2 theo phương trình SO2 + O2 --> SO3 sau phản ứng thu đc 5,6 lít hỗn hợp gồm SO2; O2; SO3
a, Tính thể tích mỗi khí sau phản ứng
b, Tính hiệu xuất
2, Cho 7,2 g Mg td với 2,24 l O2 sau phản ứng thu đc hỗn hợp chất rắn A. Hòa tan A bằng HCl thu thu dc dd B và khí C
a, Viết PTHH. Xác định khối lượng các chất trong A
1, 2SO2 +O2 ---->2SO3
2a <--- a --->2a
Ban đầu nSO2=0,2 mol ; nO2=0,1 mol
n khí sau=0,3-a=0,25 ⇒ a=0,05
Lúc sau có VSO2=2,24 l; VO2=1,12 l;VSO3=2,24 l
Có H=0,05/0,1.100=50%
2, 2Mg+O2 --->2MgO
0,2 <--- 0,1 --->0,2
hoà tan hh A có khí bay ra nên Mg dư, O2 hết
Trong A có mMgO=8 g; mMg dư=2,4 g
Đúng 1
Bình luận (0)