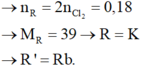Nguyên tử khối của kim loại R là 204,4 và muối clorua cua nó chứa 14,8%. Hóa trị của kim loại R là
PT
Những câu hỏi liên quan
Xác định hóa trị của kim loại, biết nguyên tử khối của nó = 204,4 và muối clorua của nó chứa 14,8% clo.
Gọi hóa trị của kim loại là a
CTHH: XCla
Theo bài ra ta có
\(\frac{35,5a}{35,5a+X}=0,148\)
=\(\frac{35,5a}{35,5a+204,4}=0,148\)
Giair ta tìm dc a=1
Vậy X hóa trị I
\(\frac{ }{ }\)
Xác định hóa trị của nguyên tố kim loại, biết nguyên tử khối là 204,4 và muối clorua của nó chứa 14,8% Clo
Gọi CTHH là RClx
Ta có: \(C\%_{Cl}=14,8\%\)
\(\Leftrightarrow\dfrac{35,5x}{35,5x+204,4}=14,8\%\)
\(\Rightarrow x=1\)
Đúng 0
Bình luận (0)
Gọi nguyên tố kim loại là R
Vậy CTHH là RClx
Ta có: \(\%R=\dfrac{35,5x}{35,5x+204,4}=14,8\%\)
\(\Rightarrow x=1\)
Vậy hóa trị của R là I
Đúng 0
Bình luận (0)
Xác định hóa trị của kim loại , biết NTK của nó = 204,4 và muối clorua của nó chứa 14,8% clo
Gọi kim loại cần tìm là R, ta có \(RCl_y\)
\(\%Cl=\dfrac{35,5y.100}{35,5y+204,4}=14,8\%\)
\(\Rightarrow y=1\)
CTHH: \(RCl\)
Vậy, hóa trị kim loại là I
Đúng 0
Bình luận (0)
Gọi CTHH là \(RCl_x\)
Ta có: \(C\%_{Cl}=14,8\%\)
\(\Leftrightarrow\dfrac{35,5x}{35,5x+204,4}=14,8\%\)
\(\Rightarrow x=1\)
Đúng 0
Bình luận (0)
Gọi kim loại cần tìm là A, ta có ACly
ta có :
%Cl = \(\dfrac{35,5y.100}{35,5y+204,4}\)=14,8%
⇒y=1
vậy hóa trị là I
Vậy, hóa trị kim loại là I
Đúng 0
Bình luận (0)
Kim loại R tạo ra 2 muối RCln và RClm biết clorua ở mức hóa trị thấp Cl chiếm 55,91% về khối lượng , muối clorua ở mức hóa trị cao Cl chiếm 65,539% về khối lượng . Xác định kim loại R
Giả sử n < m
- Với RCln: \(\%Cl=\dfrac{35,5n}{M_R+35,5n}.100\%=55,91\%\)
=> MR = 28n (g/mol)
- Với RClm: \(\%Cl=\dfrac{35,5m}{M_R+35,5m}.100\%=65,539\%\)
=> MR = 18,66m (g/mol)
TH1: n = 1 => MR = 28 => Loại
TH2: n = 2 => MR = 56 (g/mol) => R là Fe => m = 3 (thỏa mãn)
Đúng 3
Bình luận (0)
Thế gọi n là hoá trị thấp, m là hoá trị cao. (m,n:nguyên, dương)
\(\Rightarrow\left\{{}\begin{matrix}\dfrac{35,5n}{M_R+35,5n}.100\%=55,91\%\\\dfrac{35,5m}{M_R+35,5m}.100\%=65,539\%\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}\dfrac{M_R}{35,5n}=\dfrac{44,09\%}{55,91\%}=0,789\\\dfrac{M_R}{35,5m}=\dfrac{34,461\%}{65,539\%}=0,526\end{matrix}\right.\)
Xét các giá trị từ 1 đến 3 (m>n) ta nhận giá trị n=2 và m=3 => MR=56(g/mol)
=> R là Sắt (Fe=56)
Đúng 2
Bình luận (0)
Mừng năm mới 2022!
Chúc mọi người một năm vui vẻ, bình an, nhiều thành công trong công việc và cuộc sống
Đúng 0
Bình luận (5)
Hai kim loại R và R’ kế tiếp nhau trong nhóm IA (R có số hiệu nguyên tử nhỏ hơn R’). Điện phân nóng chảy một muối clorua của kim loại kiềm R, sau một thời gian thu được 2,016 lít khí (đktc) và 7,02 gam kim loại. Kim loại R’ là: A. Li B. Na C. K D. Rb
Đọc tiếp
Hai kim loại R và R’ kế tiếp nhau trong nhóm IA (R có số hiệu nguyên tử nhỏ hơn R’). Điện phân nóng chảy một muối clorua của kim loại kiềm R, sau một thời gian thu được 2,016 lít khí (đktc) và 7,02 gam kim loại. Kim loại R’ là:
A. Li
B. Na
C. K
D. Rb
Hai kim loại R và R’ kế tiếp nhau trong nhóm IA (R có số hiệu nguyên tử nhỏ hơn R’). Điện phân nóng chảy một muối clorua của kim loại kiềm R, sau một thời gian thu được 2,016 lít khí (đktc) và 7,02 gam kim loại. Kim loại R’ là: A. Li. B. Na. C. K. D. Rb.
Đọc tiếp
Hai kim loại R và R’ kế tiếp nhau trong nhóm IA (R có số hiệu nguyên tử nhỏ hơn R’). Điện phân nóng chảy một muối clorua của kim loại kiềm R, sau một thời gian thu được 2,016 lít khí (đktc) và 7,02 gam kim loại. Kim loại R’ là:
A. Li.
B. Na.
C. K.
D. Rb.
Muối clorua của một kim loại hóa trị I có 14,8% clo về khối lượng. Xác định công thức của muối?
Hòa tan hoàn toàn 3,24 gam kim loại R trong lượng dư dung dịch HCL thu được muối clorua của kim loại R gồm R liên kết với Clo và thoát ra 4,032 l khí H2 điều kiện tiêu chuẩn xác định nguyên tố R theo các trường hợp sau
A kim loại R hóa trị 3
b kim loại R hóa trị x( 1 x 3 ,x Nguyên)
Cho 55,5 gam muối clorua của một kim loại hóa trị II (muối clorua là hợp chất của kim loại với nguyên tố clo) tác dụng vừa đủ với 170 gam AgNO3. Tìm kim loại, công thức muối clorua và khối lượng các chất tạo thành sau phản ứng. mik cần gấp!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
Gọi KL cần tìm là M
\(n_{AgNO_3}=\dfrac{170}{170}=1(mol)\\ MCl_2+2AgNO_3\to M(NO_3)_2+2AgCl\downarrow\\ \Rightarrow n_{MCl_2}=\dfrac{1}{2}n_{AgNO_3}=0,5(mol)\\ \Rightarrow M_{MCl_2}=\dfrac{55,5}{0,5}=111(g/mol)\\ \Rightarrow M_M=111-35,5.2=40(g/mol)(Ca)\\ n_{Ca(NO_3)_2}=0,5(mol);n_{AgCl}=1(mol)\\ \Rightarrow m_{Ca(NO_3)_2}=0,5.164=82(g);m_{AgCl}=1.143,5=143,5(g)\)
Đúng 3
Bình luận (0)