Tính số g Na cần thiết để p/ư với 500 g nc tạo thành dd NaOH 20%
NN
Những câu hỏi liên quan
tính số gam Na cần thiết để phản ứng với 500gam H2O tạo thành dd NaOH 20%
Gọi 2x là số mol Na cần thêm=>mNa=23.2x=46x(g)
Ta có PTHH:
2Na+2H2O->2NaOH+H2
2x......................2x.........x....(mol)
Theo PTHH:\(\begin{cases} nNaOH=2x=>mNaOH=40.2x=80x(g)\\ nH2=x=>mH2=2x(g) \end{cases}\)
Sau pư,ta có:mdd=mNa+mH2O-mH2=46x+500-2x=44x+500(g)
Theo gt:C%ddsau=mNaOH:mdd.100%=20%
=>\(\dfrac{80x}{44x+500}\).100%=20%=>x=1,4 (mol)
=>mNa=46x=46.1,4=64,4g
Đúng 1
Bình luận (1)
PTHH;
Na+H2O -->NaOH + \(\dfrac{1}{2}\) H2
x mol x mol
Ta có: \(\dfrac{40x}{23x+500}.100=20\)
=> x= 2,82
mNa= 2,82 .23=3,72
Đúng 0
Bình luận (0)
Tính số gam Na cần thiết để phản ứng với 500 gam H2O tạo thành dung dịch NaOH có nồng độ 20%
PTHH: 2Na + 2H2O \(\rightarrow\) 2NaOH + H2
*Gọi nNa = a(mol)
Theo PT => nNaOH = nNa = a(mol)
=> mNaOH = n .M = 40a(g)
*C%NaOH = \(\dfrac{m_{ct}}{m_{dd}}.100\%=20\%\)
=> \(\dfrac{40a}{40a+500}=0,2\)
Giải ra được a =3,125(mol)
=> mNa = n .M = 3,125 . 23 =71,875(g)
Đúng 1
Bình luận (2)
Gọi a là số gam Na pứ
Pt: 2Na + 2H2O --> 2NaOH + H2
Ta có: \(20=\dfrac{a}{a+500}.100\)
\(\Rightarrow a=125\)
Vậy .................
Đúng 0
Bình luận (0)
hòa tan 11,5 g na vào 500 g dd naoh có nồng độ 8% thu đc dd A.a, tính nồng độ % chất tan trong dd thu đc.b,để trung hòa dd A cần dùng bn ml dd X chứa đồng thời hcl 1M và h2so4 0,5M
a) \(n_{Na}=\dfrac{11,5}{23}=0,5\left(mol\right)\)
\(n_{NaOH}=\dfrac{8\%.500}{40}=1\left(mol\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
0,5---------------->0,5------->0,25
\(\Sigma n_{NaOH}=0,5+1=1,5\left(mol\right)\)
\(m_{ddsaupu}=11,5+500-0,25.2=511\left(g\right)\)
=> \(C\%_{NaOH}=\dfrac{1,5.40}{511}.100=11,74\%\)
b) Gọi thể tích dung dịch X cần tìm là V
\(n_{H^+}=V.1+V.0,5.1=2V\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
Ta có : \(n_{H^+}=n_{OH^-}=1,5\left(mol\right)\)
=> 2V=1,5
=> V=0,75(lít)
Đúng 2
Bình luận (0)
Thủy phân hoàn toàn một tetra peptit X ( được tạo thành từ Gly) trong 500 ml dung dịch NaOH 1M thu được dd Y. Để phản ứng vừa đủ với các chất trong Y cần dd chứa 0,35 mol H2SO4 thu được dd Z chỉ chứa các muối trung hòA. Cô cạn cẩn thận Z thu được m g muối khan. Tính m A. 24,8g B. 95,8g C. 60,3g D. 94,6g
Đọc tiếp
Thủy phân hoàn toàn một tetra peptit X ( được tạo thành từ Gly) trong 500 ml dung dịch NaOH 1M thu được dd Y. Để phản ứng vừa đủ với các chất trong Y cần dd chứa 0,35 mol H2SO4 thu được dd Z chỉ chứa các muối trung hòA. Cô cạn cẩn thận Z thu được m g muối khan. Tính m
A. 24,8g
B. 95,8g
C. 60,3g
D. 94,6g
Đáp án C
nNaOH = 0,5 mol
nH2SO4 = 0,35 mol
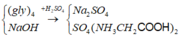
Bảo toàn nguyên tố Na : nNa2SO4 = 0,25 mol
Bảo toàn nguyên tố S → nmuối hữu cơ = 0,35-0,25=0,1 mol
→m = 0,25.142 + 0,1.248=60,3 g
Đúng 0
Bình luận (0)
1 a) Cần lấy bao nhiêu gam NaOH để cho thêm vào 126(g) dd NaOH 20% để được dd mới có nồng độ 25(g)
b) Tính khối lượng nước thêm vào 500(g) dd NaCl 12% để được dd 8%
1/ a/ Gọi khối lượng NaOH cần thêm vào là x.
Khối lượng của NaOH ban đầu là: \(126.0,2=25,2\left(g\right)\)
Khối lượng của NaOH sau khi thêm là: \(x+25,2\left(g\right)\)
Khối lượng của dung dịch NaOH sau khi thêm là: \(x+126\left(g\right)\)
\(\Rightarrow\dfrac{x+25,2}{x+126}=0,25\)
\(\Leftrightarrow5x=42\)
\(\Leftrightarrow x=8,4\left(g\right)\)
b/ Gọi khối lượng nước thêm vào là a
Khối lượng dung dịch NaCl lúc sau là: \(500+a\left(g\right)\)
Khối lượng NaCl là: \(500.0,12=60\left(g\right)\)
\(\Rightarrow\dfrac{60}{500+a}=0,08\)
\(\Leftrightarrow a=250\left(g\right)\)
Đúng 0
Bình luận (0)
1) Cho 9.6 g Na và 9.3 g Na2O vào 100g nc tính nồng độ % của dd thu đc sau pứ
2) phải thêm bao nhiêu g nước vào 200g dd KOH 20% để đc dd KOH 10%
2. Ta có: mKOH 20% = \(\frac{200.20}{100}\) = 40g
mKOH 10% = mKOH 20% = 40g
=>mdd KOH 10% = \(\frac{40.100}{10}\) = 400g
=> mH2O = 400 - 200 =200g
Đúng 0
Bình luận (1)
cho các chất sau : cuo , feo , fe2o3 , ag , naoh , ba(oh)2 , k2co3 , al , al2o3 , fe(oh)2 , al(oh)3 , na , na2o , co2 , so2 , ca(oh)2
hãy cho biết chất nào td đc với
- nc tạo thành dd axit
- nc tạo thành dd bazo
dd h2so4 loãng tạo thành muối và nc , giải phóng khí hidro
dd hcl tạo thành muối , nc , 3 chất sp
viết pt
Td với nước tạo ra axit
\(CO_2+H_2O⇌H_2CO_3\\ SO_2+H_2O⇌H_2SO_3\)
Td với nước tạo ra bazo
\(2Na+2H_2O\rightarrow2NaOH+H_2\\ Na_2O+H_2O\rightarrow2NaOH\)
Td với \(H_2SO_4\) tạo ra muối và nước
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ FeO+H_2SO_4\rightarrow FeSO_4+H_2O\\ 2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4+2H_2O\\ Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\\ Fe\left(OH\right)_2+H_2SO_4\rightarrow FeSO_4+2H_2O\\ 2Al\left(OH\right)_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+6H_2O\\ Na_2O+H_2SO_4\rightarrow Na_2SO_4+H_2O\\ Ca\left(OH\right)_2+H_2SO_4\rightarrow CaSO_4+2H_2O\)
Td với \(H_2SO_4\) giải phóng khí hiđro
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ 2Na+H_2SO_4\rightarrow Na_2SO_4+H_2\)
Td với \(HCl\) tạo ra muối, nước, 3 chất sp
\(K_2CO_3+2HCl\rightarrow2KCl+H_2O+CO_2\)
Đúng 3
Bình luận (0)
cho 4,6g kim loại Na vào 500 g dd H2SO4 20%. TÍNH C% của dd
n Na=4,6/23=0.2(mol)
m H2SO4=500.20/100=100(g)
nH2SO4=100/98 =1,02(mol)
2Na + H2SO4 ---> Na2SO4 +H2
bd 0,2 1,02
pu 0,2-> 0,1 0,1 0,1
spu 0 0,902 0,1 0,1
m dd spu=4,6 +500 -(0,1.2)=504,4(g)
m H2SO4 du =0,902.98=88,396(g)
m Na2SO4=0,1.142=14,2(g)
C% H2SO4 du= 88,392.100/504,4=17,5(%)
C% Na2SO4=14,2.100/504,4=2,8(%)
Đúng 0
Bình luận (0)
tính thể tích dd hcl 2m cần dùng để p/ư với 10,2 g al2o3
Xem chi tiết
\(n_{Al_2O_3}=\dfrac{10.2}{102}=0.1\left(mol\right)\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2\)
\(0.1..........0.6\)
\(V_{ddHCl}=\dfrac{0.6}{2}=0.3\left(l\right)\)
Đúng 1
Bình luận (0)






