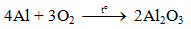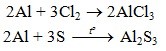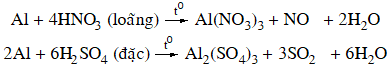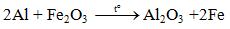Nêu tình chất hóa học của O2 ,H2,H2O. Mỗi tính chất dẫn ra 2 ví dụ minh họa
DC
Những câu hỏi liên quan
1. Nêu tính chất hóa học của oxi, hiđro. Viết phương trình hóa học minh họa.
2. Viết PTHH để điều chế H2, O2 trong phòng thí nghiệm.
3. Nêu khái niệm, cách gọi tên, phân loại oxit. Lấy ví dụ minh họa.
4. Nêu tên, khái niệm, ví dụ về các loại phản ứng hóa học đã học.
5. Nêu ứng dụng của oxi, hiđro.
Câu 1. Nêu tính chất hóa học của AXIT. Mỗi tính chất lấy 2 ví dụ minh họaCâu 2. Nêu tính chất hóa học của BAZO. Mỗi tính chất lấy 2 ví dụ minh họaCâu 3. Tính nồng độ phần trăm của 250g dung dịch có chứa 25g muối ăn.Câu 4. Tính nồng độ mol của 200ml dung dịch có 9,8g axit sunfuricCâu 5. Cho 5,6g sắt vào 100ml dung dịch HCl. Tính thể tích khí sinh ra. Tính nồng độ dung dịch HCl đã dùng.Câu 6. Hòa tan nhôm bằng 150ml dung dịch axit sunfuric 1,5M. Tính khối lượng nhôm đã dùng và nồng độ mol của muối...
Đọc tiếp
Câu 1. Nêu tính chất hóa học của AXIT. Mỗi tính chất lấy 2 ví dụ minh họa
Câu 2. Nêu tính chất hóa học của BAZO. Mỗi tính chất lấy 2 ví dụ minh họa
Câu 3. Tính nồng độ phần trăm của 250g dung dịch có chứa 25g muối ăn.
Câu 4. Tính nồng độ mol của 200ml dung dịch có 9,8g axit sunfuric
Câu 5. Cho 5,6g sắt vào 100ml dung dịch HCl. Tính thể tích khí sinh ra. Tính nồng độ dung dịch HCl đã dùng.
Câu 6. Hòa tan nhôm bằng 150ml dung dịch axit sunfuric 1,5M. Tính khối lượng nhôm đã dùng và nồng độ mol của muối tạo thành. Xem như thể tích thay đổi không đáng kể.
Câu 7. Cho 5,6g sắt tác dụng với 300ml dung dịch HCl 1,5M. Tính nồng độ chất sau phản ứng (Xem thể tích thay đổi không đáng kể)
Câu 8. Cho 16 gam hỗn hợp Mg, Fe tan hết trong 100 ml dd HCl 8M. Tính phần trăm khối lượng từng kim loại trong hỗn hợp
giải giúp em nha mọi người :))
thank mọi mười <3
Câu 1 :
+ Làm đổi màu chất chỉ thị màu : làm quỳ tím hóa đỏ
+ Tác dụng với kim loại :
vd : \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
+ Tác dụng với oxit bazo :
vd : \(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
\(BaO+H_2SO_4\rightarrow BaSO_4+H_2\)
+ Tác dụng với bazo :
vd : \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
\(KOH+HCl\rightarrow KCl+H_2O\)
Chúc bạn học tốt
Đúng 2
Bình luận (1)
Câu 2 :
+ Làm đổi màu chất chỉ thị màu : làm quỳ tím hóa xanh
+ Tác dụng với oxit axit :
vd : \(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
\(2KOH+CO_2\rightarrow K_2CO_3+H_2O\)
+ Tác dụng với axit :
vd : \(NaOH+HCl\rightarrow NaCl+H_2O\)
\(Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4+2H_2O\)
+ Bazo không tan bị nhiệt phân hủy :
vd : \(Zn\left(OH\right)_2\rightarrow\left(t_o\right)ZnO+H_2O\)
\(2Fe\left(OH\right)_3\rightarrow\left(t_o\right)Fe_2O_3+3H_2O\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
Câu 3 :
\(C_{NaCl}=\dfrac{25.100}{250}=10\)0/0
Câu 4 : \(n_{H2SO4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
200ml = 0,2l
\(C_{M_{H2SO4}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Câu 5 :
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,1 0,2 0,1
\(n_{H2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,1.22,4=2,24\left(l\right)\)
\(n_{HCl}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
200ml = 0,2l
\(C_{M_{HCl}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
Xem thêm câu trả lời
Câu 1: Nêu tính chất hóa học của O2 . Viết phương trình minh họa. Chỉ rõ vai trò của O2 trong phản ứng.Câu 2: Nêu tính chất hóa học của S . Viết phương trình minh họa. Chỉ rõ vai trò của S trong từng phản ứng.Câu 3: Nêu tính chất hóa học của H2S. Viết phương trình minh họa.Chỉ rõ vai trò của H2S trong mỗi phản ứng.Câu 4: Nêu tính chất hóa học của SO2. Viết phương trình minh họa. Trong phản ứng nào SO2 thể hiện tính khử, tính oxi hóa? Trong phản ứng nào SO2 là oxit axit?
Đọc tiếp
Câu 1: Nêu tính chất hóa học của O2 . Viết phương trình minh họa. Chỉ rõ vai trò của O2 trong phản ứng.
Câu 2: Nêu tính chất hóa học của S . Viết phương trình minh họa. Chỉ rõ vai trò của S trong từng phản ứng.
Câu 3: Nêu tính chất hóa học của H2S. Viết phương trình minh họa.Chỉ rõ vai trò của H2S trong mỗi phản ứng.
Câu 4: Nêu tính chất hóa học của SO2. Viết phương trình minh họa. Trong phản ứng nào SO2 thể hiện tính khử, tính oxi hóa? Trong phản ứng nào SO2 là oxit axit?
Mình nghĩ cái này thuộc kiến thức cơ bản, bạn nên tự học trong SGK thì hơn là đi đăng câu hỏi ở Hoc24
Đúng 0
Bình luận (0)
Câu 1: Nêu tính chất hoá học của oxi, mỗi tính chất viết một phương trình hoá học minh hoạ. Câu 2: Nêu định nghĩa phản ứng hóa hợp, phản ứng phân hủy. Cho thí dụ minh họa. Câu 3: Nêu định nghĩa oxit, cách gọi tên oxit cho thí dụ minh họa.
Xem chi tiết
Câu 1:
+ Tác dụng với kim loại: O2 oxi hóa được hầu hết các kim loại trừ Ag, Au, Pt
+ Tác dụng với Hiđro, Phản ứng có thể gây nổ mạnh nếu tỉ lệ phản ứng O2:H2 = 1:2
+ Tác dụng với một số phi kim khác:
+ Tác dụng với một số hợp chất:
Câu 2:
+ Phản ứng hóa hợp là PƯHH trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
+ Phản ứng phân hủy là PƯHH trong đó có 2 hay nhiều chất được tạo thành từ một chất ban đầu.
Đúng 1
Bình luận (0)
Câu 2:
+ Phản ứng hóa hợp là PƯHH trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
+ Phản ứng phân hủy là PƯHH trong đó có 2 hay nhiều chất được tạo thành từ một chất ban đầu.
Đúng 1
Bình luận (0)
Câu 1:
+ Tác dụng với kim loại: O2 oxi hóa được hầu hết các kim loại trừ Ag, Au, Pt
+ Tác dụng với Hiđro, Phản ứng có thể gây nổ mạnh nếu tỉ lệ phản ứng O2:H2 = 1:2
+ Tác dụng với một số phi kim khác:
+ Tác dụng với một số hợp chất:
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
1:Nêu tính chất hóa học của H2O; tính chất hóa học của H2 và Viết phương trình phản ứng minh họa? 7:Cho 2,4 gam Mg tác dụng hết với 100 gam dung dịch H2SO4, tạo thành Magie sunfat và khí Hiđrô. a) Viết phương trình phản ứng xãy ra. b) Tính thể tích khí thoát ra ở ĐKTC? c) Tính nồng độ phần trăm của dung dịch H2SO4? Giúp nốt mik 2 câu này với ạ
a) \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
b) \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
Theo PTHH: \(n_{H_2}=n_{Mg}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c) \(C\%_{MgSO_4}=\dfrac{0,1.120}{2,4+100-0,1.2}.100\%\approx11,74\%\)
Đúng 2
Bình luận (0)
Hãy trình bày tính chất hóa học của axit sunfuric\, với mỗi tính chất chất hóa học hãy dẫn ra một PTHH để minh họa.
- Tác dụng với kim loại :
$Fe + H_2SO_4 \to FeSO_4 + H_2$
- Tác dụng với với oxit bazo
$CaO + H_2SO_4 \to CaSO_4 +H_2O$
- Tác dụng với bazo :
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
- Tác dụng với dung dịch muối
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
Đúng 1
Bình luận (0)
trình bày tính chất hóa học của muối ? cho ví dụ minh họa ?
trình bày tính chất hóa học của muối ? cho ví dụ minh họa ?
trình bày tính chất hóa học của nhôm? cho ví dụ phản ứng minh họa?
Tham khảo :
1. Tác dụng với phi kim
a) Tác dụng với oxi
Al bền trong không khí ở nhiệt độ thường do có lớp màng oxit Al2O3 rất mỏng bảo vệ.
b) Tác dụng với phi kim khác
2. Tác dụng với axit
+ Axit không có tính oxi hóa: dung dịch axit HCl, H2SO4 loãng
2Al + 6HCl → 2AlCl3 + 3H2↑
+ Axit có tính oxi hóa mạnh: dung dịch HNO3 loãng, HNO3 đặc, nóng và H2SO4 đặc, nóng.
Nhôm bị thụ động hoá trong dung dịch HNO3 đặc, nguội hoặc H2SO4 đặc nguội.
3. Tác dụng với oxit kim loại( Phản ứng nhiệt nhôm)
Lưu ý: Nhôm chỉ khử oxit của các kim loại đứng sau nhôm
4. Tác dụng với nước
- Phá bỏ lớp oxit trên bề mặt Al (hoặc tạo thành hỗn hống Al-Hg thì Al sẽ phản ứng với nước ở nhiệt độ thường)
2Al + 6H2O → 2Al(OH)3↓ + 3H2↑
5. Tác dụng với dung dịch kiềm
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
6. Tác dụng với dung dịch muối
- Al đẩy được kim loại đứng sau ra khỏi dung dịch muối của chúng:
Đúng 0
Bình luận (0)
a) Nêu tính chất hóa học của oxi , hidro . mỗi tính chất cho 2 puhh minh họa
b) Nêu nguyên liệu , viết pthh điều chế khí o2 , h2 trong phòng thí nghiệm
giúp e với ạ ,e cảm ơn
a) bạn tự học SGK
b) Nguyên liệu điều chế O2: KMnO4, KClO3, KNO3 (độc), H2O,...
2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
2KClO3 -> (t°, MnO2) 2KCl + 3O2
2KNO3 -> (t°) 2KNO2 + O2
2H2O -> (đp) 2H2 + O2
Nguyên liệu điều chế H2: Pb, Zn, Fe, Al, HCl, H2SO4 loãng,...
Fe + 2HCl -> FeCl2 + H2
2Al + 3H2SO4 ->
Al2(SO4)3 + 3H2
2H2O -> (đp) 2H2 + O2
Đúng 5
Bình luận (0)