Bài 2. Một số oxit quan trọng
Nội dung lý thuyết
Các phiên bản khácA. CANXI OXIT (CaO)
I. Tính chất
- Canxi oxit CaO (vối sống) là chất rắn màu trắng, nóng chảy ở nhiệt độ rất cao (khoảng 2585oC).
- Canxi oxit có đầy đủ tính chất hóa học của một oxit bazơ.

1. Tác dụng với nước
- CaO tan trong nước tạo thành chất rắn màu trắng, ít tan trong nước là Ca(OH)2, phần tan tạo thành dung dịch bazơ.
- Phản ứng này gọi là phản ứng tôi vôi và tỏa nhiều nhiệt. Phần Ca(OH)2 tan tạo thành dung dịch bazơ còn gọi là nước vôi trong.
CaO + H2O → Ca(OH)2
- CaO có tính hút ẩm mạnh nên được dùng để làm khô nhiều chất.
@209819@
2. Tác dụng với axit
CaO tác dụng với dung dịch axit HCl, phản ứng tỏa nhiệt, tạo thành muối canxi clorua CaCl2.
CaO + 2HCl → CaCl2 + H2O
Nhờ tính chất này, canxi oxit được dùng để khử chua cho đất trồng trọt do có hàm lượng axit quá cao, xử lí nước thải của nhiều nhà máy, hóa chất.
@209902@
3. Tác dụng với oxit axit
- Canxi oxit để lâu trong không khí hấp thụ khí cacbonic CO2 có trong không khí tạo thành canxi cacbonat.
CaO + CO2 → CaCO3
- Vì vậy, vôi sống sẽ bị giảm chất lượng nếu để lâu ngày trong tự nhiên và người ta thường sử dụng luôn vôi sống sau khi điều chế để tránh hiện tượng này.
Kết luận: Canxi oxit là oxit bazơ.
@209996@
II. ỨNG DỤNG
- Phần lớn lượng canxi oxit được dùng trong công nghiệp luyện kim và làm nguyên liệu cho công nghiệp hóa học.
- Ngoài ra, CaO dùng để khử chua đất trồng, xử lí nước thải công nghiệp, sát trùng, diệt nấm, khử độc môi trường...
III. ĐIỀU CHẾ VÀ SẢN XUẤT
Vôi sống CaO được sản xuất bằng cách nung đá vôi ở nhiệt độ trên 900oC.
1. Nguyên liệu
- Nguyên liệu chính là đá vôi.
- Chất đốt là than đá, củi, dầu, khí tự nhiên...
2. Các phản ứng hóa học xảy ra
Nung đá vôi bằng lò nung vôi thủ công hoặc lò nung vôi công nghiệp.
Đầu tiên, các chất đốt cháy tạo ra khí cacbonic và tỏa nhiều nhiệt:
C + O2 CO2
Nhiệt sinh ra sẽ phân hủy đá vôi thành vôi sống.
CaCO3 CaO + CO2
1. Canxi oxit là oxit bazơ: tác dụng với nước tạo thành bazơ, tác dụng với axit tạo thành muối và nước, tác dụng với oxit axit tạo thành muối.
2. Canxi oxit được dùng trong công nghiệp luyện kim, công nghiệp hóa học và dùng để khử đất chua, sát trùng, diệt nấm, khử độc môi trường...
3. Canxi oxit được sản xuất bằng phản ứng phân hủy canxi cacbonat ở nhiệt độ cao (trên 900oC).
B. LƯU HUỲNH ĐIOXIT (SO2)
Lưu huỳnh đioxit hay còn được gọi là khí sunfurơ, có công thức hóa học là SO2.
I. TÍNH CHẤT
- Lưu huỳnh đioxit là chất khí không màu, mùi hắc, tan nhiều trong nước, độc, nếu hít phải sẽ gây ho, viêm đường hô hấp, viêm phổi, đau mắt... và nặng hơn không khí (d= \(\dfrac{64}{29}\)).
- Lưu huỳnh đioxit có tính chất hóa học của một oxit axit.
1. Tác dụng với nước
Dẫn khí SO2 vào cốc đựng nước cất và thử dung dịch thu được bằng quỳ tím, thấy quỳ tím chuyển sang màu đỏ, chứng tỏ dung dịch thu được có tính axit.
Dung dịch thu được là dung dịch axit sunfurơ H2SO3.
SO2 + H2O → H2SO3
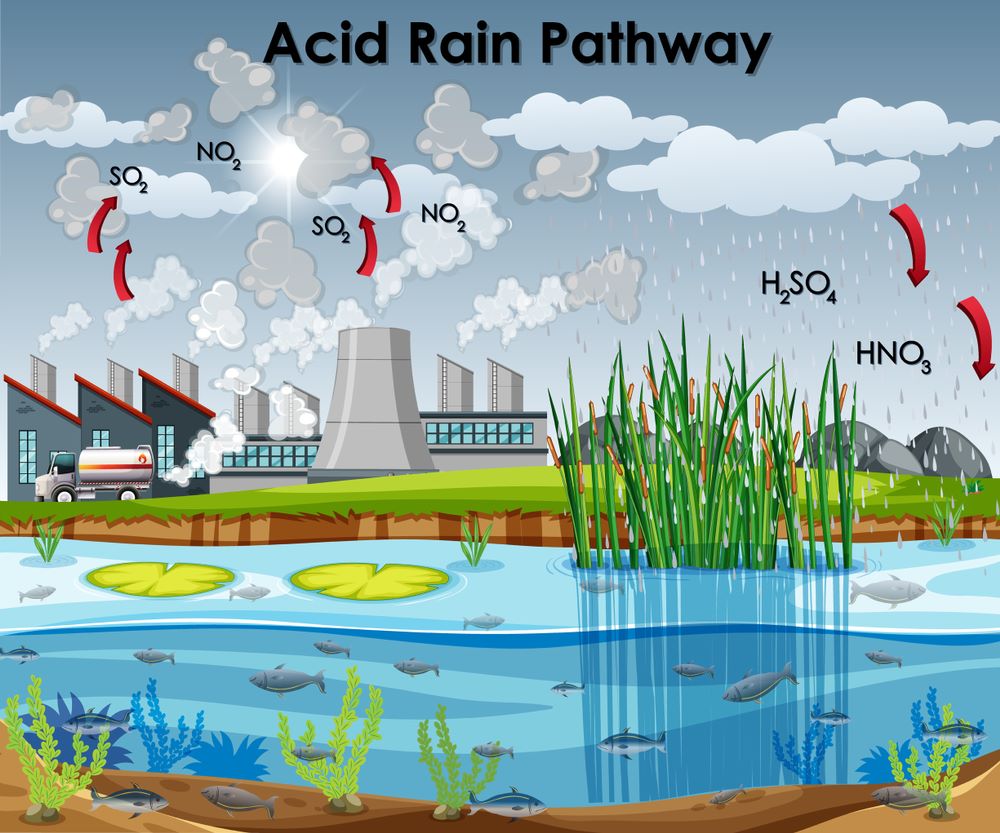
Vì vậy, SO2 là một trong những chất khí gây ô nhiễm không khí vì nó có thể tác dụng với hơi nước trong không khí hay với nước mưa tạo thành axit dẫn đến hiện tượng mưa axit. Mưa axit ăn mòn các công trình, phá hoại cây cối, biến đất đai thành vùng hoang mạc.
@210084@
2. Tác dụng với bazơ
Dẫn khí SO2 vào cốc đựng dung dịch Ca(OH)2, thấy xuất hiện kết tủa trắng canxi sunfit CaSO3.
SO2 + Ca(OH)2 → CaSO3 + H2O
3. Tác dụng với oxit bazơ
Lưu huỳnh đioxit tác dụng với oxit bazơ như Na2O, CaO,... tạo thành muối sunfit:
SO2 + Na2O → Na2SO3
Kết luận: Lưu huỳnh đioxit là oxit axit.
@210410@
II. ỨNG DỤNG
Phần lớn lượng SO2 được dùng để điều chế axit sunfuric H2SO4. Ngoài ra, SO2 còn dùng để tẩy trắng bột gỗ trong công nghiệp giấy, dùng làm chất diệt nấm mốc,...
III. ĐIỀU CHẾ
1. Trong phòng thí nghiệm
- Cho muối sunfit tác dụng với axit (dung dịch HCl, H2SO4), thu khí SO2 vào lọ bằng cách đẩy không khí.
Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O
- Đun nóng H2SO4 đặc với Cu.
2. Trong công nghiệp
- Đốt lưu huỳnh trong không khí: S + O2
SO2
- Đốt quặng pirit sắt FeS2: 4FeS2 + 11O2
2Fe2O3 + 8SO2
1. Lưu huỳnh đioxit là oxit axit: tác dụng với nước, dung dịch bazơ, oxit bazơ.
2. Ứng dụng quan trọng nhất của lưu huỳnh đi oxit là để sản xuất axit sunfuric.
3. Điều chế lưu huỳnh đioxit:
- Đốt lưu huỳnh trong không khí (trong công nghiệp).
- Muối sunfit tác dụng với axit HCl, H2SO4,... (trong phòng thí nghiệm).
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé . Chúc các em học tốt!
Danh sách các phiên bản khác của bài học này. Xem hướng dẫn