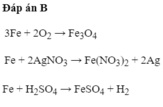Dự đoán khả năng phản ứng của muối carbonate kim loại nhóm IIA với dung dịch acid loãng.
H24
Những câu hỏi liên quan
36,0 gam hỗn hợp X gồm 2 kim loại (đều ở nhóm IIA, 2 chu kì liên tiếp) phản ứng hết với dung dịch H2SO4 loãng, sinh ra 22,4 lít khí H2 (đktc). Hai kim loại là?
Gọi công thức của hai kim loại cần tìm là A và B
công thức trung bình của hai kim loại là \(\overline{R}\)
PTHH : \(\overline{R}+H_2SO_4-->\overline{R}SO_4+H_2\uparrow\)
Theo PTHH : \(n_{\overline{R}}=n_{H_2}=\dfrac{22,4}{22,4}=1\left(mol\right)\)
\(\Rightarrow M_{\overline{R}}=\dfrac{36}{1}=36\) (g/mol)
Có : \(M_A< M_R=36< M_B\)
Mà : A và B thuộc hai chu kì liên tiếp
=> \(\left\{{}\begin{matrix}A:Mg\\B:Ca\end{matrix}\right.\)
Vậy ...
Đúng 1
Bình luận (0)
Cho 14,2g X gồm hai muối cacbonat của hai kim loại phân nhóm chính IIA thuộc 2 chu kỳ kế tiếp nhau phản ứng với dung dịch HCl dư được 3,36lít CO2 đktc . Tìm 2 kim loại đó A. Mg và Ca B. Ba và Sr C. Ca và Sr D. Be và Mg
Đọc tiếp
Cho 14,2g X gồm hai muối cacbonat của hai kim loại phân nhóm chính IIA thuộc 2 chu kỳ kế tiếp nhau phản ứng với dung dịch HCl dư được 3,36lít CO2 đktc . Tìm 2 kim loại đó
A. Mg và Ca
B. Ba và Sr
C. Ca và Sr
D. Be và Mg
nCO2 = 0,15
H+ + CO32- → CO2 + H2O
⇒ nX = nCO32- = nCO2 = 0,15
⇒ MX ≈ 94,67
⇒ X gồm 2 muối MgCO3 (84) và CaCO3 (100)
Đáp án A
Đúng 0
Bình luận (0)
Cho 11,2g một kim loại X phản ứng với 200ml dung dịch HCl 2M thu được muối của kim loại hóa trị II
a)Xác định kim loại X.
b)Tính CM dung dịch sau phản ứng
200ml = 0,2l
Số mol của dung dịch axit clohidric
CMHCl = \(\dfrac{n}{V}\Rightarrow n=C_M.V=2.0,2=0,4\left(mol\right)\)
Pt : X + 2HCl → XCl2 + H2\(|\)
1 2 1 1
0,2 0,4 0,2
a) Số mol của kim loại X
nX = \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
⇒ MX = \(\dfrac{m_X}{M_X}=\dfrac{11,2}{0,2}=56\)
Vậy kim loại X là sắt
b) Số mol của sắt (II) clorua
nFeCl2 = \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
Nồng độ mol của sắt (II) clorua
CMFeCl2 = \(\dfrac{n}{V}=\dfrac{0,2}{0,2}=1\left(M\right)\)
Chúc bạn học tốt
Đúng 3
Bình luận (0)
31,2g muối clorua của kim loại M nhóm IIA tác dụng vừa hết với dung dịch H2SO4 20% thu được 34,95g một muối sunfat kết tủa.
a,Tìm M
b,Tính khối lượng dung dịch H2SO4 đã dùng.
c,Tính nồng độ % của chất thu được sau phản ứng.
a)
$MCl_2 + H_2SO_4 \to MSO_4 + 2HCl$
$n_{MCl_2}= n_{MSO_4}$
$\Rightarrow \dfrac{31,2}{M + 71} = \dfrac{34,95}{M + 96}$
$\Rightarrow M = 137(Bari)$
b)
$n_{H_2SO_4} = n_{BaSO_4} = \dfrac{34,95}{233} = 0,15(mol)$
$m_{dd\ H_2SO_4} = \dfrac{0,15.98}{20\%} = 73,5(gam)$
c)
$n_{HCl} = 2n_{BaSO_4} = 0,3(mol)$
$m_{dd}= 31,2 + 73,5 - 34,95 = 69,75(gam)$
$C\%_{HCl} = \dfrac{0,3.36,5}{69,75}.100\% = 15,7\%$
Đúng 2
Bình luận (0)
Cho 6,8 gam hỗn hợp G gồm hai kim loại A và B liên tiếp trong nhóm IIA tác dụng với dung dịch H 2 S O 4 loãng dư, sau phản ứng thu được 5,6 lít khí (ở đktc). Xác định thành phần % khối lượng của từng kim loại trong G.
Trong các kim loại phân nhóm IIA dãy kim loại phản ứng với nước tạo thành dung dịch kiềm
A. Be, Mg, Ca
B. Ca, Sr, Ba
C. Be, Mg, Ba
D. Ca, Sr, Mg
Đáp án B
Be, Mg ở điều kiện thường không phản ứng với nước.
Đúng 0
Bình luận (0)
Hòa tan 13,4 g hỗn hợp hai muối cacbonat thuộc hai chu kì liên tiếp nhau trong nhóm IIA với một lượng dung dịch HCl dư 10%. Sau phản ứng thu được dung dịch X, cô cạn dung dịch X thì thu được 15, 05g muối khan.
a. Xác định tên của 2 kim loại
b. Cho dung dịch X tác dụng hoàn toàn với dung dịch NaOH 1M thì thu được m g dung dịch. Tính mg và thể tích dung dịch NaOH đã dùng
Xem chi tiết
Gọi công thức chung của 2 muối là RCO3
PTHH: \(RCO_3+2HCl\rightarrow RCl_2+H_2O+CO_2\uparrow\)
a) Theo PTHH: \(n_{RCO_3}=n_{RCl_2}\)
\(\Rightarrow\dfrac{13,4}{\overline{M}_R+60}=\dfrac{15,05}{\overline{M}_R+71}\) \(\Rightarrow\overline{M}_R\approx29,33\left(đvC\right)\)
Mà 2 kim loại thuộc 2 chu kì liên tiếp
\(\Rightarrow\) 2 kim loại cần tìm là Magie và Canxi
b) Mình không biết CaCl2 có tác dụng với NaOH hay không nên thôi !
Đúng 3
Bình luận (0)
Kim loại X có những tính chất hóa học sau- Phản ứng với oxi khi nung nóng- Phản ứng với dung dịch
A
g
N
O
3
- Phản ứng với dung dịch
H
2
S
O
4
loãng giải phóng khí
H
2
và muối của k...
Đọc tiếp
Kim loại X có những tính chất hóa học sau
- Phản ứng với oxi khi nung nóng
- Phản ứng với dung dịch A g N O 3
- Phản ứng với dung dịch H 2 S O 4 loãng giải phóng khí H 2 và muối của kim loại hóa trị II. Kim loại X là
A. Cu
B. Fe
C. Al
D. Na
Đáp án B
A loại vì Cu không phản ứng với H2SO4 loãng
C loại vì Al có hóa trị III trong hợp chất D loại vì Na có hóa trị I trong hợp chấ
Đúng 0
Bình luận (0)
Kim loại X có những tính chất hóa học sau:
- Phản ứng với oxit khi nung nóng.
- Phản ứng với dung dịch A g N O 3 .
- Phản ứng với dung dịch H 2 S O 4 loãng giải phóng khí và H 2 muối của kim loại hóa trị II. Kim loại X là:
A. Cu
B. Fe
C. Al
D. Na
Hòa tan hết 4,52 gam hỗn hợp gồm hai muối cacbonat của hai kim loại nhóm IIA thuộc hai chu kì kế tiếp nhau bằng 200 ml dung dịch HCl 0,5M. Sau phản ứng thu được dung dịch C và 1,12 lít khí D (đktc). Khối lượng chất tan trong dung dịch C và hai kim loại là A. 5,07 gam và Mg, Ca B. 5,70 gam và Be, Mg C. 5,70 gam và Mg, Ca D. 5,07 gam và Sr, Ba
Đọc tiếp
Hòa tan hết 4,52 gam hỗn hợp gồm hai muối cacbonat của hai kim loại nhóm IIA thuộc hai chu kì kế tiếp nhau bằng 200 ml dung dịch HCl 0,5M. Sau phản ứng thu được dung dịch C và 1,12 lít khí D (đktc). Khối lượng chất tan trong dung dịch C và hai kim loại là
A. 5,07 gam và Mg, Ca
B. 5,70 gam và Be, Mg
C. 5,70 gam và Mg, Ca
D. 5,07 gam và Sr, Ba