cân bằng các phương trình hóa học sau:
FexOy+HCl->FeCl2y/x+H2O
KMnO4+HCl->KCl+MnCl2+Cl2+H2O
Zn + H2SO4 → ZnSO4 + H2S + H2O
MnO2 + HCl → MnCl2 + Cl2 + H2O
KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
KMnO4 + K2SO3 + H2O→ K2SO4 + MnO2 + KOH
Cân bằng electron
VD.

Giúp em với ạ !
Cân bằng các phương trình phản ứng oxi hóa – khử sau bằng phương pháp thăng bằng electron:
a) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O.
b) HNO3 + HCl → NO + Cl2 + H2O.
c) HClO3 + HCl → Cl2 + H2O.
d) PbO2 + HCl → PbCl2 + Cl2 + H2O
Cân bằng các phản ứng oxi hóa – khử sau bằng phương pháp thăng bằng electron:
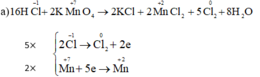
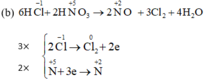
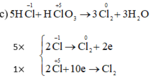
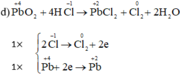
1. Cân bằng phương trình hóa học của các phản ứng sau bằng phương pháp thăng bằng electron. Cho biết chất oxi hóa và chất khử của mỗi phản ứng :
Fe + H2SO4 đặc,nóng → Fe2 (SO4)3 + SO2 + H2O
KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
2. Tính khối lượng CaF2 cần dùng để điều chế 2,5 kg dung dịch axit Flohidric nồng độ 40%.
3. Hòa tan 11 gam hỗn hợp bột sắt và nhôm trong dung dịch HCl thu được 8,96 lit khí (điều kiện tiêu chuẩn).
a. Xác định thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp. b. Tính thể tích dung dịch HCl 2M đã dùng.
(Cho Ca = 40; F = 19; H =1; Fe = 56; Al = 27)
Bài 2:
\(m_{HF}=\dfrac{2,5.40\%}{100\%}=1(kg)\\ \Rightarrow n_{HF}=\dfrac{1}{20}=0,05(kmol)\\ PTHH:CaF+H_2SO_4\to CaSO_4+2HF\\ \Rightarrow n_{CaF}=0,025(kmol)\\ \Rightarrow m_{CaF}=0,025.78=1,95(kg)\)
Bài 3:
\(a,\) Đặt \(\begin{cases} n_{Fe}=x(mol)\\ n_{Al}=y(mol) \end{cases} \)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ PTHH:2Al+6HCl\to 2AlCl_3+3H_2\\ Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow \begin{cases} 56x+27y=11\\ x+1,5y=0,4 \end{cases} \Rightarrow \begin{cases} x=0,1(mol)\\ y=0,2(mol) \end{cases}\\ \Rightarrow \begin{cases} \%_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\\ \%_{Al}=100\%-50,91\%=49,09\% \end{cases} \)
\(b,\Sigma n_{HCl}=3n_{Al}+2n_{Fe}=0,2+0,6=0,7(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,7}{2}=0,35(l)\)
Cân bằng PTHH của các phản ứng oxi hoá- khử sau bằng phương pháp thăng bằng electron (xác định chất khử, chất oxi hoá, quá trình khử, quá trình oxi hóa).
1) KClO3+HCl --> KCl +Cl2+H2O
2)K2Cr2O7 +HCl -->KCl+CrCl3 +Cl2+H2O
3) KMnO4 +HCl --> KCl+MnCl2+Cl2+H2O
4)Al+HNO3 --> Al(NO3)3+N2O+H2O
5)Fe3O4 +HNO3 -->Fe(NO3)3 +NO+H2O
6) FeS +O2 --> Fe2O3 +SO2
giúp mình với
Tổng hệ số nguyên tối giản của phương trình hóa học:
H C l + K M n O 4 → M n C l 2 + C l 2 + K C l + H 2 O là
A. 35.
B. 34.
C. 36.
D. 33.
PTHH: 16 H C l + 2 K M n O 4 → 2 M n C l 2 + 5 C l 2 + 2 K C l + 8 H 2 O .
Tổng hệ số nguyên tối giản của phương trình hóa học: 16 + 2 + 2 +5 + 2 + 8 = 35.
Chọn đáp án A.
cho phương trình hóa học: KMnO4 + HCl -> KCl + MnCl2 + Cl2 + H2O. Số phân tử HCl đóng vai trò chất khử, đóng vai trò môi trường là:
A. 10,6
B. 10,16
C. 2,16
D. 6,10
cho phương trình hóa học: KMnO4 + HCl -> KCl + MnCl2 + Cl2 + H2O. Số phân tử HCl đóng vai trò chất khử, đóng vai trò môi trường là:
A. 10,6
B. 10,16
C. 2,16
D. 6,10
Cho phản ứng HCl + KMnO4 → KCl + Cl2 + MnCl2 + H2O.
Tổng hệ số (số nguyên, tối giản) tất cả các chất trong phương trình hóa học của phản ứng trên là
A. 35
B. 34
C. 32
D. 37
Chọn A
16HCl + 2KMnO4 → 2KCl + 5Cl2 + 2MnCl2 + 8H2O.
4. Cân bằng phương trình hóa học của các phản ứng sau bằng phương pháp thăng bằng electron. Cho biết chất oxi hóa và chất khử của mỗi phản ứng :
Al + H2SO4 đặc,nóng Al2 (SO4)3 + SO2 + H2O
MnO2 + HCl MnCl2 + Cl2 + H2O
Câu 1: Cân bằng phản ứng oxi hóa khử sau theo phương pháp thăng bằng electron, chỉ rõ chất khử, chất oxi hóa, sự oxi hóa, sự khử:
(1) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
(2) HNO3 + Cu→ Cu(NO3)2 + NO2 + H2O 80
(3) NH3 + O2 NO + H2O
(1) \(K\overset{+7}{Mn}O_4+H\overset{-1}{Cl}\rightarrow KCl+\overset{+2}{Mn}Cl_2+\overset{0}{Cl_2}+H_2O\)
- Chất khử: HCl
Chất oxh: KMnO4
- Sự oxh: \(2Cl^{-1}\rightarrow Cl_2^0+2e|\times5\)
Sự khử: \(Mn^{+7}+5e\rightarrow Mn^{+2}|\times2\)
\(\rightarrow2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
(2) \(H\overset{+5}{N}O_3+\overset{0}{Cu}\rightarrow\overset{+2}{Cu}\left(NO_3\right)_2+\overset{+4}{N}O_2+H_2O\)
- Chất khử: Cu
Chất oxh: HNO3
- Sự khử: \(N^{+5}+1e\rightarrow N^{+4}|\times2\)
Sự oxh: \(Cu^0\rightarrow Cu^{+2}+2e|\times1\)
\(\rightarrow4HNO_3+Cu\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\)
(3) \(\overset{-3}{N}H_3+\overset{0}{O_2}\rightarrow\overset{+2}{N}\overset{-2}{O}+H_2O\)
- Chất khử: NH3
Chất oxh: O2
- Sự khử: \(O_2^0+4e\rightarrow2O^{-2}|\times5\)
Sự oxh: \(N^{-3}\rightarrow N^{+2}+5e|\times4\)
\(\rightarrow4NH_3+5O_2\rightarrow4NO+6H_2O\)