Phần trăm khối lượng của Cu trong CuO là
A. 60%
B. 70%
C. 80%
D. 50%
Phần trăm khối lượng của Cu trong CuO là
A. 60%
B. 70%
C. 80%
D. 50%
Câu 62) Thành phần phần trăm khối lượng của các nguyên tố Cu và O2 trong đồng(II)oxit lần lượt là:
A. 70% và 30%
B. 60% và 30%
C. 80% và 20%
D. 79% và 21%
Câu 71) Oxit của 1 nguyên tố có hoá trị II chứa 20% oxi(về khối lượng). Oxit có CT hoá học là:
A. CuO
B. CaO
C. FeO
D. MgO
Câu 100) phải hoà tan thêm bao nhiêu gam KOH nguyên chất vào 1200g dung dịch KOH 12% để có dung dịch KOH 20%
A. 199g
B. 121g
C. 130g
D. 120g
Câu 62 :
$\%Cu = \dfrac{64}{80}.100\% = 80\%$
$\%O = 100\% -80\% = 20\%$
Đáp án C
Câu 71 :
CTHH : RO
$\%O = \dfrac{16}{R + 16}.100\% = 20\%$
Suy ra $R = 64(Cu)$
Đáp án A
Gọi $m_{KOH} = a(gam)$
Sau khi thêm :
$m_{KOH} = a + 1200.12\% = a + 144(gam)$
$m_{dd} = a + 1200(gam)$
Suy ra :
$\dfrac{a + 144}{a + 1200} = \dfrac{20}{100}$
Suy ra a = 120(gam)
Đáp án D
cho 20 gam hổn hợp X gồm cuo và fe2o3 tác dụng vừa đủ với 0,2l dd hcl có nồng đọ 3,5M. Thành phần phần trăm theo khối lượng của cuo và fe2o3 trong hỗn hợp x lần lượt là:
a 30% và 70%
b 20% và 80%
c 22% và 78%
d 25% và 75%
b) 20 % và 80%
Gọi \(n_{CuO} và n_{Fe_2O_3} là x y\)
\(\begin{cases} 80x + 160y= 20\\ 2x+ 6y= 0,2 . 3,5=0,7 \end{cases} \)
x=0,05
y= 0,1
%\(m_{CuO}= \dfrac{0,05 . 80}{20} . 100\)%= 20%
=> %m\(Fe_2O_3\)= 80%
Câu 17. Phần trăm về khối lượng của nguyên tố Fe trong hợp chất Fe2O3 là:
A.70% B. 60% C. 50% D. 30%
Câu 18. Công thức hóa học của hợp chất tạo bởi 80% Cu và 20%O. Biết khối lượng phân tử là 80 amu:
A. Cu2O B. CuO C. CuO2 D. Cu2O2
Câu 19. Liên kết cộng hóa trị được hình thành do
A. Lực hút tĩnh điện yếu giữa các nguyên tử.
B. Các cặp electron dùng chung.
C. Các đám mây electron.
D. Các electron hoá trị.
Câu 20. Trong phân tử potassium chloride, nguyên tử K (potassium) và nguyên tử Cl (chlorine) liên kết với nhau bằng liên kết
A. cộng hóa trị. B. ion. C. phi kim. D. kim loại.
Câu 21. Biết N có hoá trị IV, hãy chọn công thức hoá học phù hợp với qui tác hoá trị trong đó có các công thức sau:
A. NO B. N2O C. N2O3 D. NO2
Câu 22. Nguyên tố X có hoá trị III, công thức của X với SO4 là:
A. XSO4 B. X(SO4)3 C. X2(SO4)3 D. X3SO4
Câu 23. Tốc độ chuyển động của vật có thể cung cấp cho ta thông tin gì về chuyển động của vật?
A. Cho biết hướng chuyển động của vật.
B. Cho biết vật chuyển động theo quỹ đạo nào.
C. Cho biết vật chuyển động nhanh hay chậm.
D. Cho biết nguyên nhân vì sao vật lại chuyển động được.
Câu 24. Đơn vị của tốc độ là:
A. m.h B. km/h C. m.s D. s/km
Câu 25. 54 km/h = ................m/s?
A. 10 m/s B.15 m/s C. 20m/s D. 18m/s
Câu 26. Theo quy tắc “3 giây” khoảng cách an toàn đối với ô tô chạy với tốc độ 25 m/s là bao nhiêu?
A. 35 m B. 55 m C. 75 m D. 100 m
Câu 27. Khi nói đến tốc độ chuyển động của các phương tiện giao thông như xe máy, ô tô, xe lửa, máy bay… người ta nói đến:
A. Tốc độ tức thời của chuyển động.
B. Tốc độ trung bình của chuyển động.
C. Tốc độ lớn nhất có thể đạt được của phương tiện đó.
D. Tốc độ nhỏ nhất có thể đạt được của phương tiện đó.
Câu 28. Một vật chuyển động càng nhanh khi:
A. Quãng đường đi được càng lớn.
B. Thời gian chuyển động càng ngắn.
C. Tốc độ chuyển động càng lớn.
D. Quãng đường đi trong 1s càng ngắn.
Câu 29. Để đo tốc độ của một người chạy cự li ngắn, ta cần những dụng cụ đo nào?
A. Thước cuộn và đồng hồ bấm giây
B. Thước thẳng và đồng hồ treo tường
C. Đồng hồ đo thời gian hiện số kết nối với cổng quang điện.
D. Cổng quang điện và đồng hồ bấm giây.
Câu 30. Trong phòng thí nghiệm, người ta thường sử dụng những dụng cụ đo nào để đo tốc độ của các vật chuyển động nhanh và có kích thước nhỏ?
A. Thước, cổng quang điện và đồng hồ bấm giây.
B. Thước, đồng hồ đo thời gian hiện số kết nối với cổng quang điện.
C. Thước và đồng hồ đo thời gian hiện số.
D. Cổng quang điện và đồng hồ bấm giây.
Câu 31. Để vẽ đồ thị quãng đường thời gian cho một chuyển động thì trước hết phải làm gì?
A. Cần lập bảng ghi quãng đường đi được theo thời gian.
B. Cần vẽ hai trục tọa độ
C. Cần xác định các điểm biểu diễn quãng đường đi được theo thời gian.
D. Cần xác định vận tốc của các vật.
(Gíup tui nha cần gấp ạ)![]()
17.A
18.B
19.B
20.B
21.D
22.C
23.C
24.B
25.B
26. (theo mình là 70m)
27.B
28.C
29.A
30.B
31.A.
Hãy xác định công thức hóa học của hợp chất X biết: (a) Phần trăm khối lượng của các nguyên tố trong X là 50%S, còn lại là oxi. (b) Phần trăm khối lượng của các nguyên tố trong X là 80%Cu, còn lại là O. (c) Phần trăm khối lượng của các nguyên tố trong X là 2%H, 32,65%S, còn lại là O
Hỗn hợp rắn gồm CuO và Cu có khối lượng 10g cho tác dụng với dung dịch axit sunfuric loãng, dư còn lại 8,4g chất rắn. Phần trăm về khối lượng CuO và Cu trong hỗn hợp rắn ban đầu
\(\%m_{Cu}=\dfrac{8,4}{10}\cdot100\%=84\%\\ \%_{CuO}=100\%-84\%=16\%\)
Hòa tan hết 50 gam hỗn hợp X gồm Cu và CuO trong H2SO4 đặc, nóng, dư thu được 11,2 lít khí SO2 (sản phẩm khử duy nhất ở đktc). Phần trăm khối lượng của CuO trong hỗn hợp X là
A. 64%.
B. 36%.
C. 32%.
D. 68%.
Đáp án B
Số mol SO2 thu được là: n SO 2 = 11 , 2 22 , 4 = 0 , 5 mol
Sơ đồ phản ứng:
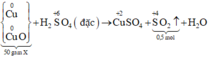
Các quá trình nhường , nhận electron:
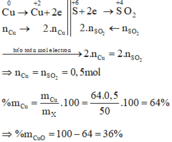
Một hợp chất tạo bởi Cu và O có phân tử khối = 80 đơn vị Cacbon trong đó phần trăm khối lượng Cu = 80% .xác định công thức hóa học của hợp chất
Gọi CTHH là CuxOy
Ta có: \(\%Cu=\frac{64x}{80}\times100\%=80\%\)
\(\Leftrightarrow\frac{64x}{80}=0,8\)
\(\Rightarrow64x=64\)
\(\Leftrightarrow x=1\)
Ta có: \(PTK_{CuO_y}=80\)
\(\Leftrightarrow NTK_{Cu}+yNTK_O=80\)
\(\Leftrightarrow64+16y=80\)
\(\Leftrightarrow y=\frac{80-64}{16}=1\)
Vậy CTHH là CuO
Cho CO dư đi qua hỗn hợp X gồm Fe3O4 ; MgO ; CuO và Al2O3 nung nóng thấy khối lượng X giảm 20% và thu được chất rắn Y . Cho Y qua dung dịch NaOH dư, khuấy kỹ còn lại phần không tan Z có khối lượng bằng 80% khối lượng của Y . Tìm phần trăm khối lượng của Al2O3 trong X
A. 24%
B. 64%
C. 16%
D. 20%
Giả sử mX = 100g ⇒ mY = 80g
Y gồm Fe, Cu, MgO , Al2O3
Z gồm Fe, Cu, MgO
⇒ mAl2O3 = mY – mZ = 80 - 80×80% = 16g
⇒ %mAl2O3 = 16%
Đáp án C
Cho hỗn hợp X gồm 60% Fe2O3 và 40% CuO về khối lượng. Khử hoàn toàn 20 gam hỗn hợp X bằng luồng khí H2 dư thu được hỗn hợp kim loại Y. Thành phần phần trăm về khối lượng kim loại Cu trong Y?
\(m_{CuO}=\dfrac{20.40}{100}=8\left(g\right)\) => \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
\(m_{Fe_2O_3}=\dfrac{60.20}{100}=12\left(g\right)\) => \(n_{Fe_2O_3}=\dfrac{12}{160}=0,075\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
______0,1---------------->0,1
Fe2O3 + 3CO --to--> 2Fe + 3CO2
0,075---------------->0,15
=> \(\%Cu=\dfrac{0,1.64}{0,1.64+0,15.56}.100\%=43,243\%\)