TH
Những câu hỏi liên quan
Lập CTHH của oxit và gọi tên:a) Oxit của nhôm.b) Oxit của Mn, biết Mn có hóa trị (IV).c) Oxit của lưu huỳnh, biết S có hóa trị VI.d) Oxit của nitơ, biết N có hóa trị III.e) Oxit của magie, biết Mg có hóa trị II.f) Oxit của kali, biết K có hóa trị I.
a, Al2O3 _ Nhôm oxit.
b, MnO2 _ Mangan đioxit.
c, SO3 _ Lưu huỳnh trioxit.
d, N2O3 _ Đinitơ trioxit.
e, MgO _ Magie oxit.
f, K2O _ Kali oxit.
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
a, Al2IIIO3II
b, MnIVO2II
c, SIVO2II
d, N2IIIO3II
e, MgIIOII
f, K2IOII
Đúng 0
Bình luận (1)
a) Oxit của nhôm._ Al2O3 _nhôm oxit
b) Oxit của Mn, biết Mn có hóa trị (IV)._ MnO2 _mangan đi oxit
c) Oxit của lưu huỳnh, biết S có hóa trị VI._ SO2 _lưu huỳnh đi oxit
d) Oxit của nitơ, biết N có hóa trị III._ N2O3 _đi nitơ tri oxit
e) Oxit của magie, biết Mg có hóa trị II._ MgO _magie oxit
f) Oxit của kali, biết K có hóa trị I._ K2O _kali oxit
Đúng 0
Bình luận (0)
Hãy tìm công thức hóa học đơn giản nhất của một loại oxit của lưu huỳnh, biết rằng trong oxit này có 2g lưu huỳnh kết hợp với 3g oxi.
Số mol của nguyên tử lưu huỳnh là: 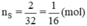
Số mol của nguyên tử oxi là: 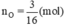
Ta có: 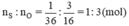
⇒ Trong một phân tử lưu huỳnh trioxit có 1 nguyên tử S và có 3 nguyên tử O.
Vậy công thức hóa học đơn giản nhất của oxit lưu huỳnh là SO3.
Đúng 0
Bình luận (0)
Bài 4: hãy tìm CTHH đơn giản nhất của một loại lưu huỳnh oxit, biết rằng trong oxit này có 2g lưu huỳnh kết hợp với 3g oxi
Gọi công thức là SxOy (x,y \(\in\) N*)
x : y = \(\dfrac{2}{32}:\dfrac{3}{16}\)
= 0,0625 : 0,1875
= 1 : 3
\(\rightarrow\) x = 1, y = 3
Vậy công thức là SO3
Đúng 0
Bình luận (0)
Gọi CTHH dạng chung là SxOy
Ta có x:y=\(\dfrac{2}{32}:\dfrac{3}{16}=1:3\)
=>x=1;y=3
Vậy CTHH:SO3
Chúc bạn học tốt![]()
Đúng 0
Bình luận (0)
Hãy tìm công thức hóa học đơn giản nhất của một loại oxit của lưu huỳnh, biết rằng trong oxit này có 2 g lưu huỳnh kết hợp với 3 g oxi.
\(\frac{n_S}{n_O}=\frac{\frac{2}{32}}{\frac{3}{16}}=\frac{1}{3}\Rightarrow SO_3\)
Đúng 0
Bình luận (1)
Giả sử CTHH là SxOy , ta có tỉ lệ:
\(\dfrac{x}{y}\)=\(\dfrac{2}{32}\):\(\dfrac{3}{16}\)=\(\dfrac{1}{3}\)⇒CTHH là SO3
Đúng 0
Bình luận (1)
Giả sử CTHH là SxOy , ta có tỉ lệ:
xyxy=232232:316316=1313⇒CTHH là SO3
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
a) Khi đốt cháy 6g kim loại A hoá trị II cần vừa đủ 2,8 lít oxit (dktc). Xác định tên kiem loại A và CTHH oxit đó ?
b) Muốn tạo ra 128g một oxit lưu huỳnh cần đốt cháy 64g lưu huỳnh trong õi. Tìm CTHH của oxit lưu huỳnh trên?
Gọi CTTQ là AO
2A+O2-->2AO
nO2=2,8:22,4=0,125mol
theo PTHH-->nA =2nO2=0,125x2=0,25mol
MA=6:0,25=24
--> Kim loại đó là Mg
Đúng 0
Bình luận (0)
a. PTHH: \(2A+O_2\underrightarrow{t^o}2AO\\ 0,25mol:0,125\rightarrow0,25mol\)
\(n_{O_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\)
\(M_A=\dfrac{6}{0,25}=24\left(g/mol\right)\)
Vậy kim loại đó là Magie, kí hiệu Mg.
b. PTHH: \(S+O_2\rightarrow SO_2\\ 2mol:2mol\rightarrow2mol\)
\(n_S=\dfrac{64}{32}=2\left(mol\right)\)
\(M_{Oxit}=\dfrac{128}{2}=64\left(g/mol\right)\)
\(\left[{}\begin{matrix}M_{SO_2}=32+32=64\left(g/mol\right)\left(Đ\right)\\M_{SO_3}=32+48=80\left(g/mol\right)\left(S\right)\end{matrix}\right.\)
Vậy CTHH của lưu huỳnh oxit trên là \(SO_2\)
Đúng 0
Bình luận (3)
Gọi CTHH của kin loại là 2AO
Số mol 02 là:
nO2=\(\dfrac{2,8}{22,4}\) =0,125(mol)
PTHH
2A + .......O2 ➞to ........2AO
.2mol........1mol.............2mol
.x=?mol ...0,125mol
Số mol A là:
nA=x=\(\dfrac{0,125.2}{1}\) =0,25 (mol)
Khối lượng mol của A là :
MA=\(\dfrac{mA}{nA}\) \(\dfrac{6}{0,25}\) =24g/mol
vậy tên nguyên tố là Mg(magie)
Đúng 0
Bình luận (0)
Một oxit của lưu huỳnh có thành phần trăm của lưu huỳnh là 50% và Oxi là 50%.Biết oxit này có khối lượng mol phân tử là 64g/mol.Hãy tìm công thức hóa học của oxit đó.
Ta có: \(\left\{{}\begin{matrix}m_S=64\cdot50\%=32\left(g\right)\\m_O=64\cdot50\%=32\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_S=\dfrac{32}{32}=1\left(mol\right)\\n_O=\dfrac{32}{16}=2\left(mol\right)\end{matrix}\right.\)
Vậy CTHH là \(SO_2\)
Đúng 2
Bình luận (2)
một hợp chất A gồm 2 nguyên tố hóa học là lưu huỳnh và Oxi trong đó lưu huỳnh chiếm 40% theo khối lượng. Hãy tìm CTHH của khí A, biết rằng ở đktc 1 gam khí A chiểm thế tích là 0,28l
\(M_A=\dfrac{1}{\dfrac{0,28}{22,4}}=80\left(g/mol\right)\)
\(m_S=\dfrac{40.80}{100}=32\left(g\right)\Rightarrow n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=80-32=48\left(g\right)\Rightarrow n_O=\dfrac{48}{16}=3\left(mol\right)\)
=> CTHH: SO3
Đúng 4
Bình luận (0)
Bài 15: Một hợp chất oxit (X) của lưu huỳnh, trong đó hàm lượng của lưu huỳnh chiếm 50% theo khối lượng. Hãy xác định CTHH của oxit X
Gọi CTHH là \(SO_x\)
\(\%S=\dfrac{32}{32+16x}\cdot100\%=50\%\Rightarrow x=2\)
Vậy CTHH là \(SO_2\)
Đúng 6
Bình luận (0)
Một oxit của lưu huỳnh có thành phần trăm của lưu huỳnh là 50% và Oxi là 50%.Hãy tìm công thức hóa học của oxit đó.
Gọi CTHH của oxit là $S_xO_y$
Ta có :
$\dfrac{32x}{50} = \dfrac{16y}{50} \Rightarrow \dfrac{x}{y} = \dfrac{1}{2}$
Vậy CTHH là $SO_2$
Đúng 0
Bình luận (0)








