Đốt cháy hoàn toàn 7,2 gam một hidrocacbon cần vừa đủ 17,92 lit O2 . Tìm CTPT hidrocacbon
TN
Những câu hỏi liên quan
Hỗn hợp khí A gồm metan và một hidrocacbon. Đốt cháy hoàn toàn 1.0 lít A cần dùng vừa đủ 2.6 lít khí O2. Dẫn toàn bộ sản phẩm qua bình đựng H2SO4 đặc thấy 1.6 lít khí KHÔNG bị hấp thụ. Xác định CTPT của hidrocacbon
Đốt cháy hoàn toàn 4,3g hidrocacbon X cần dùng vừa đủ V lít O2 (đktc). Sản phẩm cháy cho hấp thụ hết vào bình đựng dd Ca(OH)2. Sau khi các pứ xảy ra hoàn toàn thu đc 20g kết tủa và 1 dd có khối lượng giảm 0.5g.
Xem chi tiết
a. Xác định CTPT của X
b. Tính V
c. Xác định công thức cấu tạo của X. Biết khi mono clo hóa X thu được tối đa 4 sản phẩm thế
\(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\)
Đặt CTHH của X là \(C_xH_y\)
\(C_xH_y+\left(x+\dfrac{y}{4}\right)O_2\underrightarrow{t^o}xCO_2+\dfrac{y}{2}H_2O\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
\(m_{dd.giảm}=m_{kt}-\left(m_{CO_2}+m_{H_2O}\right)\\ \Leftrightarrow0,5=20-\left(m_{CO_2}+m_{H_2O}\right)\\ \Rightarrow m_{CO_2}+m_{H_2O}=20-0,5=19,5\left(g\right)\left(I\right)\)
Mặt khác:
\(m_{O_2}=m_{CO_2}+m_{H_2O}-m_X=19,5-4,3=15,2\left(g\right)\\ \Rightarrow n_{CO_2}+0,5n_{H_2O}=\dfrac{15,2}{32}=0,475\left(mol\right)\left(II\right)\)
Từ (I), (II) suy ra: \(\left\{{}\begin{matrix}n_{CO_2}=0,3\\n_{H_2O}=0,35\end{matrix}\right.\)
Vì \(n_{H_2O}>n_{CO_2}\Rightarrow X:ankan\) \(\left(C_nH_{2n+2}\right)\)
\(n=\dfrac{n_{CO_2}}{n_{H_2O}-n_{CO_2}}=\dfrac{0,3}{0,35-0,3}=6\)
a
CTPT của X: \(C_6H_{14}\)
b
\(V_{O_2}=0,475.22,4=10,64\left(l\right)\)
c
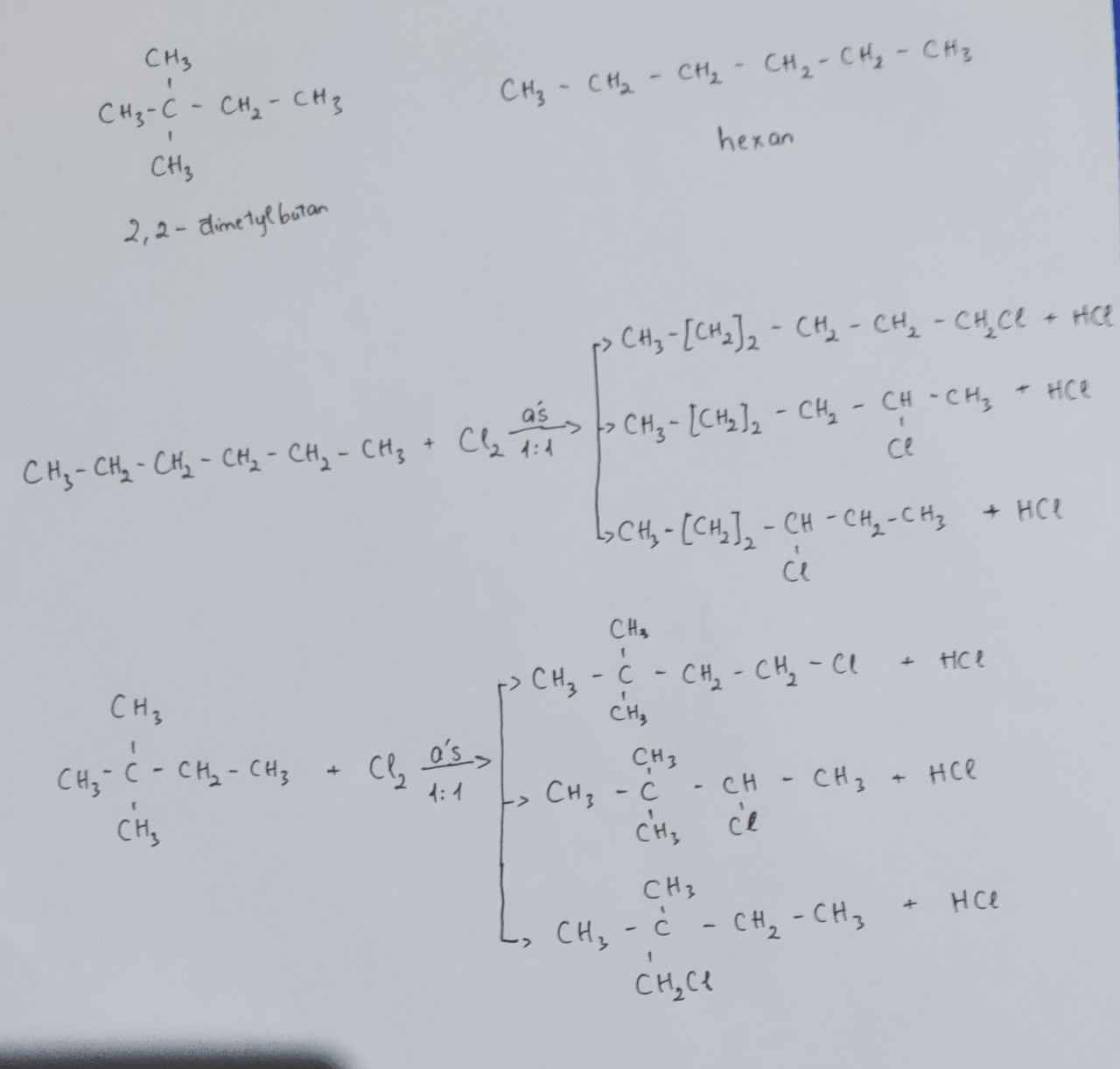
Đúng 3
Bình luận (1)
Hỗn hợp khí A gồm metan và hidrocacbon. Đốt cháy hoàn toàn 1,0 lít A cần dùng vừa đủ 2,6 lít khí O2 thu được CO2 và hơi nước. Dẫn toàn bộ sản phẩm cháy lội từ từ vào dung dịch H2SO4 đặc dư thấy có 1,6 lít khí KHÔNG bị hấp thụ. Xác định CTPT của hiddrocacbon và tính phần trăm thể tích của CH4 trong hỗn hợp A. Biết rằng các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất.
Đọc tiếp
Hỗn hợp khí A gồm metan và hidrocacbon. Đốt cháy hoàn toàn 1,0 lít A cần dùng vừa đủ 2,6 lít khí O2 thu được CO2 và hơi nước. Dẫn toàn bộ sản phẩm cháy lội từ từ vào dung dịch H2SO4 đặc dư thấy có 1,6 lít khí KHÔNG bị hấp thụ. Xác định CTPT của hiddrocacbon và tính phần trăm thể tích của CH4 trong hỗn hợp A. Biết rằng các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất.
Đốt cháy hoàn toàn 1,64 gam hỗn hợp các hidrocacbon trong vừa đủ V lít O2 (đktc) thu được m gam CO2 và 1,8 gam H2O. Xác định giá trị của m và V
Ta có: \(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\Rightarrow n_H=0,1.2=0,2\left(mol\right)\)
⇒ mC = 1,64 - mH = 1,24 (g) ⇒ nC = 0,12 (mol) = nCO2
⇒ mCO2 = 0,12.44 = 5,28 (g)
BTNT O, có: 2nO2 = 2nCO2 + nH2O ⇒ nO2 = 0,17 (mol)
⇒ VO2 = 0,17.22,4 = 3,808 (l)
Đúng 2
Bình luận (0)
Cho 5, 6 lit hỗn hợp X gồm một anken và một ankan đi qua dung dịch brom thấy có 16 g brom tham gia phản ứng. Nếu đốt cháy hoàn toàn 22,4 lit X thu được 88 gam CO2 1. Xác định công thức phân tử của hai hidrocacbon. 2. Tính thể tích O2 cần để đốt cháy hỗn hợp X trên.Các khí đo ở (đktc).
1)
\(\left\{{}\begin{matrix}C_nH_{2n+2}:a\left(mol\right)\\C_mH_{2m}:b\left(mol\right)\end{matrix}\right.\)\(\left(n\ge1;m\ge2\right)\)
=> \(a+b=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: CmH2m + Br2 --> CmH2mBr2
=> b = \(\dfrac{16}{160}=0,1\left(mol\right)\)
=> a = 0,15 (mol)
22,4l X chứa \(\left\{{}\begin{matrix}C_nH_{2n+2}:4a\left(mol\right)\\C_mH_{2m}:4b\left(mol\right)\end{matrix}\right.\)
Bảo toàn C: 4an + 4bm = \(\dfrac{88}{44}=2\)
=> 0,6n + 0,4.m = 2
Có n \(\ge1\) => m \(\le3,5\), mà \(m\ge2\)
=> \(\left[{}\begin{matrix}m=2=>n=2\left(TM\right)\\m=3=>n=\dfrac{4}{3}\left(L\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_2H_6:0,15\left(mol\right)\\C_2H_4:0,1\left(mol\right)\end{matrix}\right.\)
2)
PTHH: 2C2H6 + 7O2 --to--> 4CO2 + 6H2O
______0,15->0,525
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,1--->0,3
=> VO2 = (0,525 + 0,3).22,4 = 18,48(l)
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn 5,1 gam hỗn hợp x gồm 2 hidrocacbon đồng phân của nhau cần vừa đủ 11,76 lít o2 (đktc)
a, xác định công thức phân tử của x?
b, biết rằng x là hidrocacbon mạch nhánh và x + AgNO3/NH3 tạo kết tủa xác định công thức cấu tạo của các chất trong x và tên thay thế?
Đốt cháy hoàn toàn 6 gam một hidrocacbon bằng 15,68 lít khí O2,thu đc 8,96 lít khí CO (các khí đo ở đktc).CTPT của hiđrocacbon là A, C5H10 B, C4H12 C, C3H4 D, C4H8
\(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{15,68}{22,4}=0,7\left(mol\right)\)
BTNT O, có: 2nO2 = 2nCO2 + nH2O ⇒ nH2O = 0,6 (mol)
⇒ nH2O > nCO2 → ankan.
Có: nankan = 0,6 - 0,4 = 0,2 (mol)
Gọi CTPT cần tìm là CnH2n+2.
\(\Rightarrow n=\dfrac{n_{CO_2}}{n_{ankan}}=\dfrac{0,4}{0,2}=2\)
→ C2H6.
Đúng 2
Bình luận (0)
đốt cháy hoàn toàn 4,48 lít một ankan X thì cần vừa đủ 15,68 lít O2 (đkc). Tìm ctpt
\(n_{ankan}=\dfrac{4,48}{22,4}=0,2\left(mol\right);n_{O_2}=\dfrac{15,68}{22,4}=0,7\left(mol\right)\)
Đặt CTTQ của ankan là CnH2n+2
PTHH: \(2C_nH_{2n+2}+\left(3n+1\right)O_2\xrightarrow[]{t^o}2nCO_2+\left(2n+2\right)H_2O\)
Theo PTHH: \(\dfrac{n_{C_nH_{2n+2}}}{n_{O_2}}=\dfrac{2}{3n+1}=\dfrac{0,2}{0,7}=\dfrac{2}{7}\)
=> n = 2
Vậy ankan là C2H6
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 0,495 mol hỗn hợp X gồm metyl propionat, metyl axetat và 2 hidrocacbon mạch hở cần vừa đủ 1,905 mol O2, tạo ra 21,6 gam H2O. Nếu cho 0,5775 mol X vào dung dịch Br2 dư thì số mol Br2 phản ứng tối đa là A. 0,70 B. 0,60 C. 0,40 D. 1,2
Đọc tiếp
Đốt cháy hoàn toàn 0,495 mol hỗn hợp X gồm metyl propionat, metyl axetat và 2 hidrocacbon mạch hở cần vừa đủ 1,905 mol O2, tạo ra 21,6 gam H2O. Nếu cho 0,5775 mol X vào dung dịch Br2 dư thì số mol Br2 phản ứng tối đa là
A. 0,70
B. 0,60
C. 0,40
D. 1,2
Chọn đáp án A
X gồm C2H5COOCH3, CH3COOCH3 và CaHb.
Đặt neste = x mol ⇒ nhiđrocacbon = 0,495 – x mol.
nH2O = 1,2 mol ⇒ bảo toàn nguyên tố Oxi có:
nCO2 = (2x + 1,905 × 2 – 1,2)/2 = x + 1,305 mol.
tương quan đốt:
nCO2 – nH2O = (k – 1).nhỗn hợp
= k.nhỗn hợp - nhỗn hợp = ∑nπ - nhỗn hợp
(với k là tổng số liên kết π trong hỗn hợp).
Thay số liệu:
(x + 1,305) – 1,2 = (nBr2 + x) – 0,495
⇒ nBr2 = 0,6 mol.
⇒ ứng với 0,5775 mol X thì nBr2 phản ứng = 0,7 mol
Đúng 0
Bình luận (0)




