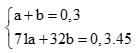Cho 6,72 lít (đktc) hỗn hợp X gồm O 2 , C l 2 có d X / H 2 = 22 , 5 tác dụng vừa đủ với m (g) hỗn hợp Y gồm Al và Zn thu được 31,9 gam hỗn hợp B gồm muối clorua và oxit của 2 kim loại. Tính m và %m mỗi chất trong Y?
NN
Những câu hỏi liên quan
Hỗn hợp X gồm hai khí O2 và Cl2 có tỷ khối so với không khí bằng 2.
a) Tính số mol O2 và Cl2 có trong 6,72 lít X (ở đktc).
b) Cho 6,72 lít hỗn hợp X nói trên phản ứng vừa đủ với m gam Mg. Tính khối lượng Mg
đã phản ứng.
Cho 16,6g hỗn hợp X gồm Al, Cu, Mg vào dung dịch H2SO4 loãng dư thu được 11,2 lít khí (đktc). Mặt khác nếu cho 8,3g hỗn hợp X trên vào dung dịch H2SO4 đặc nóng dư thu được 6,72 lít khí SO2 (đktc). Tính %m mỗi kim loại trong X
Đốt cháy một hỗn hợp X gồm 2 hiđrocacbon A (CnH2n+2) và B (CmH2m) thu được 15,68lít CO2 (đktc) và 14,4 gam H2O. Biết X chiếm thể tích là 6,72 lít ở đktc. Xác định thành phần % thể tích của hỗn hợp X, xác định CTPT của A, B.
Cho 11,1 gam hỗn hợp X gồm kim loại M và Al có tỉ lệ mol tương ứng 3:2 vào dung dịch HCl dư, sinh ra 6,72 lít H2 ở đktc. Xác định kim loại M.
gọi số mol M là X số mol Al là Y ta có X/Y=3/2
X=3/2 Y (1)
mà X * klrM + Y * 27 = 11,1 (2) thế (1) và (2) ta rút hệ Y = 11,1/3/2*klrM + 27 (3)
phương trình
2M + 2nHCl --> 2MCln + nH2
X n/2 X
2Al + HCl --> 2AlCl3 + 3H2
Y 3/2Y
theo đề bài ta có n/2X + 3/2 Y = 0,3(4) (mol hidro)
thay (1) vào (4) ta rút Y = 0,3/3/2 +3n/4 (5)
từ (3) và (5) ta có bảng nghiệm thế hóa trị ta có nghiệm thỏa mản n bằng 2 klr M = 56 vậy M là Fe
Đúng 0
Bình luận (0)
dẫn hỗn hợp ( X) gồm 6,72 lít ( đktc) khí etilen và metan đi qua bình đựng dung dịch Brom thấy khối lượng bình tăng lên 5,6 gam . Tính thể tích mỗi chất khí có trong hỗn hợp ( X)
( cho nguyên tử khối Br= 80, H= 1, C=12, O=16)
giải giúp mình với
mtăng = mC2H4
=> \(n_{C_2H_4}=\dfrac{5,6}{28}=0,2\left(mol\right)\)
=> VC2H4 = 0,2.22,4 = 4,48 (l)
=> VCH4 = 6,72 - 4,48 = 2,24 (l)
Đúng 3
Bình luận (0)
Cho 6,72 lít (đktc) hỗn hợp X gồm O2, Cl2 có dX/H2=22,5 tác dụng vừa đủ với m (g) hỗn hợp Y gồm Al và Zn thu được 31,9 gam hỗn hợp B gồm muối clorua và oxit của 2 kim loại. Tính m và %m mỗi chất trong Y?
Tham khảo:
Gọi số mol Cl2 là a, số mol O2 là b. Theo bài ra ta có hệ PT:
Giải hệ tìm được a = 0,1; b = 0,2 .
Gọi nAl = x, nZn=y (mol)
Sử dụng định luật bảo toàn electron: 3x + 2y = 0,2.4 + 0,1.2 = 1 (1)
Áp dụng bảo toàn khối lượng:
m = 31,9 - 45.0,3 = 18,4 gam nên 27x + 65y = 18,4 (2)
Giải hệ được: x = 0,2 và y = 0,2 → %mAl = 29,35%; %mZn= 70,65%
Đúng 0
Bình luận (0)
Hỗn hợp khí X gồm N2 va O2 . Ở đktc 6,72 lít khí X có khối lượng 8,8 gam.
a: Tính phần trăm thể tích các khí trong hỗn hợp X.
b: Tính thể tích H2 ( dktc) có thể tích bằng thể tích của 1,1 gam hỗn hợp khí X.
Xem thêm câu trả lời
Hỗn hợp X gồm Fe và kim loại M hóa trị 3. Chia 38,6 gam X thành 2 phần bằng nhau. Phần 1 cho tan hoàn toàn trong dung dịch HNO3 loãng dư thu được 6,72 lít hỗn hợp khí Y gồm NO, N2O, d(Y/H2) 17,8. Phần 2 cho vào dung dịch kiềm sau một thời gian thấy lượng H2 thoát ra vượt quá 6,72 lít. Tính % khối lượng kim loại M (khí đo ở đktc) A. 58,03% B. 41,97% C. 56,12% D. 43,08%
Đọc tiếp
Hỗn hợp X gồm Fe và kim loại M hóa trị 3. Chia 38,6 gam X thành 2 phần bằng nhau. Phần 1 cho tan hoàn toàn trong dung dịch HNO3 loãng dư thu được 6,72 lít hỗn hợp khí Y gồm NO, N2O, d(Y/H2) = 17,8. Phần 2 cho vào dung dịch kiềm sau một thời gian thấy lượng H2 thoát ra vượt quá 6,72 lít. Tính % khối lượng kim loại M (khí đo ở đktc)
A. 58,03%
B. 41,97%
C. 56,12%
D. 43,08%
Thể tích của hỗn hợp khí X gồm: 0,2 mol CO 2 ; 0,5 mol H 2 và 0,3 mol 0 2 ở 0 0 C, 1 atm là: A. 22,4 lít. B. 3,36 lít. C. 6,72 lít. D. 15,68 lít.
nhh = 0,2 + 0,5 + 0,3 = 1 (mol)
0oC, 1atm là đktc => Vhh = 1 .22,4 = 22,4 (l)
=>A
Đúng 1
Bình luận (0)
Dùng 13,44 lít khí hidro (đktc) khử hoàn toàn 39,2 gam hỗn hợp X gồm đồng oxit và một oxit sắt thu được hỗn hợp B gồm 2 kim loại.Cho B vào dung dịch HCl dư thu được 6,72 lít H2 (đktc),dung dịch C và chất rắn không tan D.Tính thành phần phần trăm theo khối lượng của mỗi chất trong X