Đốt cháy hoàn toàn 1 mol khí hidrocacbon, sinh ra 2 mol khí CO2 và 2 mol nước.Vậy hidrocacbon đó là
H24
Những câu hỏi liên quan
Bài 1: Đốt cháy hoàn toàn một hidrocacbon X thu được 0,1 mol CO2 và 0,15 mol H2O. Tìm tên gọi của X
Bài 2: Khi đốt cháy hoàn toàn 4,48 lít hỗn hợp khí gồm CH4, C2H6, C3H8 (đktc) thu được V lít khí CO2(đktc) và 18g H2O. Tìm V
Bài 1 :
\(n_{H_2O}>n_{CO_2}\Rightarrow X:ankan\)
\(Đặt:CTHH:C_nH_{2n+2}\)
\(\dfrac{n}{2n+2}=\dfrac{0.1}{0.3}\Rightarrow n=2\)
\(Vậy:Xlà:C_2H_6\left(etan\right)\)
Đúng 1
Bình luận (0)
Bài 1
\(n_{CO_2} < n_{H_2O} \to\) X là ankan (CnH2n+2)
\(n_X = n_{H_2O} - n_{CO_2} = 0,15 - 0,1 = 0,05(mol)\)
Suy ra: \(n = \dfrac{n_{CO_2}}{n_X} = \dfrac{0,1}{0,05} = 2\)
Vậy X là C2H6(etan)
Bài 2 :
Hỗn hợp có dạng CnH2n+2
\(n_{hỗn\ hợp} = \dfrac{4,48}{22,4} = 0,2(mol)\\ n_{H_2O} = \dfrac{18}{18} = 1(mol)\\ \Rightarrow n + 2 = \dfrac{2n_{H_2O}}{n_{hh}} = 5\\ Suy\ ra\ n = 3\)
\(\Rightarrow n_{CO_2} = 3n_{hh} = 0,2.3 = 0,6(mol)\\ \Rightarrow V = 0,6.22,4 = 13,44(lít)\)
Đúng 1
Bình luận (0)
Bài 2 :
\(n_{H_2O}=\dfrac{18}{18}=1\left(mol\right)\)
\(n_{ankan}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(n_{CO_2}=n_{H_2O}-n_{ankan}=1-0.2=0.8\left(mol\right)\)
\(V_{CO_2}=0.8\cdot22.4=17.92\left(l\right)\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn V lít (đktc) hỗn hợp khí X gồm axetilen, etilen và hidrocacbon Y, thu được số mol CO2 đúng bằng số mol H2O. Nếu dẫn V lít (đktc) hỗn hợp khí X như trên qua lượng dư dung dịch Br2 thấy khối lượng bình đựng tăng 0,82 gam. Khí thoát ra khỏi bình đem đốt cháy hoàn toàn thì thu được 1,32 gam CO2 và 0,72 gam H2O. Công thức phân tử của hidrocacbon Y và giá trị của V là: A. C3H4 và 0,336 B. C3H8 và 0,672. C. C3H8 và 0,896. D. C4H10 và 0,448.
Đọc tiếp
Đốt cháy hoàn toàn V lít (đktc) hỗn hợp khí X gồm axetilen, etilen và hidrocacbon Y, thu được số mol CO2 đúng bằng số mol H2O. Nếu dẫn V lít (đktc) hỗn hợp khí X như trên qua lượng dư dung dịch Br2 thấy khối lượng bình đựng tăng 0,82 gam. Khí thoát ra khỏi bình đem đốt cháy hoàn toàn thì thu được 1,32 gam CO2 và 0,72 gam H2O. Công thức phân tử của hidrocacbon Y và giá trị của V là:
A. C3H4 và 0,336
B. C3H8 và 0,672.
C. C3H8 và 0,896.
D. C4H10 và 0,448.
Đáp án C
Khí thoát ra khỏi bình là Y ; nCO2 = 0,03 ; nH2O= 0,04
→ Y là ankan → nY = 0,04 - 0,03 = 0,01 → Y là C3H8
Đốt cháy X thu được nCO2 = nH2O
→ nC2H2= nC3H8 = 0,01 mol
→ nC2H4 = ( 0,82 - 0,01 × 26 ) : 28 = 0,02 mol
→ nX = 0,01 + 0,02 + 0,01 = 0,04 → VX = 0,896 (l)
Đúng 0
Bình luận (0)
đốt cháy hoàn toàn một hidrocacbon thu được số mol H20 bằng số mol CO2 .Công thức phân tử hidrocacbon đó là :
\(C_nH_{2n}\left(n>=2\right)\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn một hidrocacbon X thu được 0,11 mol CO2 và 0,132 mol H2O. Khi X tác dụng với khí clo (theo tỉ lệ số mol 1 : 1) thu được một sản phẩm hữu cơ duy nhất. Tên gọi của X là:
A. 2-Metylbutan
B. etan
C. 2,2-Đimetylpropan
D. 2-Metylpropan
Đáp án C

Dựa vào CTCT ta thấy chỉ có 2,2 – đimetylpropan khi tác dụng với Cl2 (tỉ lệ mol 1 : 1) thu được sản phẩm hữu cơ duy nhất.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp X gồm hidrocacbon Y và khí CO thu được số mol
C
O
2
bằng số mol nước. Y là: A.
C
3
H
8
B.
C
3
H
6
C.
C
3
H
4
D.
C
4
H...
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp X gồm hidrocacbon Y và khí CO thu được số mol C O 2 bằng số mol nước. Y là:
A. C 3 H 8
B. C 3 H 6
C. C 3 H 4
D. C 4 H 8
Gọi số mol của C x H y và CO lần lượt là a và b.
Theo định luật bảo toàn nguyên tố ta có:
n C = a . x + b → n C O 2 = a . x + b n H = a . y → n H 2 O = a . y 2
Đốt cháy C x H y và CO thu được số mol C O 2 bằng số mol H 2 O
⇒ a . x + b = a . y 2 ⇒ a . x < a . y 2 ⇒ x < y 2
Vậy khi đốt cháy hiđrocacbon C x H y có n C O 2 < n H 2 O
Vậy hợp chất hidrocacbon là ankan, suy ra CTTQ là C n H 2 n + 2 .
⇒ Chọn A.
Đúng 0
Bình luận (0)
Hợp chất hữu cơ là chất khí ít tan trong nước, làm mất màu dung dịch brom, đốt cháy hoàn toàn 1 mol khí này sinh ra 2 mol khí CO2 và 1 mol nước. Hợp chất đó là
A.CH4
B.C2H4
C.C2H2
D.C6H6
\(n_{CO_2}:n_{H_2O}=2:1\\ \Rightarrow n_C:n_H=2:2=1:1\\ \Rightarrow HCHC:n_C=n_H\\ \Rightarrow Chọn.C\left(Vì:C_6H_6.không.làm.mất.màu.dd.Br_2\right)\\ \)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn một hidrocacbon X thu được 0,11 mol CO2 và 0,132 mol H2O. Khi X tác dụng với khí Clo (theo tỷ lệ 1:1) thu được 1 sản phẩm hữu cơ duy nhất. Tên gọi của X là A. etan B. 2,2-đimetylpropan C. 2-metylbutan D. 2-metylpropan
Đọc tiếp
Đốt cháy hoàn toàn một hidrocacbon X thu được 0,11 mol CO2 và 0,132 mol H2O. Khi X tác dụng với khí Clo (theo tỷ lệ 1:1) thu được 1 sản phẩm hữu cơ duy nhất. Tên gọi của X là
A. etan
B. 2,2-đimetylpropan
C. 2-metylbutan
D. 2-metylpropan
Đốt cháy hoàn toàn 0,3 mol hỗn hợp X gồm 2 hidrocacbon mạch hở có số mol bằng nhau thu được 0,75 mol CO2 và 0,9 mol H2O. Số cặp chất thỏa mãn X là: A. 3 B. 5 C. 6 D. 4
Đọc tiếp
Đốt cháy hoàn toàn 0,3 mol hỗn hợp X gồm 2 hidrocacbon mạch hở có số mol bằng nhau thu được 0,75 mol CO2 và 0,9 mol H2O. Số cặp chất thỏa mãn X là:
A. 3
B. 5
C. 6
D. 4
Đáp án C
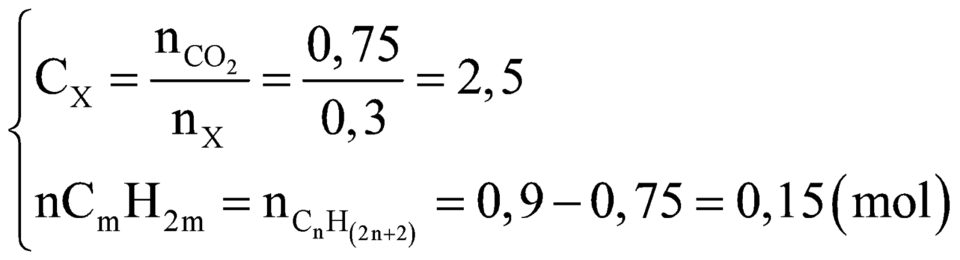
Suy ra X có 6 cặp chất:
C2H6 và C3H6
C3H8 và C2H4
CH4 và CH2 = CH-CH2 -CH3
CH4 và CH3 -CH = CH-CH3 cis
CH4 và CH3CH = CHCH3 trans
CH4 và CH2 =C(CH3)-CH3
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 0,3 mol hỗn hợp X gồm 2 hidrocacbon mạch hở có số mol bằng nhau thu được 0,75 mol CO2 và 0,9 mol H2O. Số cặp chất thỏa mãn X là?
A. 3
B. 5
C. 6
D. 4