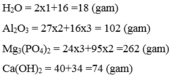tính khối lượng của 2mol O ,2 mol O2,0.25mol H2O
KJ
Những câu hỏi liên quan
Tính khối lượng của H2 và khối lượng NaOH tạo thành khi cho 2mol Na tác dụng với H2O,biết phương trình phản ứng
Na+H2O -> NaOH + H2
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(\dfrac{2}{2}\) = \(\dfrac{2}{2}\) ( mol )
2 2 2 2 ( mol )
( Cả 2 chất đều không dư )
\(m_{H_2}=1.2=2g\)
\(m_{NaOH}=2.40=80g\)
Đúng 2
Bình luận (1)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
2 2 1 ( mol )
\(m_{H_2}=1.2=2g\)
\(m_{NaOH}=2.40=80g\)
tính khối lượng hợp chat X có chứa 2mol khí H2 và 2,5 Mol khí CH4
\(m_{X}=m_{H_2}+m_{CH_4}=2.2+2,5.16=44(g)\)
Đúng 2
Bình luận (1)
Một dung dịch chứa a mol
Na
+
, 2mol
Ca
2
+
, 4 mol
Cl
-
, 2 mol
HCO
3
-
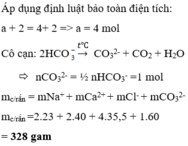
. Cô cạn dung dịch này ta được lượng chất rắn có khối lượng là A. 390 gam. B. 436 gam. C. 328 gam D. 374 gam.
Đọc tiếp
Một dung dịch chứa a mol Na + , 2mol Ca 2 + , 4 mol Cl - , 2 mol HCO 3 - . Cô cạn dung dịch này ta được lượng chất rắn có khối lượng là
A. 390 gam.
B. 436 gam.
C. 328 gam
D. 374 gam.
1. 2mol mol nguyên tử sắt (fe) là lượng có chứa bao nhiêu nguyên tử sắt 2. 3 mol phân tử nước (H2O) là lượng có chứa bao nhiêu phân tử nước 3. 3,011.10²³ nguyên tử sắt (Fe) có chứa mấy mol? 4. 18,066.10²³ nguyên tử K có chứa mấy mol?
1)
Số nguyên tử Fe = 2.6,022.1023 = 12,044.1023 (nguyên tử)
2)
Số phân tử H2O = 3.6,022.1023 = 18,066.1023 (nguyên tử)
3)
\(n_{Fe}=\dfrac{3,011.10^{23}}{6,022.10^{23}}=0,5\left(mol\right)\)
4)
\(n_K=\dfrac{18,066.10^{23}}{6,022.10^{23}}=3\left(mol\right)\)
Đúng 1
Bình luận (0)
Bài 1: Tính khối lượng của 1 mol Cl2, CH4 , CO2 , K2O , Fe2O3, CuSO4, NaOH, Fe(NO3)2 , Fe(OH)2 , K NO3, Tính khối lượng của 0,1 mol CaCO3 ; 0,5 mol H2O ; 0,15 mol CuO.
\(m_{Cl_2}=1.71=71\left(g\right)\)
\(m_{CH_4}=1.16=16\left(g\right)\)
\(m_{CO_2}=1.44=44\left(g\right)\)
\(m_{K_2O}=1.94=94\left(g\right)\)
\(m_{Fe_2O_3}=1.160=160\left(g\right)\)
\(m_{CuSO_4}=1.160=160\left(g\right)\)
\(m_{NaOH}=1.40=40\left(g\right)\)
\(m_{Fe\left(NO_3\right)_2}=1.242=242\left(g\right)\)
\(m_{Fe\left(OH\right)_2}=1.90=90\left(g\right)\)
\(m_{KNO_3}=1.101=101\left(g\right)\)
\(m_{CaCO_3}=0,1.100=10\left(g\right)\)
\(m_{H_2O}=0,5.18=9\left(g\right)\)
\(m_{CuO}=0,15.80=12\left(g\right)\)
Đúng 0
Bình luận (1)
a/ Tính khối lượng và thể tích ở đktc của hỗn hợp khí gồm: 1,2.1023 phân tử CH4, 0,25 mol O2, 22 gam khí CO2.
b/ Tính khối lượng của N phân tử các chất sau: H2O, CuSO4, C6H12O6, Ca(OH)2.
c/ Tính số mol nguyên tử H, P, O có trong 19,6 gam axit photphoric (H3PO4).
Tính khối lượng muối thu được trong các trường hợp sau: a. 2mol CO2 + 1mol NaOH b. 1mol CO2 + 2mol NaOH c. 2mol CO2 + 3mol NaOH
\(T=\dfrac{n_{NaOH}}{n_{CO_2}}\)
a.
\(T=\dfrac{1}{2}=0.5< 1\)
\(\Rightarrow\) Tạo muối NaHCO3
\(NaOH+CO_2\rightarrow NaHCO_3\)
\(1..................................1\)
\(m_{NaHCO_3}=1\cdot84=84\left(g\right)\)
b.
\(T=\dfrac{2}{1}=2\)
=> Tạo muối Na2CO3
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
\(2.................................1\)
\(m_{Na_2CO_3}=1\cdot106=106\left(g\right)\)
c.
\(T=\dfrac{3}{2}=1.5\)
=> Tạo 2 muối
\(n_{Na_2CO_3}=a\left(mol\right),n_{NaHCO_3}=b\left(mol\right)\)
\(n_{NaOH}=2a+b=3\left(mol\right)\)
\(n_{CO_2}=a+b=2\left(mol\right)\)
\(\Rightarrow a=b=1\)
\(m_{Muối}=1\cdot84+1\cdot106=190\left(g\right)\)
Đúng 2
Bình luận (0)
Cho 14,1gam hỗn hợp bột (Mg,Al) tan hoàn toàn trong 2mol HNO3, thu được 6,72lít
hỗn hợp khí (đktc) N2O, NO tỉ lệ mol 1 : 2 và dung dịch X
a) Tính khối lượng nhôm (Al) trong hỗ hợp kim loại
b) Lấy toàn bộ dung dịch X tác dụng với 1,7 mol NaOH . Tính số mol kết tủa thu được
a) \(n\uparrow=\dfrac{6,72}{22,4}=0,3mol\)\(\Rightarrow n_{N_2O}+n_{NO}=0,3\)
Mà \(\dfrac{n_{N_2O}}{n_{NO}}=\dfrac{1}{2}\)
\(\Rightarrow\left\{{}\begin{matrix}N_2O:0,1mol\\NO:0,2mol\end{matrix}\right.\)
Ta có: \(\left\{{}\begin{matrix}2n_{Mg}+3n_{Al}=8n_{N_2O}+3n_{NO}\left(BTe\right)\\24n_{Mg}+27n_{Al}=14,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,25mol\\n_{Al}=0,3mol\end{matrix}\right.\) \(\Rightarrow m_{Al}=0,3\cdot27=8,1\left(g\right)\)
b) Dung dịch X thu đc: \(\left\{{}\begin{matrix}Mg^{2+}\\Al^{3+}\\NO^-_3\end{matrix}\right.\) \(\underrightarrow{+1,7molNaOH}\)\(\downarrow\left\{{}\begin{matrix}Mg\left(OH\right)_2\\Al\left(OH\right)_3\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Tính khối lượng mol của các chất sau: H 2 O , A l 2 O 3 , M g 3 P O 4 2 , C a ( O H ) 2 .