Khí A chứa 80% C và 20% H. 1 lít khí A ( ở đktc) nặng 1,34 g . Xác định công thức hóa học của A
TT
Những câu hỏi liên quan
a. Khí A chứa 80% cacbon và 20% hiđro; 1 lít khí A (ở đkt) nặng 1,34 gam. Xác định công thức hóa học của A?b. Đốt hợp chất Y sinh ra khí cacbonic, hơi nước và khí Nitơ. Cho biết nguyên tố nào bắt buộc có trong thành phần của Y? Nguyên tố nào có thể có, có thể không trong thành phần của Y? Giải thích?c. Cho luồng khí hiđro đi qua ống thủy tinh chứa 10 gam bột đồng (II) oxit ở nhiệt độ cao. Sau phản ứng thu được 8,4 gam chất rắn. Nêu hiện tượng phản ứng. Tính thể tích khí hiđro tham gia phản ứng ở...
Đọc tiếp
a. Khí A chứa 80% cacbon và 20% hiđro; 1 lít khí A (ở đkt) nặng 1,34 gam. Xác định công thức hóa học của A?
b. Đốt hợp chất Y sinh ra khí cacbonic, hơi nước và khí Nitơ. Cho biết nguyên tố nào bắt buộc có trong thành phần của Y? Nguyên tố nào có thể có, có thể không trong thành phần của Y? Giải thích?
c. Cho luồng khí hiđro đi qua ống thủy tinh chứa 10 gam bột đồng (II) oxit ở nhiệt độ cao. Sau phản ứng thu được 8,4 gam chất rắn. Nêu hiện tượng phản ứng. Tính thể tích khí hiđro tham gia phản ứng ở đkt?
a) CTHH: CxHy
\(M_A=\dfrac{1,34}{\dfrac{1}{22,4}}=30\left(g/mol\right)\)
\(m_C=\dfrac{30.80}{100}=24\left(g\right)\Rightarrow x=\dfrac{24}{12}=2\)
\(m_H=\dfrac{30.20}{100}=6\left(g\right)\Rightarrow y=\dfrac{6}{1}=6\)
=> CTHH: C2H6
b)
Y + O2 --to--> CO2 + H2O + N2
Do đốt cháy Y được sản phẩm chứa các nguyên tố C, H, O, N
=> Y bắt buộc phải chứa C, H, N; có thể có O
c) Hiện tượng: Chất rắn màu đen chuyển dần sang màu đỏ
\(n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)\)
Gọi số mol CuO pư là a (mol)
PTHH: CuO + H2 --to--> Cu + H2O
a--->a--------->a
=> 80(0,125 - a) + 64a = 8,4
=> a = 0,1 (mol)
=> VH2(đktc) = 0,1.22,4 = 2,24 (l)
Đúng 0
Bình luận (0)
khí A chứa 80% C và 20% H . 1 lít khí A ( ở đktc) nặng 1,34 g . xác định công thức hóa học của A
Gọi CTHH của A là CxHy
PTK của A =\(1,34:\dfrac{1}{22,4}=30\left(dvC\right)\)
x=\(\dfrac{30.80\%}{12}=2\)
y=\(\dfrac{30-12.2}{1}=6\)
Vậy CTHH của A là C2H6
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn mg hỗn hơp A cần vừa đủ 42 lít không khí. Sau phản ứng thu được 9gam nước và 44,8 lít hỗn hợp B gồm CO2 và N2. dB/H2=15. (Các khí đo ở đktc, không khí có 20%O2 và 80%N2 theo thể tích). Tính m và xác định công thức hóa học của A
Xác định công thức phân tử của các chất A, B, C, biết thành phần % khối lượng như sau:
1. Chất A chứa 85,71% Cacbon và 14,29% Hidro; 1 lit khí A ở đktc nặng 1,25gam.
2. Chất B chứa 80% cacbon và 20% là oxi
3. Chất C chứa 40% Cacbon, 6,67% Hidro và còn lại là Oxi, biết C có chứa 2 nguyên tử oxi
1) \(n_A=\dfrac{1}{22,4}=\dfrac{5}{112}\left(mol\right)=>M_A=\dfrac{1,25}{\dfrac{5}{112}}=28\left(g/mol\right)\)
\(m_C=\dfrac{85,71.28}{100}=24\left(g\right)=>n_C=\dfrac{24}{12}=2\left(mol\right)\)
\(m_H=\dfrac{14,29.28}{100}=4\left(g\right)=>n_H=\dfrac{4}{1}=4\left(mol\right)\)
=> CTPT: C2H4
2) Mình nghĩ phải là 80% C và 20% H :v
\(\dfrac{m_C}{m_H}=\dfrac{80\%}{20\%}=4=>\dfrac{12n_C}{n_H}=4=>\dfrac{n_C}{n_H}=\dfrac{1}{3}\)
=> CTPT: (CH3)n hay CnH3n
Xét độ bất bão hòa \(k=\dfrac{2.n+2-3.n}{2}=\dfrac{2-n}{2}\)
=> n = 2 (do k là số nguyên không âm)
=> CTPT: C2H6
3) %O = 100% - 40% - 6,67% = 53,33%
\(M_C=\dfrac{16.2.100}{53,33}=60\left(g/mol\right)\)
\(m_C=\dfrac{60.40}{100}=24\left(g\right)=>n_C=\dfrac{24}{12}=2\left(mol\right)\)
\(m_H=\dfrac{6,67.60}{100}=4\left(g\right)=>n_H=\dfrac{4}{1}=4\left(mol\right)\)
=> CTPT: C2H4O2
Đúng 0
Bình luận (0)
Một hợp chất A tạo bởi nguyên tố R (hóa trị I) và O. Biết 5,6 lít khí A (đktc) nặng 11g . Xác định công thức hóa học của hợp chất A
Giả sử CTHH của A là: R2O.
Ta có: \(n_{R_2O}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(\Rightarrow M_{R_2O}=\dfrac{11}{0,25}=44\left(g/mol\right)\)
\(\Rightarrow2M_R+16=44\)
\(\Rightarrow M_R=14\left(g/mol\right)\)
⇒ R là Nitơ.
Vậy: CTHH của A là N2O.
Bạn tham khảo nhé!
Đúng 3
Bình luận (0)
chỉ mình với
Hợp chất A ở thể khí có công thức là RO 2 . Biết rằng khối lượng của 11,2 lít A ở đktc là 32g. Xác định tên và kí hiệu hóa học của R. Viết công thức hóa học của hợp chất khí .
\(n_A=\dfrac{11,2}{22,4}=0,5\left(mol\right)=>M_A=\dfrac{32}{0,5}=64\left(g/mol\right)\)
=> MR + 2.16 = 64
=> MR = 32(g/mol)
=> R là S (lưu huỳnh)
CTHH: SO2
Đúng 1
Bình luận (0)
A là khí không màu mùi hắc, rất độc và nặng hơn không khíHãy xác định công thức của hợp chất khí A, biết rằng+ A là oxit của lưu huỳnh chứa 50% oxi + 1 gam khí A chiếm thể tích 0,35 lít ở đktc A. SO B.
SO
3
C.
SO
2
D.
NO
2
Đọc tiếp
A là khí không màu mùi hắc, rất độc và nặng hơn không khí
Hãy xác định công thức của hợp chất khí A, biết rằng
+ A là oxit của lưu huỳnh chứa 50% oxi
+ 1 gam khí A chiếm thể tích 0,35 lít ở đktc
A. SO
B. SO 3
C. SO 2
D. NO 2
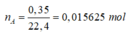
M A = m A n A = 1 0,015625 = 64 g / m o l
- Tìm số mol nguyên tử S, O trong phân tử A
Cứ 1 mol phân tử A có:
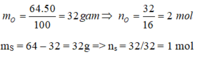
Suy ra trong 1 phân tử A có 1S và 2O, công thức của A là SO 2
Đáp án: C
Đúng 0
Bình luận (0)
Khí A nặng hơn khí Hiđro là 14 lần. thành phần theo khối lượng của khí A là 85,71% C và 14,29% H. Hãy xác định công thức hóa học của A
Xem chi tiết
MH2 = 2(g/mol) => MA = 14.2 = 28 (g/mol)
Gọi công thức hóa học của A là CxHy
%C trong A = \(\dfrac{12.x}{28}.100\) = 85,71 => x = 2
%H trong A = \(\dfrac{1.y}{28}.100\) = 14,29 => y = 4
Vậy CTHH của A là C2H4
Đúng 0
Bình luận (0)
Hợp chất khí A có thành phần các nguyên tố là: 80% C, 20% H. Biết tỉ khối của khí A so với H là 15 (dA/H2 = 15). Xác định công thức hóa học của khí A?
Giúp mình với ạ:<<





