Một oxit sắt có nhiều quặng hematit đỏ chứa 30% về khối lượng sắt.Tìm khối lượng mol của oxit sắt.
HM
Những câu hỏi liên quan
Hematit là một loại quặng chứa sắt (III) oxit. Trong một mẩu hematit có 5,6 (g) sắt. Khối lượng sắt III oxit có trong mẩu quặng đó là
nFe=0,1mol
2Fe2O3+6H2 -> 4Fe+6H2O ( đk nhiệt)
0,05 <- 0,1
mFe2O3=0,05.(56.2+16.3)=8g
Đúng 1
Bình luận (0)
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là A. 506,9 kg B. 515,8 kg C. 533,6 kg D. 490 kg
Đọc tiếp
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là
A. 506,9 kg
B. 515,8 kg
C. 533,6 kg
D. 490 kg
Đáp án B
Ta có: m(Fe2O3) = 7.103 (kg) → n(Fe2O3) = 4,375 mol → n(Fe trong gang) = 4,375. 2 = 8,75
→ m(Fe trong gang) = 490 → m(gang) = 490. 100 : 95 = 515,8 (kg)
Đúng 0
Bình luận (0)
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là A. 506,9 kg B. 515,8 kg C. 533,6 kg D. 490 kg
Đọc tiếp
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là
A. 506,9 kg
B. 515,8 kg
C. 533,6 kg
D. 490 kg
Đáp án B
Ta có: m(Fe2O3) = 7.103 (kg) → n(Fe2O3) = 4,375 mol → n(Fe trong gang) = 4,375. 2 = 8,75
→ m(Fe
trong gang) = 490 → m(gang) = 490. 100 : 95 = 515,8 (kg) Câu 86: Đáp án D
Gọi n(Fe) = a và n(C) = b → 56a + 12b = 99,2
BT e: 3a + 4b =2n(SO2) → n(SO2) = 1,5a + 2b
→ n(hh khí) = 1,5a + 2b + b = 1,5a + 3b = 2,925
→ a = 1,75 và b = 0,1 → % = 0,1. 12. 100% : 99,2 = 1,21%
Đúng 0
Bình luận (0)
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là A. 506,9 kg B. 515,8 kg C. 533,6 kg D. 490 kg
Đọc tiếp
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là
A. 506,9 kg
B. 515,8 kg
C. 533,6 kg
D. 490 kg
Đáp án A
Gọi n(Fe) = a và n(Cu) = b → 56x + 64y = 15,2
BT e: 3x + 2y = 3n(NO) = 0,6
→ x = 0,1 và y = 0,15 → m(Cu) = 9,6 → % = 63,16%
Đúng 0
Bình luận (0)
Hematit là một loại quặng chứa sắt (III) oxit. Trong một mẩu hematit có 5,6 (g) sắt. Khối lượng sắt III oxit có trong mẩu quặng đó là
(1 Point)
Biết : O = 16 ; Fe = 56
A.16 g
B.11,2 g
C.8 g
D.6 g
nFe = 5,6/56 = 0,1 (mol)
=> nFe2O3 = 0,1/2 = 0,05 (mol)
mFe2O3 = 0,05 . 160 = 8 (g)
=> C
Đúng 0
Bình luận (0)
A,N2O5+H2O---HNO3
B,Fe2O3+CO----Fe+CO2
C,KOH+H2SO4----K2SO4+H2O
D,Ca(OH)2+H3PO4----CA3(PO4)+H2O
E,Al+O2----Al2O3
Bài 2:quặng hematit có thành phần chính là sắt (III)oxit Fe2O3.Dùng 0,6kg khí hydro khử 18 kg quặng hematit thì thu được 11,2 kg sắt và 5,4kg nước
A.lập pthh của phản ứng
B.viết công thức về khối lượng của các chất trong phản ứng
C.tính khối lượng của sắt (III)oxit tham gia phản ứng
D.tính tỉ lệ phần trăm về khối lượng sắt (III) oxit chứa trong mẫu quặng
Đọc tiếp
A,N2O5+H2O--->HNO3
B,Fe2O3+CO---->Fe+CO2
C,KOH+H2SO4---->K2SO4+H2O
D,Ca(OH)2+H3PO4---->CA3(PO4)+H2O
E,Al+O2---->Al2O3
Bài 2:quặng hematit có thành phần chính là sắt (III)oxit Fe2O3.Dùng 0,6kg khí hydro khử 18 kg quặng hematit thì thu được 11,2 kg sắt và 5,4kg nước
A.lập pthh của phản ứng
B.viết công thức về khối lượng của các chất trong phản ứng
C.tính khối lượng của sắt (III)oxit tham gia phản ứng
D.tính tỉ lệ phần trăm về khối lượng sắt (III) oxit chứa trong mẫu quặng
https://i.imgur.com/GX8qvP7.jpg
A,N2O5+H2O--->2HNO3
B,Fe2O3+3CO---->2Fe+3CO2
C,2KOH+H2SO4---->K2SO4+2H2O
D3,Ca(OH)2+2H3PO4---->CA3(PO4)2+3H2O
E,4Al+3O2---->2Al2O3
Cho khí cacbon oxit ( CO ) tác dụng với quặng hematit có thành phần chính là sắt (III) oxit ( Fe2O3 ) tạo thành cacbon đioxit ( CO2 ) và kim loại sắt ( Fe ) theo phương trình hóa học sauCO + Fe2O3 à 2Fe + 3CO2a) Viết công thức về khối lượng của phản ứng xảy ra?b) Tính % khối lượng Fe2O3 có trong quặng hematit biết rằng khi cho 84 kg CO tác dụng hết với 300 kg quặng hematit thì sau phản ứng tạo thành 112 kg Fe và 132 kg CO2
Đọc tiếp
Cho khí cacbon oxit ( CO ) tác dụng với quặng hematit có thành phần chính là sắt (III) oxit ( Fe2O3 ) tạo thành cacbon đioxit ( CO2 ) và kim loại sắt ( Fe ) theo phương trình hóa học sau
CO + Fe2O3 à 2Fe + 3CO2
a) Viết công thức về khối lượng của phản ứng xảy ra?
b) Tính % khối lượng Fe2O3 có trong quặng hematit biết rằng khi cho 84 kg CO tác dụng hết với 300 kg quặng hematit thì sau phản ứng tạo thành 112 kg Fe và 132 kg CO2
Từ 400kg quặng hematit đỏ chứa 60% Fe2O3 về khối lượng) có thể luyện được m kg gang có hàm lượng sắt bằng 95%. Biết lượng sắt bị hao hụt trong sản xuất là 2%. Giá trị của m là: A. 116,2 B. 180,5 C. 155,1 D. 173,3
Đọc tiếp
Từ 400kg quặng hematit đỏ chứa 60% Fe2O3 về khối lượng) có thể luyện được m kg gang có hàm lượng sắt bằng 95%. Biết lượng sắt bị hao hụt trong sản xuất là 2%. Giá trị của m là:
A. 116,2
B. 180,5
C. 155,1
D. 173,3
Chọn đáp án D
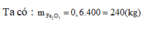
![]()

Khối lượng của gang là :
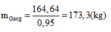
Đúng 0
Bình luận (0)
Giúp em với Làm Ơn !1.Một nguyên tố hoá trị II, Chiếm 80% khối lượng trong oxit của nó. Em hãy cho biết oxit trên thuộc loại oxit gì?Oxit axitOxit bazơKhông thuộc 1 trong hai loại oxit trên2.Khối lượng sắt có trong 1 tấn quặng chứa 70% sắt (III) oxit là560kg700kg245 kg490 kg3.Đốt cháy một đoạn dây sắt nặng 28 gam trong bình chứa 6,16 lít khi oxi ở đktc, Xác định khối lượng oxit tạo thành116 gam38,67 g31,9 gam63,8 gam
Đọc tiếp
Giúp em với Làm Ơn !
1.Một nguyên tố hoá trị II, Chiếm 80% khối lượng trong oxit của nó. Em hãy cho biết oxit trên thuộc loại oxit gì?
Oxit axit
Oxit bazơ
Không thuộc 1 trong hai loại oxit trên
2.Khối lượng sắt có trong 1 tấn quặng chứa 70% sắt (III) oxit là
560kg
700kg
245 kg
490 kg
3.Đốt cháy một đoạn dây sắt nặng 28 gam trong bình chứa 6,16 lít khi oxi ở đktc, Xác định khối lượng oxit tạo thành
116 gam
38,67 g
31,9 gam
63,8 gam
Câu 1: C
Câu 2: A
Câu 3: C
Đúng 0
Bình luận (0)





