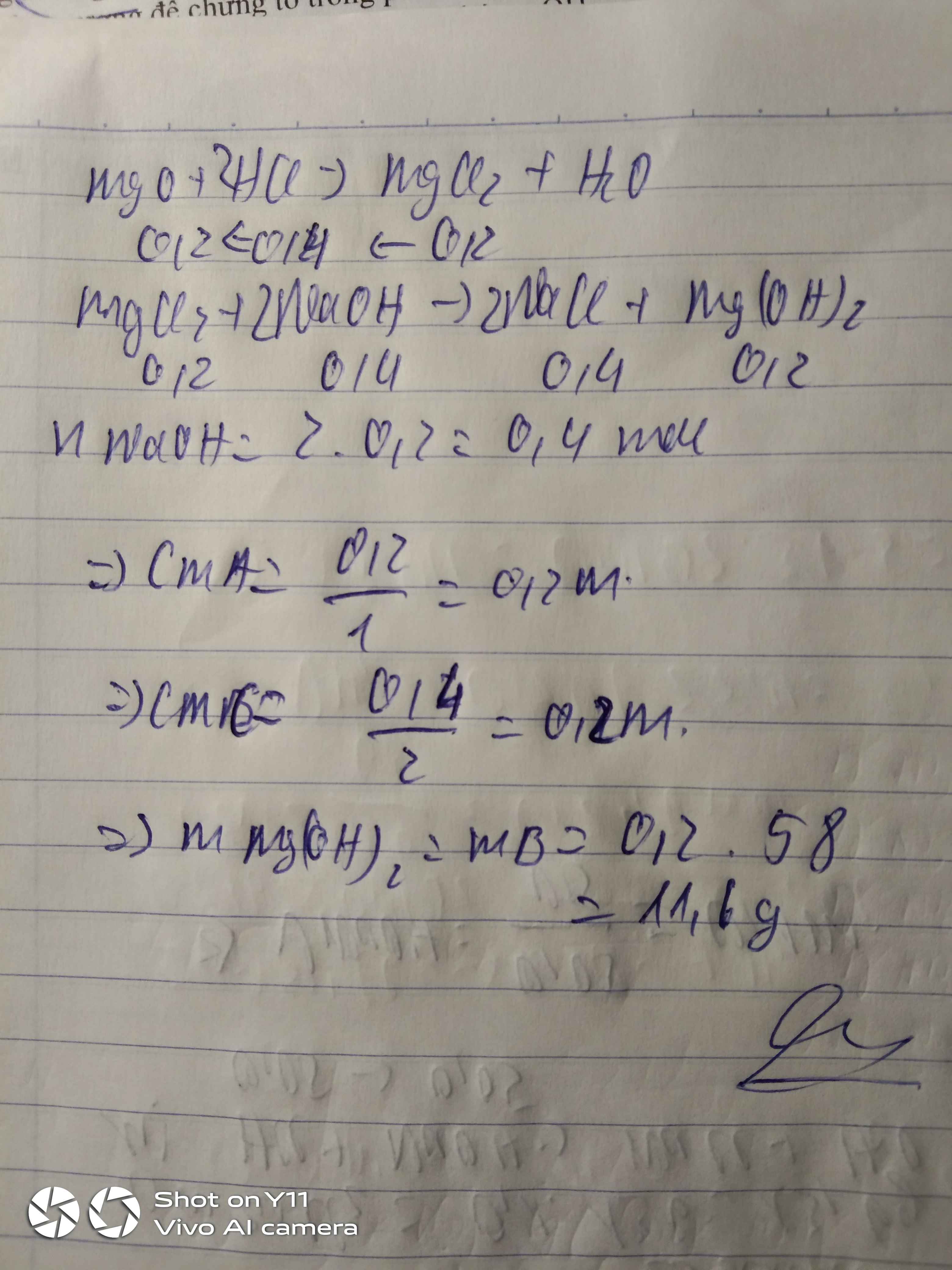cho 300ml naoh 4m tác dụng hoàn toàn với 200ml dd x gồm dd hcl 1m và dd h3so4 2m. tính ph dd sau pu
PH
Những câu hỏi liên quan
Cho 200ml dd K2SO4 2M tác dụng với 300ml dd BaCl2 1M. Sau khi phản ứng xảy ra hoàn toàn thu được chất không tan A và dd B.a) Viết phương trình phản ứng.b) Tính khối lượng chất kết tủa A.c) Tính nồng độ mol của các chất có trong dd B. Biết thể tích của dd thay đổi không đáng kể.
Xem chi tiết
a)
$K_2SO_4 + BaCl_2 \to BaSO_4 + 2KCl$
b)
$n_{K_2SO_4} = 0,2.2 = 0,4(mol)$
$n_{BaCl_2} = 0,3.1 = 0,3(mol)$
Ta thấy :
$n_{K_2SO_4} : 1 > n_{BaCl_2} : 1$ nên $K_2SO_4$ dư
$n_{BaSO_4} = n_{BaCl_2} = 0,3(mol)$
$m_{BaSO_4} = 0,3.233 = 69,9(gam)$
c) $n_{K_2SO_4} = 0,4 - 0,3 = 0,1(mol)$
$V_{dd\ sau\ pư} = 0,2 + 0,3 = 0,5(lít)$
$C_{M_{K_2SO_4} } = \dfrac{0,1}{0,5} = 0,2M$
$C_{M_{KCl}} = \dfrac{0,6}{0,5} = 1,2M$
Đúng 1
Bình luận (0)
Cho 300 ml dd NaOH 1M tác dụng vừa đủ với 200ml dd HCl xM a, Tìm x ? b, Tính CM dd sau pư
\(^nNaOH=1.0,3=0,3\left(mol\right)\)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
mol 0,3 0,3 0,3
a) \(CM_{HCl}=\dfrac{0,3}{0,2}=1,5M\)
b) \(CM_{d^2saupứ}=\dfrac{0,3}{0,3+0,2}=0,6M\)
Chúc bạn học tốt!!!
Đúng 1
Bình luận (0)
a) \(n_{NaOH}=0,3.1=0,3\left(mol\right)\)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
\(n_{HCl}=n_{NaOH}=0,3\left(mol\right)\)
=> \(x=CM_{HCl}=\dfrac{0,3}{0,2}=1,5M\)
b) \(n_{NaCl}=n_{NaOH}=0,3\left(mol\right)\)
=> \(CM_{NaCl}=\dfrac{0,3}{0,3+0,2}=0,6M\)
Đúng 1
Bình luận (0)
dd A chứa đồng thời 2 axit H2SO4 1m và HCl 2M tác dụng với dd b gồm 200ml NaOH 1,5M và BaOH 0,5M môi trường trung tính thì cần thể tích dd x là?
mol H+ = 0,2+0,5.0,2.2 = 0,4 = mol OH-
Đặt mol NaOH = x, mol Ba(OH)2 = y.
Có: x + 2y = 0,4
......x/y = 1/2 (tỉ lệ CM).
=> x = 0,08; y = 0,16
=> Thể tích dd = 0,08/1 = 0,08 lit = 80ml
Đúng 0
Bình luận (2)
Hoà tan MgO bằng dd HCl 1M thu được dd A. Cho dd A tác dụng với 200ml dd NaOH 2M thu được kết tủa B và dd C.
a.Viết PTHH
b.Tính CM dd A và CM dd C
c.Tính khối lượng kết tủa B
Trung hòa 300ml dd Ca(OH)2 1M bằng 200ml dd HCl 0,2M
a) Tính khối lượng muối tạo thành
b) Muối p.ư xảy ra hoàn toàn phải thêm dd Ca(OH)2 1M hay dd HCl 0,2M và thêm với thể tích bao nhiêu ?
c) Tính Cm của dd tạo thành sau p.ư trong trường hợp p.ư xảy ra hoàn toàn
\(n_{Ca\left(OH\right)_2}=0,3.1=0,3\left(mol\right)\\ n_{HCl}=0,2.0,2=0,04\left(mol\right)\)
a
\(Ca\left(OH\right)_2+2HCl\rightarrow CaCl_2+2H_2O\)
0,02<------0,04----->0,02
Xét \(\dfrac{0,3}{1}>\dfrac{0,04}{2}\Rightarrow Ca\left(OH\right)_2.dư\)
\(m_{CaCl_2}=0,02.111=2,22\left(g\right)\)
b
Muốn pứ xảy ra hoàn toàn phải thêm dung dịch HCl 0,2 M
\(n_{HCl.cần}=2n_{Ca\left(OH\right)_2}=0,3.2=0,6\left(mol\right)\\ n_{HCl.cần.thêm}=0,6-0,04=0,56\left(mol\right)\)
\(V_{cần.\left(HCl\right)}=\dfrac{0,56}{0,2}=2,8\left(l\right)=280\left(ml\right)\\ V_{cần.thêm\left(HCl\right)}=280-200=80\left(ml\right)\)
c
\(CM_{CaCl_2}=\dfrac{0,02}{0,3+0,28}=\dfrac{1}{29}M\)
Đúng 3
Bình luận (1)
\(n_{Ca\left(OH\right)_2}=0,3.1=0,3\left(mol\right)\\ n_{HCl}=0,2.0,2=0,04\left(mol\right)\\ Ca\left(OH\right)_2+2HCl\rightarrow CaCl_2+2H_2O\)
0,02<----0,04------>0,02
a
\(m_{CaCl_2}=0,02.111=2,22\left(g\right)\)
b
Muốn pứ xảy ra hoàn toàn thì phải thêm dd HCl 0,2M.
\(n_{HCl.cần}=0,3.2=0,6\left(mol\right)\\ n_{HCl.cần.thêm}=0,6-0,04=0,56\left(mol\right)\\ V_{HCl.cần.}=\dfrac{0,56}{0,2}=2,8\left(l\right)\\ V_{HCl.cần.thêm}=2,8-0,2=2,6\left(l\right)=260\left(ml\right)\)
c
\(CM_{CaCl_2}=\dfrac{0,3}{0,3+2,8}=\dfrac{3}{31}M\)
Đúng 3
Bình luận (2)
Cho 2,7 gam kim loại M thuộc IIIA tác dụng hết với 250ml dd HCl 2M sau phản ứng thu được dd X và 0,15 mol h2 .cho dd X tác dụng với 200ml dd naoh 1,75 sau phản ứng thu được m gam kết tủa.xác định kim loại và tính m?
Hấp thụ hoàn toàn 4,48l khí co2 vào 200ml dd X gồm na2co3 0.3M và naoh xM,sau khi các phản ứng xảy ra hoàn toàn thu được dd Y.Cho toàn bộ Y tác dụng với dd cacl2 dư thu đc 10g kết tủa. Tính x
CO2+ → Na2CO3:0,06 →Na2CO3:0,1
NaOH NaHCO3
kết tủa là CaCO3, nCaCO3 = 0,1 mol -> nNaHCO3 = 0,1
Ta có nCO2 = 0,2 ; nNa2CO3(bđ) = 0,06 mol
Bảo toàn C: => nNaHCO3 = (nCO2 + nNa2CO3(bđ)) - nNa2CO3
= (0,2 + 0,06) - 0,1 = 0,16 mol
Bảo toàn Na: => nNaOH = ( nCaCO3 + nNaHCO3 ) - nNa2CO3
<=> nNaOH = 0,2 => x = 1M
Đúng 0
Bình luận (0)
mấy bạn ở dưới làm sai cả
CO2+ → Na2CO3:0,06 →Na2CO3:0,1
NaOH :0,2x NaHCO3
kết tủa là CaCO3, nCaCO3 = 0,1 mol -> nNaHCO3 = 0,1
Ta có nCO2 = 0,2 ; nNa2CO3(bđ) = 0,06 mol
Bảo toàn C: => nNaHCO3 = (nCO2 + nNa2CO3(bđ)) - nNa2CO3
= (0,2 + 0,06) - 0,1 = 0,16 mol
Bảo toàn Na: => 2nNa2CO3 bđ+nNaOH=2nNa2CO3+nNaHCO3
<=> 2.0,06+0,2x=2.0,1 +0,16
=> x=1,2 M
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 200ml dd hcl 0,5M vào 300ml dd nạo 0,5 M tính pH của dd sau phản ứng
\(n_{H^+}=0,5.0,2=0,1\left(mol\right)\)
\(n_{OH^-}=0,5.0,3=0,15\left(mol\right)\)
\(\Rightarrow n_{OH^-dư}=0,15-0,1=0,05\left(mol\right)\)
\(\Rightarrow\left[OH^-\right]_{\text{sau pư}}=\dfrac{0,05}{0,5}=0,1\)
\(\Rightarrow\left[H^+\right]=10^{-13}\)
\(\Rightarrow pH=13\)
Đúng 1
Bình luận (0)
Cho 5,64g hh A gồm 2 kim loại Mg và Al tác dụng với 200ml dd HCl, khi phản ứng xảy ra hoàn toàn thu được dd chứa kết tủa. Cô hạn hỗn hợp, thu được 21,26g chất rắn khan. Lại lấy 5,64g hh A, cho tác dụng với 300ml dd HCl đã dùng ở trên khi đun nóng, thu được dd và V1 lít H2 (ĐKTC). Lại làm bay hơi hỗn hợp cuối cùng thu được 25,52g muối khan. Tính nồng độ mol của dd HCl và thể tích V1 của khí H2?
Đọc tiếp
Cho 5,64g hh A gồm 2 kim loại Mg và Al tác dụng với 200ml dd HCl, khi phản ứng xảy ra hoàn toàn thu được dd chứa kết tủa. Cô hạn hỗn hợp, thu được 21,26g chất rắn khan. Lại lấy 5,64g hh A, cho tác dụng với 300ml dd HCl đã dùng ở trên khi đun nóng, thu được dd và V1 lít H2 (ĐKTC). Lại làm bay hơi hỗn hợp cuối cùng thu được 25,52g muối khan. Tính nồng độ mol của dd HCl và thể tích V1 của khí H2?