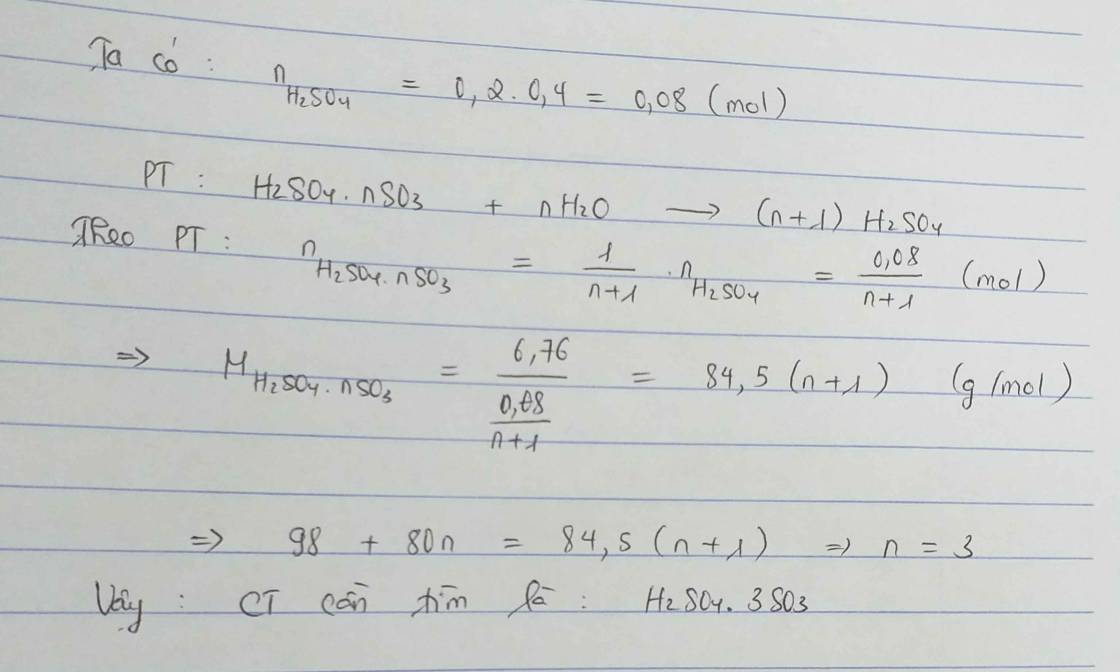Chương 1. Sự điện li
Cho hỗn hợp A gồm hai muối (NH4)2CO3 và NH4HCO3 tác dụng hết với dung dịch NaOH đun nóng, thu được 7,437 lít khí B (đkc). Dẫn toàn bộ khí B vào 100 ml dung dịch AlCl3 1M. Khối lượng kết tủa thu được
Ta có: \(n_{NH_3}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
\(n_{AlCl_3}=0,1.1=0,1\left(mol\right)\)
PT: \(3NH_3+AlCl_3+3H_2O\rightarrow Al\left(OH\right)_3+3NH_4Cl\)
Xét tỉ lệ: \(\dfrac{0,3}{3}=\dfrac{0,1}{1}\), ta được pư vừa đủ.
⇒ nAl(OH)3 = 0,1 (mol)
⇒ mAl(OH)3 = 0,1.78 = 7,8 (g)
Đúng 2
Bình luận (0)
Pt ion : \(NH_4+OH^--->NH_3+H_2O\)
Do đó chất khi thu được là NH3 --> \(n_{NH3}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
Ta có : \(n_{AlCl3}=0,1.1=0,1\left(mol\right)\)
\(AlCl_3+3NH_3+H_2O\rightarrow Al\left(OH\right)_3+3NH_4Cl\)
0,1 0,3 0,1
Xét tỉ lệ :\(\dfrac{0,1}{1}=\dfrac{0,3}{3}\Rightarrow phản.ứng.hết\)
\(\Rightarrow m_{kt}=0,1.78=7,8\left(g\right)\)
Đúng 2
Bình luận (0)
Để xác định nồng độ của dung dịch NaOH ta thực hiện phương pháp chuẩn độ như sau:- Dùng pipete lấy 10ml dung dịch HCl 0,1M (dung dịch chuẩn) cho vào bình tam giác 100ml, thêm 1 - 2 giọt phnolphthalein- Cho dung dịch NaOH cần xác định nồng độ vào burete, điều chỉnh dung dịch trong burete về mức 0- Mở khóa burete, nhỏ từng giọt dung dịch NaOH xuống bình tam giác (lắc đều trong quá trình chuẩn độ) đến khi dung dịch trong bình tam giác từ không màu chuyển sang màu hồng nhạt (bền trong khoảng 10 giây...
Đọc tiếp
Để xác định nồng độ của dung dịch NaOH ta thực hiện phương pháp chuẩn độ như sau:
- Dùng pipete lấy 10ml dung dịch HCl 0,1M (dung dịch chuẩn) cho vào bình tam giác 100ml, thêm 1 - 2 giọt phnolphthalein
- Cho dung dịch NaOH cần xác định nồng độ vào burete, điều chỉnh dung dịch trong burete về mức 0
- Mở khóa burete, nhỏ từng giọt dung dịch NaOH xuống bình tam giác (lắc đều trong quá trình chuẩn độ) đến khi dung dịch trong bình tam giác từ không màu chuyển sang màu hồng nhạt (bền trong khoảng 10 giây) thì ngừng chuẩn độ.
- Ghi lại thể tích dung dịch NaOH đã dùng là 10,2 ml
Vậy nồng độ của dung dịch NaOH là bao nhiêu ?
\(NaOH+HCl\rightarrow NaCl+H_2O\)
Ta có : \(n_{NaOH}=n_{HCl}\Leftrightarrow C_{MNaOH}.V_{NaOH}=C_{MHCl}.V_{HCl}\)
\(\Rightarrow C_{MNaOH}=\dfrac{C_{MHCl}.V_{HCl}}{V_{NaOH}}=\dfrac{0,1.0,01}{0,0102}\simeq0,1l=100ml\)
Đúng 2
Bình luận (1)
Trộn lẫn 100ml dd Koh 1M và H2So4 0.625M thu đc dd Y a) tính nồng độ các ion trong dd b) tính ph sau phản ứng
Đề có cho thể tích dd H2SO4 không bạn nhỉ?
Đúng 0
Bình luận (0)
Có 100 ml dung dịch X gồm NH4+, K+, CO32- ; SO42-. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 cho tác dụng với dung dịch Ba(OH)2 dư, thu được 2,24 lít (đktc) khí NH3 và 66,3 gam kết tủa. Phần 2 tác dụng với lượng dư dung dịch HCl, thu được 2,24 lít (đktc) khí CO2. Cô cạn dung dịch X thu được m gam muối khan. Tính giá trị của m
Đọc tiếp
Có 100 ml dung dịch X gồm NH4+, K+, CO32- ; SO42-. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 cho tác dụng với dung dịch Ba(OH)2 dư, thu được 2,24 lít (đktc) khí NH3 và 66,3 gam kết tủa. Phần 2 tác dụng với lượng dư dung dịch HCl, thu được 2,24 lít (đktc) khí CO2. Cô cạn dung dịch X thu được m gam muối khan. Tính giá trị của m
- Phần 1:
\(n_{NH_4^+}=n_{NH_3}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(197n_{CO_3^{2-}}+233n_{SO_4^{2-}}=66,3\left(1\right)\)
- Phần 2:
\(n_{CO_3^{2-}}=n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Thay vào (1) ⇒ nSO42- = 0,2 (mol)
BT điện tích trong 50ml dd, có: nNH4+ + nK+ = 2nCO32- + 2nSO42-
⇒ mK+ = 2.0,1 + 2.0,2 - 0,1 = 0,5 (mol)
⇒ m = 2.(0,1.18 + 0,1.60 + 0,2.96 + 0,5.39) = 93 (g)
Đúng 3
Bình luận (0)
Câu 1: Cho các chất và ion sau: Fe 3+ ; NaCl ; NH4 + ; S 2- ; HCl ; HCO3 - ; CH3COO - ; NaHSO4 ; HS - . Theo thuyết Bronsted - Lowry, số chất đóng vai trò acid là ?A. 4 B. 3 C. 5 D. 2Câu 2: Chuẩn độ dung dịch NaOH chưa biết nồng độ ( biết nồng độ trong khoảng gần 0,1M ) bằng dung dịch chuẩn HCl 0,1M với chất chỉ thị phenolphtalein. Để xác định nồng độ dung dịch NaOH, số lần thí nghiệm cần lặp lại ít nhất làA. 1 B. 2 C. 3 D. 4Câu...
Đọc tiếp
Câu 1: Cho các chất và ion sau: Fe 3+ ; NaCl ; NH4 + ; S 2- ; HCl ; HCO3 - ; CH3COO - ; NaHSO4 ; HS - . Theo thuyết Bronsted - Lowry, số chất đóng vai trò acid là ?
A. 4 B. 3 C. 5 D. 2
Câu 2: Chuẩn độ dung dịch NaOH chưa biết nồng độ ( biết nồng độ trong khoảng gần 0,1M ) bằng dung dịch chuẩn HCl 0,1M với chất chỉ thị phenolphtalein. Để xác định nồng độ dung dịch NaOH, số lần thí nghiệm cần lặp lại ít nhất là
A. 1 B. 2 C. 3 D. 4
Câu 3: Khi chuẩn độ bằng phương pháp acid - base, người ta thêm từ từ dung dịch đựng trong burette vào dung dịch đựng trong bình tam giác. Thời điểm mà hai chất tác dụng vừa đủ với nhau gọi là gì
A. điểm tương đương
B. điểm cuối
C. điểm chuẩn độ
D. điểm nhận biết
Câu 4: Một hồ bơi tiêu chuẩn khi có độ pH trong nước khoảng từ 7,2 - 7,8. Mất cân bằng pH là một trong những vấn đề thường gặp ở nhiều hồ bơi. Trong trường hợp pH hồ bơi quá thấp sẽ gây tình trạng kích ứng da và mắt cho người bơi. Để làm tăng pH của nước hồ bơi, hóa chất liệu quả được sử dụng là
A. Na2CO3
B. NaOH
C. HCl
D. H2SO4
Câu 1: A
Câu 2: C
Câu 3: A
Câu 4: A
Đúng 3
Bình luận (0)
pH của dung dịch nào sau đây có giá trị nhỏ nhất
a, Dung dịch HNO3 0,1 M
b, Dung dịch HF 0,1M
c, Dung dịch KCL 0,1 M
d, Dung dịch KOH 0,01M
\(a,pH=-log\left[H^+\right]=1\\ b,pH=-log\left[H^+\right]=-log\left[0,1\right]=1\\ c,pH=7\\ d,pH=14-\left(-log\left[OH^-\right]\right)=14-\left(log\left[0,01\right]\right)=12\)
Chọn A và B
Đúng 2
Bình luận (0)
Đáp án: A
a, pH = -log[H+] = 1 (HNO3 là axit mạnh nên phân li hoàn toàn)
b, HF là axit yếu, phân ly không hoàn toàn ⇒ [H+] < 0,1 ⇒ pH > 1
c, KCl là muối trung hòa ⇒ pH = 7
d, KOH là bazo mạnh, phân ly hoàn toàn ⇒ pH = 14 - (-log[0,01]) = 12
Đúng 2
Bình luận (0)
Cho ví dụ: \(KAl\left(SO_4\right)_2.12H_2O\rightarrow K^++Al^{3+}+2SO_4^{2-}+12H_2O\)
Hãy cho biết dung dịch phèn \(\left(NH4Fe\left(SO_4\right)_2.12H_2O\right)\) có môi trường acid hay base. Giải thích. Vì sao người ta có thể dùng phèn sắt để loại bỏ các chất lơ lửng trong nước
Hòa tan 6,76 gam oleum vào nước thì thu được 200ml dung dịch H2SO4 0,4M. Công thức của oleum
Help mình với mọi người:
Hòa tan a gam NaOH khan vào nước thu được 200 mL dung dịch X. Sử dụng máy đo xác định được trong dung dịch X, [OH-] = 0,010M. Tính giá trị của a?
\(NaOH\rightarrow OH^-+Na^+\)
0,01<----0,01
`=> n_{NaOH} = 0,01.0,2 = 0,002(mol)`
`=> a = 0,002.40 = 0,08(g)`
Đúng 1
Bình luận (0)