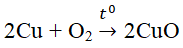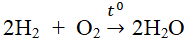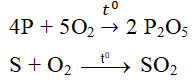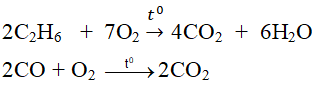nêu tính chất hóa học của silic đioxit ,cho ví dụ về từng tính chất
TP
Những câu hỏi liên quan
nêu tính chất hóa học của silic đioxit và cho ví dụ
Tham khảo:
Tính chất của SiO2:
SiO2 là oxit axit. Ở nhiệt độ cao, tác dụng với kiềm và oxit bazơ tạo thành muối silicat. Silic đioxit không phản ứng với nước.
Ví dụ:
SiO2 + 2NaOH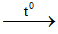 H2O + Na2SiO3 (natri silicat)
H2O + Na2SiO3 (natri silicat)SiO2 + CaO 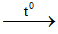
Đúng 1
Bình luận (0)
Nêu tính chất hóa học của Cacbon đioxit và cho ví dụ
Câu 1. Nêu tính chất hóa học a/của oxi ví dụ về sự oxi hóa
Tham khảo:
Câu 1:
Khí oxi là một đơn chất phi kim rất hoạt động, đặc biệt ở nhiệt độ cao, dễ dàng tham gia phản ứng hóa học với nhiều phi kim, nhiều kim loại và hợp chất. Trong các hợp chất hóa học, nguyên tố oxi có hóa trị II.
Cụ thể:
- Tác dụng với kim loại: O2 oxi hóa được hầu hết các kim loại trừ Ag, Au, Pt.
Ví dụ:
- Tác dụng với hiđro, phản ứng có thể gây nổ mạnh nếu tỉ lệ thể tích O2 : H2 = 1:2
Phương trình hóa học:
- Tác dụng với một số phi kim khác:
Ví dụ:
+ Tác dụng với một số hợp chất:
Ví dụ:
Đúng 1
Bình luận (0)
Câu 1. Nêu tính chất hóa học của AXIT. Mỗi tính chất lấy 2 ví dụ minh họaCâu 2. Nêu tính chất hóa học của BAZO. Mỗi tính chất lấy 2 ví dụ minh họaCâu 3. Tính nồng độ phần trăm của 250g dung dịch có chứa 25g muối ăn.Câu 4. Tính nồng độ mol của 200ml dung dịch có 9,8g axit sunfuricCâu 5. Cho 5,6g sắt vào 100ml dung dịch HCl. Tính thể tích khí sinh ra. Tính nồng độ dung dịch HCl đã dùng.Câu 6. Hòa tan nhôm bằng 150ml dung dịch axit sunfuric 1,5M. Tính khối lượng nhôm đã dùng và nồng độ mol của muối...
Đọc tiếp
Câu 1. Nêu tính chất hóa học của AXIT. Mỗi tính chất lấy 2 ví dụ minh họa
Câu 2. Nêu tính chất hóa học của BAZO. Mỗi tính chất lấy 2 ví dụ minh họa
Câu 3. Tính nồng độ phần trăm của 250g dung dịch có chứa 25g muối ăn.
Câu 4. Tính nồng độ mol của 200ml dung dịch có 9,8g axit sunfuric
Câu 5. Cho 5,6g sắt vào 100ml dung dịch HCl. Tính thể tích khí sinh ra. Tính nồng độ dung dịch HCl đã dùng.
Câu 6. Hòa tan nhôm bằng 150ml dung dịch axit sunfuric 1,5M. Tính khối lượng nhôm đã dùng và nồng độ mol của muối tạo thành. Xem như thể tích thay đổi không đáng kể.
Câu 7. Cho 5,6g sắt tác dụng với 300ml dung dịch HCl 1,5M. Tính nồng độ chất sau phản ứng (Xem thể tích thay đổi không đáng kể)
Câu 8. Cho 16 gam hỗn hợp Mg, Fe tan hết trong 100 ml dd HCl 8M. Tính phần trăm khối lượng từng kim loại trong hỗn hợp
giải giúp em nha mọi người :))
thank mọi mười <3
Câu 1 :
+ Làm đổi màu chất chỉ thị màu : làm quỳ tím hóa đỏ
+ Tác dụng với kim loại :
vd : \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
+ Tác dụng với oxit bazo :
vd : \(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
\(BaO+H_2SO_4\rightarrow BaSO_4+H_2\)
+ Tác dụng với bazo :
vd : \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
\(KOH+HCl\rightarrow KCl+H_2O\)
Chúc bạn học tốt
Đúng 2
Bình luận (1)
Câu 2 :
+ Làm đổi màu chất chỉ thị màu : làm quỳ tím hóa xanh
+ Tác dụng với oxit axit :
vd : \(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
\(2KOH+CO_2\rightarrow K_2CO_3+H_2O\)
+ Tác dụng với axit :
vd : \(NaOH+HCl\rightarrow NaCl+H_2O\)
\(Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4+2H_2O\)
+ Bazo không tan bị nhiệt phân hủy :
vd : \(Zn\left(OH\right)_2\rightarrow\left(t_o\right)ZnO+H_2O\)
\(2Fe\left(OH\right)_3\rightarrow\left(t_o\right)Fe_2O_3+3H_2O\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
Câu 3 :
\(C_{NaCl}=\dfrac{25.100}{250}=10\)0/0
Câu 4 : \(n_{H2SO4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
200ml = 0,2l
\(C_{M_{H2SO4}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Câu 5 :
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,1 0,2 0,1
\(n_{H2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,1.22,4=2,24\left(l\right)\)
\(n_{HCl}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
200ml = 0,2l
\(C_{M_{HCl}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
Xem thêm câu trả lời
Câu 1: lấy 2 ví dụ về hỗn hợp, 2 vd về chất tinh khiết?phân biệt hốn hợp và chất tinh khiết?Câu 2:Nguyên tử là gì? nêu cấu tạo của nguyên tử?Câu 3: Nguyên tố hóa học là gì? Nguyên tử khối là gì?Câu 4: lấy 2 ví dụ về đơn chất? 2 ví dụ về hợp chất? phân biệt giữa đơn chất và hợp chất?Câu 5: Nếu ý nghĩa của công thức hóa học SO2 ( lưu huỳnh đioxit )Câu 6: a, phát biểu quy tắc hóa trị?b, tính hóa trị của Fe trong Fe2O3. lập công thức hóa học của Mg(II), và NO3(I). Tính phân tử khốiCâu 7: phân biệt h...
Đọc tiếp
Câu 1: lấy 2 ví dụ về hỗn hợp, 2 vd về chất tinh khiết?
phân biệt hốn hợp và chất tinh khiết?
Câu 2:Nguyên tử là gì? nêu cấu tạo của nguyên tử?
Câu 3: Nguyên tố hóa học là gì? Nguyên tử khối là gì?
Câu 4: lấy 2 ví dụ về đơn chất? 2 ví dụ về hợp chất? phân biệt giữa đơn chất và hợp chất?
Câu 5: Nếu ý nghĩa của công thức hóa học SO2 ( lưu huỳnh đioxit )
Câu 6: a, phát biểu quy tắc hóa trị?
b, tính hóa trị của Fe trong Fe2O3. lập công thức hóa học của Mg(II), và NO3(I). Tính phân tử khối
Câu 7: phân biệt hiện tượng vật lí và hiện tượng hóa học rồi lấy vd
Giups với mai nọp rồi, cám ơn ạ
Nêu các điểm giống và khác nhau về tính chất giữa cacbon đioxit và silic đioxit ?
- Giống nhau: đều là oxit axit
CO2 + 2NaOH → Na2CO3 + H2O
SiO2 tan chậm trong kiềm đặc nóng, tan dễ trong kiềm nóng chảy:
SiO2 + 2NaOHn,c → Na2SiO3 + H2O
- Khác nhau:
| CO2 | SiO2 |
|---|---|
| - Tính chất vật lí: + Chất khí không màu + Tan ít trong nước - Tính chất hóa học: + Có tính oxi hóa CO2 + 2Mg → C + 2MgO |
- Tính chất vật lí: + Chất rắn + Không tan trong nước - Tính chất hóa học: + Tan trong axit HF SiO2 + HF → SiF4 + 2H2O |
Đúng 0
Bình luận (0)
trình bày tính chất hóa học, điều chế, ứng dụng của các chất sau: axit cacbonic muối cacbonat, metan, silic đioxit, etilen, rượu etylic, chất béo
-axit cacbonic
+tính chất hóa học:
- H2CO3 là một axit yếu, dung dịch H2CO3 chỉ làm quỳ tím chuyển thành màu đỏ nhạt, bị axit mạnh đẩy ra khỏi muối.
- H2CO3 là một axit không bền: H2CO3 tạo thành trong các phản ứng hóa học bị phân hủy ngay thành CO2 và H2O.
-điều chế:(SGK)
-Ứng dụng:
- CaCO3 là thành phần chính của đá vôi, được dùng để sản xuất vôi, xi măngr..
- Na2CO3 được dùng để nấu xà phòng, sản xuất thủy tinh,..
- NaHCO3 được dùng làm dược phẩm, hóa chất trong bình cứu hỏa,...- NaHCO3 được dùng làm dược phẩm, hóa chất trong bình cứu hỏa,...- NaHCO3 được dùng làm dược phẩm, hóa chất trong bình cứu hỏa,...
Đúng 2
Bình luận (3)
Xem thêm câu trả lời
Nêu những điểm giống nhau và khác nhau về tính chất giữa cacbon đioxit và silic đioxit.
Nêu tính chất hóa học của oxi, cho ví dụ kèm PTHH
GIÚP MÌNH VỚI Ạ
- Tác dụng với kim loại tạo oxit bazo tương ứng :
\(2Mg + O_2 \xrightarrow{t^o} 2MgO\\ 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\)
- Tác dụng với phi kim :
\(S + O_2 \xrightarrow{t^o} SO_2\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\)
- Tác dụng với một số hợp chất khác :
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ H_2S + \dfrac{3}{2}O_2 \xrightarrow{t^o} SO_2 + H_2O\)
Đúng 3
Bình luận (0)
1. Tác dụng với hầu hết với các kim loại ở nhiệt độ cao trừ Au,Pt,Ag
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
2. Tác dụng với một số phi kim ở nhiệt độ cao
\(C+O_2\underrightarrow{t^o}CO_2\)
3. Tác dụng với một số hợp chất khác:
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Đúng 2
Bình luận (0)
Phản ứng đặc trưng của oxi là phản ứng cháy. Oxi có thể tác dụng với hầu hết các kim loại dưới tác dụng của nhiệt độ để tạo ra các oxit (trừ kim loại vàng và bạch kim Oxi không phản ứng).
VD: PTHH: 2Cu + O2 _____> 2CuO
Đúng 0
Bình luận (1)
Xem thêm câu trả lời