Quan sát Hình 17.1, cho biết vị trí nhóm halogen trong bảng tuần hoàn.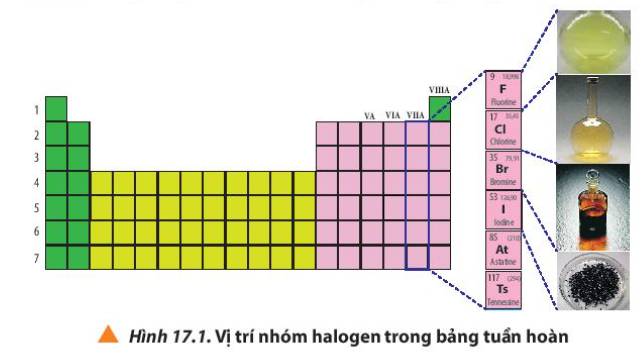
Tuyển Cộng tác viên Hoc24 nhiệm kì 26 tại đây: https://forms.gle/dK3zGK3LHFrgvTkJ6
H24
Những câu hỏi liên quan
Quan sát hình 3.5 và bảng tuần hoàn, hãy cho biết số electron lớp ngoài cùng của nguyên tử Li (lithium) và Cl (chlorine). Hai nguyên tố đó nằm ở nhóm nào trong bảng tuần hoàn?
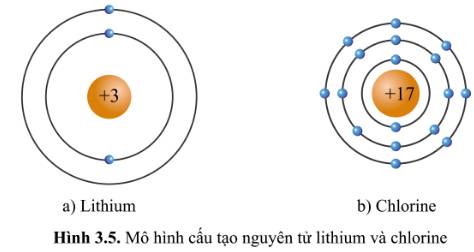
- Xét mô hình cấu tạo của nguyên tử lithium: có 1 hình tròn xanh ở vòng tròn ngoài cùng => Có 1 electron ở lớp vỏ ngoài cùng => Thuộc nhóm IA
- Xét mô hình cấu tạo của nguyên tử chlorine: có 7 hình tròn xanh ở vòng tròn ngoài cùng => Có 7 electron ở lớp vỏ ngoài cùng => Thuộc nhóm VIIA
Đúng 0
Bình luận (0)
Quan sát bảng tuần hoàn các nguyên tố hóa học, hãy cho biết vị trí của các nguyên tố kim loại, phi kim và khí hiếm
- Vị trí kim loại: nằm ở phía bên trái và góc dưới bên phải của bảng tuần hoàn
- Vị trí phi kim: nằm ở phía trên, bên phải của bảng tuần hoàn
- Vị trí khí hiếm: tất cả các nguyên tố nằm trong nhóm VIIIA
Đúng 0
Bình luận (0)
Viết cấu hình electron nguyên tử Na. Cho biết trong bảng tuần hoàn, Na nằm ở ô số 11, chu kì 3, nhóm IA. Nêu mối liên hệ giữa số hiệu nguyên tử, số lớp electron, số electron lớp ngoài cùng và vị trí của Na trong bảng tuần hoàn.
- Cấu hình electron của Na (Z = 11): 1s22s22p63s1
- Trong bảng tuần hoàn, Na nằm ở ô số 11, chu kì 3, nhóm IA.
⟹ Ta thấy:
+ Số hiệu nguyên tử = số thứ tự ô = 11
+ Số lớp electron = số thứ tự chu kì = 3
+ Số electron lớp ngoài cùng = số thứ tự nhóm = 1e
Đúng 0
Bình luận (0)
Dựa vào bảng tuần hoàn (Hình 4.2), em hãy cho biết vị trí (nhóm, chu kì) của các nguyên tố K, Mg, Al
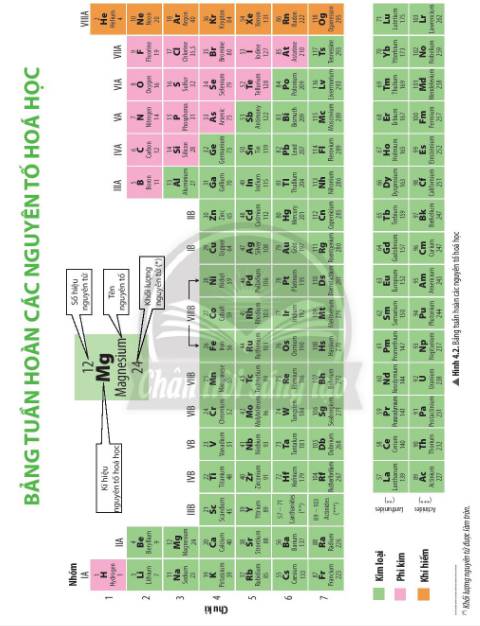
K ở nhóm IA, chu kì2
Mg ở nhóm IIA,chu kì 3
Al thuộc nhóm IIIA, chu kì 3
Đúng 0
Bình luận (0)
Câu 4: Hai nguyên tố X và Y thuộc hai nhóm A liên tiếp trong cùng một chu kì của bảng tuần hoàn và có tổng số điện tích hạt nhân bằng 51. Viết cấu hình electron của X, Y và cho biết vị trí của X, Y trong bảng tuần hoàn.
Đọc tiếp
Câu 4: Hai nguyên tố X và Y thuộc hai nhóm A liên tiếp trong cùng một chu kì của bảng tuần
hoàn và có tổng số điện tích hạt nhân bằng 51. Viết cấu hình electron của X, Y và cho biết vị trí
của X, Y trong bảng tuần hoàn.
Cho biết số hiệu nguyên tử Cr là 24. Vị trí của Cr ( chu kỳ, nhóm) trong bảng hệ thống tuần hoàn là:
A. chu kỳ 4, nhóm VIB
B. chu kỳ 3, nhóm VIB
C. chu kỳ 4, nhóm IVB.
D. chu kỳ 3, nhóm IVB.
Đáp án A
Cấu hình e của Cr là [Ar]3d54s1 → Cr có 6e hóa trị, e cuối cùng điền vào phân lớp d → Cr thuộc nhóm VIB, chu kì 4
Đúng 0
Bình luận (0)
Quan sát bảng tuần hoàn (Phụ lục 1) và cho biết các nguyên tố nhóm IA có đặc điểm về cấu hình electron tương tự nhau như thế nào?
- Nhóm IA gồm: H, Li, Na, K, Rb, Cs, Fr.
- Cấu hình electron của các nguyên tố nhóm IA:
H: 1s1 ; Li: 2s1 ; Na: 3 s1 ; K: 4 s1 ; Rb: 5 s1 ; Cs: 6 s1 ; Fr: 7 s1
- Các nguyên tố nhóm IA là các nguyên tố nhóm s, chỉ có 1 electron ở lớp ngoài cùng (ns1).
Đúng 0
Bình luận (0)
Cấu hình electron nguyên tử nguyên tố X là [Ne] 3 s 2 3 p 1
Cho biết vị trí (số thứ tự, chu kì, nhóm) của nguyên tố X trong bảng tuần hoàn. X là kim loại, phi kim hay khí hiếm ?
Cấu hình e đầy đủ của X : 1 s 2 2 s 2 2 p 6 3 s 2 3 p 1 → Z = 13 = STT, chu kì 3 (có 3 lớp e), nhóm IIIA, (có 3 lớp ngoài cùng, là nguyên tố p), kim loại.v
Đúng 0
Bình luận (0)
và Y là hai nguyên tố thuộc 2 chu kì kế tiếp nhau và cùng trong 1 nhóm A của bảng tuần hoàn . Tổng điện tích hạt nhân của X và Y là 52 Cho biết vị trí của X và Y trong bảng tuần hoàn hoá học
Gọi \(Z_X,Z_Y\) là điện tích của hạt nhân X,Y.
Tổng điện tích hạt nhân : \(Z_X+Z_Y=52\)(1)
X và Y thuộc hai chu kì liên tiếp nên xảy ra 2 trường hợp:
\(\left[{}\begin{matrix}Z_X-Z_Y=8\\Z_X-Z_Y=18\end{matrix}\right.\)
TH1: \(Z_X-Z_Y=8\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}Z_X=30\\Z_Y=22\end{matrix}\right.\)
\(X\left(Z=30\right):\left[Ar\right]3d^{10}4s^2\)\(\Rightarrow\)X nằm ở ô thứ 30, chu kì 4 nhóm llB.
\(Y\left(Z=22\right):\left[Ar\right]3d^24s^2\)\(\Rightarrow\) Y nằm trong ô thứ 22, chu kì 4 nhóm lllB.
Vậy TH này loại vì cùng thuộc 1 chu kì.
TH2: \(Z_X-Z_Y=18\) (3)
Từ (1) và (3) \(\Rightarrow\left\{{}\begin{matrix}Z_X=35\\Z_Y=17\end{matrix}\right.\)
\(X\left(Z=35\right):\left[Ar\right]3d^{10}4s^24p^5\)\(\Rightarrow\)X nằm trong ô thứ 35, chu kì 4 nhóm VllA.
\(Y\left(Z=17\right):\left[Ne\right]3s^23p^5\)\(\Rightarrow\) Y nằm trong ô thứ 17 chu kì 3 nhóm VllA.
Vậy TH này thỏa mãn ycbt.
Đúng 1
Bình luận (0)




