Vận dụng quy tắc octet để giải thích sự hình thành liên kết trong các phân tử: F2, CCl4, NF3.
Tuyển Cộng tác viên Hoc24 nhiệm kì 26 tại đây: https://forms.gle/dK3zGK3LHFrgvTkJ6
H24
Những câu hỏi liên quan
Vận dụng quy tắc octet để giải thích sự hình thành liên kết hóa học trong một số phân tử của các nguyên tử nguyên tố nhóm A.
Quy tắc octet: Khi hình thành liên kết hoá học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững của nguyên tử khí hiếm.
Ví dụ:
- Phân tử O2
Khi hình thành liên kết hoá học trong phân tử O2, nguyên tử oxygen có 6 electron hoá trị, mỗi nguyên tử oxygen cần thêm 2 electron để đạt cấu hình electron bão hoà theo quy tắc octet nên mỗi nguyên tử oxygen góp chung 2 electron.
Phân tử O2 được biểu diễn như sau:

Đúng 0
Bình luận (0)
Cho các phân tử CCl4, NF3 Sử dụng thuyết VB và thuyết lai hóa hãy: - Giải thích sự hình thành liên kết - Cho biết cấu trúc phân tử (vẽ hình) - Cho biết loại liên kết được hình thành. - Cho biết số cặp electron liên kết và không liên kết. - Cho biết từ tính của phân tử.
bạn nên chụp rồi lưu ảnh thì nó mới hiện lên dc
Đúng 0
Bình luận (0)
Cho các phân tử CCl4, NF3 Sử dụng thuyết VB và thuyết lai hóa hãy:
- Giải thích sự hình thành liên kết
- Cho biết cấu trúc phân tử (vẽ hình)
- Cho biết loại liên kết được hình thành.
- Cho biết số cặp electron liên kết và không liên kết.
- Cho biết từ tính của phân tử.
Cho các phân tử CCl4, NF3 Sử dụng thuyết VB và thuyết lai hóa hãy:
- Giải thích sự hình thành liên kết
- Cho biết cấu trúc phân tử (vẽ hình)
- Cho biết loại liên kết được hình thành.
- Cho biết số cặp electron liên kết và không liên kết.
- Cho biết từ tính của phân tử.
Cho các phân tử CCl4, NF3 Sử dụng thuyết VB và thuyết lai hóa hãy: - Giải thích sự hình thành liên kết - Cho biết cấu trúc phân tử (vẽ hình) - Cho biết loại liên kết được hình thành. - Cho biết số cặp electron liên kết và không liên kết. - Cho biết từ tính của phân tử.
có ai trả lời giúp tui đi
Quát đờ ku, hoá lớp 10 luôn đó bay, xỉu ót xỉu đao
Câu 616. Theo quy tắc octet (bát tử): Trong quá trình hình thành liên kết hóa học, nguyên tử các nguyên tố nhóm Á có xu hướng tạo thành lớp vỏ ngoài cùng cóA. 8 electron tương ứng với khí hiểm gần nhất.B. & electron tương ứng với khi hiếm gần nhất ( hoặc 2 electron tương ứng với khí hiểmHelium.).C. 2 electron tương ứng với kim loại gần nhất.D. 6 electron tương ứng với phi kim gần nhất.Câu 617. Nguyên tử nguyên tố nào sau đây có xu hướng đạt cấu hình electron bền vững của khi hiếm argon khi tham...
Đọc tiếp
Câu 616. Theo quy tắc octet (bát tử): Trong quá trình hình thành liên kết hóa học, nguyên tử các nguyên tố nhóm Á có xu hướng tạo thành lớp vỏ ngoài cùng có
A. 8 electron tương ứng với khí hiểm gần nhất.
B. & electron tương ứng với khi hiếm gần nhất ( hoặc 2 electron tương ứng với khí hiểm
Helium.).
C. 2 electron tương ứng với kim loại gần nhất.
D. 6 electron tương ứng với phi kim gần nhất.
Câu 617. Nguyên tử nguyên tố nào sau đây có xu hướng đạt cấu hình electron bền vững của khi hiếm argon khi tham gia hình thành liên kết hóa học
A. Fluorine.
B. Oxygen.
C. Hydrogen.
D. Chlorine.
Câu 618: Liên kết ion là liên kết được tạo thành
A. bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
B. bởi cặp electron chung giữa 1 nguyên tử kim loại và 1 nguyên tử phi kim.
C. bởi cặp electron chung giữa 2 nguyên tử phi kim điển hình.
D. bởi cặp electron chung giữa 2 nguyên tử kim loại.
Câu 619: Liên kết ion thường được tạo thành giữa
A. kim loại điển hình (Na, K...) và phi kim điển hình (F, Cl, O...).
B. kim loại và phi kim bất kỳ.
C. hai phi kim có chênh lệch độ âm điện không đáng
kể.
D. hai phi kim có chênh lệch độ âm điện tương đối (1,7 > Ax>0,4
Câu 620: Liên kết ion trong KC1 là do
A.kali và clo chung 1 electron tạo thành cặp electron chung lệch về phía kali
B. kali và cho góp chung 1 electron tạo thành cặp electron chung lệch về phía cho.
C. nguyên tử kali có nhường electron tạo anion, nguyên tử clo nhận electron tạo cation.
D. nguyên tử kali có nhường electron tạo cation, nguyên tử clo nhận electron tạo anion.
Câu 621: Bản chất liên kết trong phân tử NaCl là
A. liên kết ion.
B. liên kết cộng hóa trị có cực.
C. liên kết cộng hóa trị không cực.
D. liên kết phối trí (cho nhận).
Câu 622: Chất nào dưới đây có liên kết ion :
A. Cl₂
B. HCI
C. NaF
D. O₂
Câu 623: Dãy các chất đều chứa liên kết ion là:
B. Na O, MgO, HCI
D. O2, NaCl, KCI
A. Cl₂, NaCl, H₂O
C. NaF, KCI, KO
623: C
622: C
621: A
619:A
617: D
618:A
Đúng 1
Bình luận (0)
Giải thích sự hình thành liên kết trong phân tử H2O bằng cách áp dụng quy tắc octet.
tham khảo
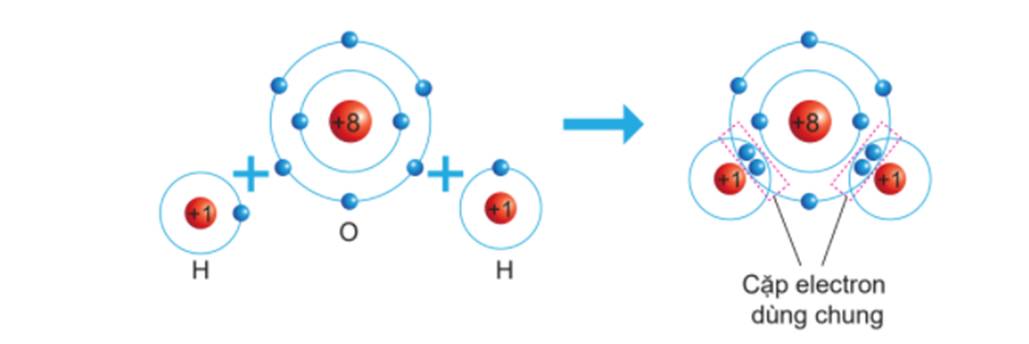
- Nguyên tử O (Z = 8): 1s22s22p4 ⇒ Có 6 electron lớp ngoài cùng ⇒ Có xu hướng nhận 2 electron để đạt được cấu hình electron giống khí hiếm.
- Nguyên tử H (Z = 1): 1s1 ⇒ Có xu hướng nhận 1 electron để đạt được cấu hình electron giống khí hiếm.
⇒ Mỗi nguyên tử H sẽ góp chung 1 electron với nguyên tử O (góp chung 2 electron) tạo thành 2 cặp electron dùng chung
Đúng 0
Bình luận (0)
Bài 4: Giải thích sự hình thành liên kết trong phân tử H2O bằng cách áp dụng quy tắc octet
- Phân tử H2O được hình thành bởi 2 ion H+ và 1 ion O2-
- Nguyên tử nguyên tố hydrogen cho đi 1 electron tạo thành H+ để đạt cấu hình electron bền vững của khí hiếm
- Nguyên tử nguyên tố oxygen nhận 2 electron tạo thành O2- để đạt cấu hình electron bền vững của khí hiếm Ne
Đúng 1
Bình luận (0)
Nguyên tử fluorine (F) có cấu hình electron là [He]2s22p5. Khi các nguyên tử F liên kết với nhau, để thỏa mãn quy tắc octet, một bạn học sinh đề xuất như sau: Một nguyên tử F nhường 7 electron, tạo ion F7+ có cấu hình là [He]; 7 nguyên tử F khác, mỗi nguyên tử nhận 1 electron tạo 7 ion F- có cấu hình [Ne]. Sau đó 8 ion này hút nhau tạo thành chất có công thức (F7+)(F-)7. Vì sao đề xuất này không hợp lí trong thực tế? Hãy mô tả sự hình thành liên kết trong phân tử F2.
Đọc tiếp
Nguyên tử fluorine (F) có cấu hình electron là [He]2s22p5. Khi các nguyên tử F liên kết với nhau, để thỏa mãn quy tắc octet, một bạn học sinh đề xuất như sau: Một nguyên tử F nhường 7 electron, tạo ion F7+ có cấu hình là [He]; 7 nguyên tử F khác, mỗi nguyên tử nhận 1 electron tạo 7 ion F- có cấu hình [Ne]. Sau đó 8 ion này hút nhau tạo thành chất có công thức (F7+)(F-)7. Vì sao đề xuất này không hợp lí trong thực tế? Hãy mô tả sự hình thành liên kết trong phân tử F2.
- Cấu hình electron của F (Z = 9): 1s22s22p5
- Đề xuất của bạn học sinh không hợp lí trong thực tế vì:
+ Fluorine là nguyên tử có độ âm điện lớn nên khả năng nhận 1 electron dễ hơn nhường 7 electron.
+ Hai nlguyên tử F có độ âm điện bằng nhau nên không hình thành được liên kết ion như công thức (F7+)(F-)7 mà chỉ tạo được liên kết cộng hóa trị không cực.
- Sự hình thành liên kết trong phân tử F2:
Để đạt cấu hình của khí hiếm gần nhất, mỗi nguyên tử F đều cần thêm 1 electron. Vì vậy mỗi nguyên tử N cùng góp 1 electron để tạo nên 1 cặp electron chung cho 2 nguyên tử N.

⟹ Hai nguyên tử F liên kết với nhau bằng liên kết cộng hóa trị không cực tạo phân tử F2:
F - F
Đúng 0
Bình luận (0)






