Trình bày tính chất hoá học của nước, viết các phương trính hoá học minh hoạ
NK
Những câu hỏi liên quan
ÔN TẬP HỌC KÌ 1I,Viết sơ đồ cây cho các nội dung sau:+ PHT1: Nêu những tính chất hoá học của oxi. Viết phương trình phản ứng minh hoạ.+ PHT 2: Nêu những tính chất hoá học của hiđro. Viết phương trình minh hoạ.+ PHT 3: Nêu tính chất hoá học của nước. Viết phương trình hoá học minh hoạ.+ PHT 4:Nêu tính chất hóa học của oxit+ PHT 5: Nêu khái niệm và công thức tính nồng độ dung dịch II, Bài tậpB/ BÀI TẬP:1. Nhiệt phân hoàn toàn 12,25g KClO3. Tính thể tích khí O2 ( ở đktc) thu được ?2. Muốn điều c...
Đọc tiếp
ÔN TẬP HỌC KÌ 1
I,Viết sơ đồ cây cho các nội dung sau:
+ PHT1: Nêu những tính chất hoá học của oxi. Viết phương trình phản ứng minh hoạ.
+ PHT 2: Nêu những tính chất hoá học của hiđro. Viết phương trình minh hoạ.
+ PHT 3: Nêu tính chất hoá học của nước. Viết phương trình hoá học minh hoạ.
+ PHT 4:Nêu tính chất hóa học của oxit
+ PHT 5: Nêu khái niệm và công thức tính nồng độ dung dịch
II, Bài tập
B/ BÀI TẬP:
1. Nhiệt phân hoàn toàn 12,25g KClO3. Tính thể tích khí O2 ( ở đktc) thu được ?
2. Muốn điều chế được 48 g O2 thì khối lượng KClO3 cần nhiệt phân là bao nhiêu g ?
3. Muốn điều chế được 2,8 lít O2 (ở đktc) thì khối lượng KMnO4 cần nhiệt phân là bao nhiêu ?
4. Trong phòng thí nghiệm, người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng O2 oxi hóa sắt ở nhiệt độ cao. Để điều chế được 2,32g Fe3O4 cần dùng :
a/ Bao nhiêu gam sắt ?
b/ Bao nhiêu lít khí O2 ( ở đktc) :
5. Đốt cháy 1kg than trong khí O2, biết trong than có 10% tạp chất không cháy.Tính:
a. thể tích oxi (đktc) cần thiết để đốt cháy 1kg than trên.
b. thể tích khí cacbonic CO2 (đktc) sinh ra trong phản ứng trên
6. Người ta dùng đèn xì oxi –axetilen để hàn cắt kim loại. Phản ứng cháy của axetilen C2H2 trong oxi tạo thành khí cacbonic và hơi nước. Hãy tính thể tích oxi (đktc) cần thiết để đốt cháy 1mol C2H2
7. Đốt cháy hoàn toàn 5,4g nhôm. Tính :
a. thể tích khí O2 (đktc) cần dùng ?
b. số gam KMnO4 cần dùng để điều chế lượng khí O2 trên ?
8. Xác định công thức hóa học của nhôm oxit, biết tỉ lệ khối lượng của 2 nguyên tố nhôm và oxi bằng 4,5 : 4.
9. Một oxit của lưu huỳnh trong đó oxi chiếm 60% về khối lượng. Tìm công thức phân tử của oxit đó?
10. Cho 5,6 g sắt vào 100 ml dung dịch HCl 1M . Hãy:
a) Tính lượng khí H2 tạo ra ở đktc?
b) Chất nào còn dư sau phản ứng và lượng dư là bao nhiêu?
c) Tính nồng độ các chất sau phản ứng?
11. Nếu đốt cháy 13,5g nhôm trong một bình kín chứa 6,72 lít oxi (ở đktc) tạo thành nhôm oxit Al2O3 thì :
a/ Chất nào còn dư sau phản ứng? Số gam chất dư ?
b/ Tính khối lượng Al2O3 tạo thành?
12. Đốt cháy 6,2g photpho trong bình kín chứa 7,84 lít oxi (ở đktc) tạo thành điphotpho pentaoxit P2O5 thì
a/ Chất nào còn dư sau phản ứng? Số gam chất dư ?
b/ Tính khối lượng P2O5 tạo thành?
13. Cho 28,4g điphotpho pentaoxit P2O5 vào cốc chứa 90g nước để tạo thành axit photphoric. Tinh khối lượng axit H3PO4 được tạo thành ?
14. Hoàn thành những phản ứng hóa học sau :
a/ . . . + . . . ![]() MgO
MgO
b/ . . . + . . . ![]() P2O5
P2O5
c/ . . . + . . . ![]() Al2O3
Al2O3
d/ . . . + . . . ![]() Na2S
Na2S
e/ H2O ![]() . . . + . . .
. . . + . . .
f/ KClO3![]() . . . + . . .
. . . + . . .
g/ . . . + . . . ![]() CuCl2
CuCl2
h/ KMnO4 ![]() K2MnO4 + MnO2 + . . .
K2MnO4 + MnO2 + . . .
i/ Mg + HCl ![]() . . . + . . .
. . . + . . .
j/ Al + H2SO4 ![]() . . . + . . .
. . . + . . .
k/ H2 + . . . ![]() Cu + . . .
Cu + . . .
l/ CaO + H2O ![]() . . .
. . .
Cho biết mỗi phản ứng hóa học trên thuộc loại phản ứng hoá học nào ?
15. Gọi tên, phân loại các chất sau: Ca(OH)2, NaOH, KOH, Mg(OH)2, HNO3, H2SO4, HCl, H3PO4, NaCl, FeO, CuO, K2SO4, Na3PO4, AgNO3, CaSO4, NaHCO3, MgO, NaHSO4, Ca(HCO3)2, NaH2PO4
16. Hãy phân biệt các chất sau :
a. 4 bình đựng riêng biệt các khí sau: không khí, khí oxi, khí hiđro, khí cacbonic
b. 3 lọ mất nhãn đựng dung dịch NaOH, H2SO4, Na2SO4
c. Có 3 gói bột mất nhãn chứa các chất sau : Na2O, SO3, MgO
17. Khử 48g đồng (II) oxit bằng khí hiđro. Khối lượng đồng kim loại thu được và thể tích khí hiđro (ở đktc) cần dùng là bao nhiêu ?
18. Trong phòng thí nghiệm, người ta dùng hiđro để khử sắt (III) oxit và thu được 11,2g sắt. Tinh khối lượng sắt (III) oxit đã phản ứng ?
19. Khử 12g sắt (III) oxit bằng khí hiđro.Tính: thể tích khí hiđro (đktc) cần dùng và khối lượng sắt thu được ?
20. Người ta điều chế được 24g đồng bằng cách dùng hiđro khử đồng (II) oxit. Tính :khối lượng đồng (II) oxit bị khử và thể tích khí hiđro (đktc) đã dùng ?
21. Cho 22,4g sắt tác dụng với dung dịch loãng chứa 24,5g axit sunfuric. Tính :
Khối lượng chất còn dư sau phản ứng? Thể tích khí hiđro thu được ở đktc ?
22. Khi cho 13g kẽm tác dụng với 0,3 mol HCl. Khối lượng ZnCl2 được tạo thành trong phản ứng này là bao nhiêu gam?
23. Cho 19,5g kẽm tác dụng hết với dung dịch axit clohiđric. Hãy cho biết :
a/ Tính thể tích khí H2 (đktc) thu được
b/ Nếu dùng thể tích khí H2 trên để khử 19,2g sắt (III) oxit thì thu được bao nhiêu gam sắt ?
24. Thể tích khí hiđro và khí oxi (ở đktc) cần tác dụng với nhau để tạo ra được 1,8g nước là ?
25. Để có 1 dung dịch chứa 16g NaOH, cần phải lấy bao nhiêu gam Na2O cho tác dụng với nước ?
26.Cho 9,2g Na vào nước dư thì thu được dung dịch NaOH và khí H2. Tính thể tích khí H2 (đktc) thoát ra và khối lượng NaOH tạo thành ?
27. Khối lượng mol của 1 oxit kim loại là 160gam, thành phần về khối lượng của kim loại trong oxit đó là 70%. Xác định công thức hóa học của oxit ?
28. Lập phương trình hoá học của các phản ứng sau và cho biết các phản ứng trên thuộc loại phản ứng nào?
a/ Sắt (III) oxit + hiđro ![]() sắt + nước
sắt + nước
b/ Lưu huỳnh trioxit + nước ![]() axit sunfuric
axit sunfuric
c/ Nhôm + sắt (III)oxit ![]() sắt + nhôm oxit
sắt + nhôm oxit
d/ Canxi oxit + nước ![]() canxi hiđroxit
canxi hiđroxit
e/ Kali + nước ![]() kali hiđroxit + khí hiđro
kali hiđroxit + khí hiđro
f/ Kẽm + axit sufuric (loãng) ![]() kẽm sunfat + khí hiđro
kẽm sunfat + khí hiđro
29. Hãy tính nồng độ mol của mỗi dung dịch sau:
a/ 1 mol KCl trong 750ml dung dịch
b/ 400g CuSO4 trong 4 lít dung dịch
c/ 0,5mol MgCl2 trong 1,5 lít dung dịch
d/ 0,06mol Na2CO3 trong 1500ml dung dịch
30. Hãy tính số mol và số gam chất tan trong mỗi dung dịch sau:
a/ 500ml dung dịch KNO3 2M
b/ 250ml dung dịch CaCl2 0,1M
31. Tính nồng độ % của những dung dịch sau :
a. 20g KCl trong 600g dung dịch
b. 75g K2SO4 trong 1500g dung dịch
c. Hòa tan 15g NaCl vào 45g nước
d. Hòa tan 4,48 lít khí hiđro clorua HCl ( đktc) vào 500g nước
32. Tính số gam chất tan cần dùng để pha chế mỗi dung dịch sau:
a/ 2,5 lít dung dịch NaCl 0,9M
b/ 250 ml dung dịch MgSO4 0,1M
c/ 50g dung dịch MgCl2 4%
d/ 200g dung dịch KCl 15%
33. Để pha chế 250ml dung dịch NaOH 0,5M cần bao nhiêu ml dung dịch NaOH 2M và bao nhiêu ml nước?
34. Cho 200 g dung dịch NaOH 20% tác dụng vừa hết với 100 g dung dịch HCl . Tính:
a) Nồng độ muối thu được sau phản ứng?.
b) Tính nồng độ axit HCl. Biết phản ứng xảy ra hoàn toàn?.
35. Hòa tan hoàn toàn 10,6g Na2CO3 vào nước đựơc 200ml dung dịch Na2CO3. Tính nồng độ phần trăm và nồng độ mol của dung dịch trên. Biết khối lượng riêng của dung dịch là 1,05g/ml.
36. Hãy tính:
1. Số mol của Kali hiđrôxit trong 28 gam dung dịch KOH 10%..
2. Nồng độ phần trăm của dung dịch tạo thành khi cho 36 gam đường vào 144 gam nước ?
3. Nồng độ mol của dung dịch NaOH, biết rằng trong 80 ml dung dịch này có chứa 0,8 gam NaOH 37. Dùng 500 ml dung dịch H2SO4 1,2M để hoà tan hết lượng kim loại sắt, phản ứng tạo thành sắt (II) sunfat và khí hiđro.
a) Viết phương trình hoá học của phản ứng.
b) Tính khối lượng muối sắt(II) sunfat thu được.
c) Tính thể tích khí H2 thoát ra (ở đktc) ? (Cho Fe = 56; H = 1; O = 16; S = 32)
38. Hòa tan 32,5 gam Zn bằng dung dịch HCl, sau phản ứng tạo ra muối kẽm clorua (ZnCl2) và khí H2.
a) Hãy viết phương trình hóa học của phản ứng ?
b) Tính khối lượng muối ZnCl2 và thể tích H2 tạo thành sau phản ứng ? (Biết các khí đo ở điều kiện tiêu chuẩn) (Cho Zn = 65; H = 1; O = 16; Cl = 35,5)
39. Cho 8,1 g Al tác dụng vừa đủ với dung dịch HCl
a) Hoàn thành phương trình hoá học.
b) Tính thể tích khí hiđro tạo thành (ở đktc)
c) Tính khối lượng AlCl3 tạo thành. (Biết Al = 27, H = 1, O = 16, Cl = 35,5).
40. Cho a gam kim loại Kẽm vào 400 ml dung dịch HCl. Sau khi phản ứng kết thúc thu được 2,24 lít khí Hiđro ( ở đktc).
a) Viết phương trình hoá học xảy ra.
b) Tính a.
c) Tính nồng độ mol/lít của dung dịch HCl đã tham gia phản ứng.
41. Cho 6,5g Zn tác dụng với 100g dung dịch HCl 14,6%.
a) Viết phương trình phản ứng xảy ra.
b) Chất nào còn dư lại sau phản ứng, với khối lượng là bao nhiêu?
c) Tính thể tích khí Hidro thoát ra ở ĐKTC (Cho Zn = 65; H = 1; O = 16; Cl = 35,5)
42. Cho 13 gam Zn tác dụng với dung dịch có chứa 18,25 gam HCl.
a) Tính xem chất nào còn dư sau phản ứng và khối lượng dư là bao nhiêu ?
b) Tính khối lượng ZnCl2 tạo thành sau phản ứng.
c) Tính thể tích khí H2 thu được ở đktc. (Cho Zn = 65; H = 1; O = 16; Cl = 35,5)
43. Người ta dẫn luồng khí H2 đi qua ống đựng 4,8 gam bột CuO được nung nóng trên ngọn lửa đèn cồn, cho đến khi toàn bộ lượng CuO màu đen chuyển thành Cu màu đỏ thì dừng lại.
a) Viết phương trình phản ứng xảy ra ?
b) Tính số gam Cu sinh ra?
c) Tính thể tích khí hiđrô (đktc) vừa đủ dùng cho phản ứng trên ?
d) Để có lượng H2 đó phải lấy bao nhiêu gam Fe cho tác dụng vừa đủ với bao nhiêu gam axít HCl. (Cho Cu = 64; H = 1; O = 16; Cl = 35,5)
44. Cho 13 gam kẽm phản ứng hoàn toàn với dung dịch HCl.
1. Viết phương trình hoá học
2. Tính thể tích khí hidro sinh ra (đktc)
3. Nếu dùng toàn bộ lượng H2 bay ra ở trên đem khử 12 gam bột CuO ở nhiệt độ cao thì chất nào còn dư bao nhiêu gam ? ( Zn = 65 ; Cl = 35,5 ; Cu = 64 ; O = 16 ; H= 1 )
C/ TRẮC NGHIỆM KHÁCH QUAN:
Khoanh tròn vào một chữ cái A, B, C hoặc D đứng trước phương án chọn đúng:
1. Oxit là:
A. Hợp chất của oxi với 1 nguyên tố khác
B. Hợp chất gồm 2 nguyên tố, trong đó có 1 nguyên tố là oxi.
C. Hợp chất được tạo bởi nguyên tố oxi và 1 nguyên tố nào đó.
D. Cả A, B, C đúng.
2. Oxit axit là:
A. Là oxit của phi kim và tương ứng với 1 axit B. Là oxit của kim loại và tương ứng với 1 axit
C.Là oxit của phi kim và tương ứng với 1 oxit axit D.Thường là oxit của phi kim và tương ứng với 1 axit
3. Oxit bazơ là:
A. Là oxit của phi kim và kim loại, tương ứng với 1 bazơ
B. Là oxit của kim loại và tương ứng với 1 bazơ
C. Thường là oxit của phi kim và tương ứng với 1 bazơ
D. Là oxit của phi kim và tương ứng với 1 oxit axit
4. Cho các oxit sau: CO2, SO2, Fe2O3, P2O5, K2O. Trong đó có:
A. Hai oxit axit và 3 oxit bazơ B. Ba oxit axit và 2 oxit bazơ
C. Một oxit axit và 4 oxit bazơ D. Bốn oxit axit và 1 oxit bazơ
5. Cho các oxit sau: CaO, SO2, Fe2O3, P2O5, K2O. Trong đó có:
A. Hai oxit axit và 3 oxit bazơ B. Ba oxit axit và 2 oxit bazơ
C. Một oxit axit và 4 oxit bazơ D. Bốn oxit axit và 1 oxit bazơ
6. Cho các oxit sau: CO2, SO2, Fe2O3, P2O5, Mn2O7. Trong đó có:
A. Hai oxit axit và 3 oxit bazơ B. Ba oxit axit và 2 oxit bazơ
C. Một oxit axit và 4 oxit bazơ D. Bốn oxit axit và 1 oxit bazơ
7. Cho các oxit sau: CuO, BaO, Fe2O3, P2O5, K2O. Trong đó có:
A. Hai oxit axit và 3 oxit bazơ B. Ba oxit axit và 2 oxit bazơ
C. Một oxit axit và 4 oxit bazơ D. Bốn oxit axit và 1 oxit bazơ
8. Cho các oxit có công thức hóa học sau:
CO2 ; CO ; CaO ; P2O5 ; NO2 ; Na2O ; MgO ; N2O5 ; Al2O3
a) Các oxit axit được sắp xếp như sau:
A. CO2 ; CO ; NO2 ; Na2O B. CO ; CaO ; P2O5 ; N2O5
C. CO2 ; P2O5 ; NO2 ; N2O5 D. CaO ; P2O5 ; Na2O ; Al2O3
b) Các oxit bazơ được sắp xếp như sau:
A. CaO ; Na2O; MgO ; N2O5 B. CaO ; MgO ; Na2O ; Al2O3
C. CaO ; P2O5 ; Na2O ; Al2O3 D. MgO ; N2O5 ; Na2O ; Al2O3
9. Trong các oxít sau đây, oxít nào tác dụng được với nước.
A. SO3, CuO, Na2O, B. SO3 , Na2O, CO2, CaO.
C. SO3, Al2O3, Na2O. D. Tất cả đều sai.
10. Trong những chất sau đây, chất nào là axít .
A. H2SiO3, H3PO4, Cu(OH)2, Na2SiO3 B. HNO3, Al2O3, NaHSO4, Ca(OH)2.
C. H3PO4, HNO3, H2SiO3. D. Tất cả đều sai.
11. Dãy chất nào chỉ gồm toàn axit:
A. HCl; NaOH B. CaO; H2SO4 C. H3PO4; HNO3 D. SO2; KOH
12. Dãy chất nào sau đây gồm toàn oxit bazơ:
A. Fe2O3 , CO2, CuO, NO2 B. Na2O, CuO, HgO, Al2O3
C. N2O3, BaO, P2O5 , K2O D. Al2O3, Fe3O4, BaO, SiO2.
13. Dãy hợp chất gồm các bazơ tan trong nước :
A. Mg(OH)2 ; Cu(OH)2 ; Fe(OH)3 B. NaOH ; KOH ; Ca(OH)2
C. NaOH ; Fe(OH)2 ; AgOH D. Câu b, c đúng
14. Dãy hợp chất gồm các bazơ đều không tan trong nước :
A. Mg(OH)2 ; Cu(OH)2 ; Fe(OH)3 B. NaOH ; KOH ; Ca(OH)2
C. NaOH ; Fe(OH)2 ; LiOH D. Al(OH)3 ; Zn(OH)2 ; Ca(OH)2.
15. Dãy các chất nào sau đây đều tan trong nước:
A. NaOH, BaSO4, HCl, Cu(OH)2. B. NaOH, HNO3, CaCO3, NaCl.
C. NaOH, Ba(NO3)2 , FeCl2, K2SO4. D. NaOH, H2SiO3, Ca(NO3)2, HCl.
16. Dung dịch làm quỳ tím hóa đỏ là :
A. H2O B. Dung dịch NaOH
C. Dung dịch H2SO4 D. Dung dịch K2SO4
17. Trong số những chất có công thức HH dưới đây, chất nào làm cho quì tím không đổi màu:
A. HNO3 B. NaOH C. Ca(OH)2 D. NaCl
18. Có thể phân biệt các dung dịch axit, muối ăn, kiềm bằng cách dùng :
A. Nước cất B. Giấy quỳ tím C. Giấy phenolphtalein D. Khí CO2
19. *Có những chất rắn sau: FeO, P2O5, Ba(OH)2, NaNO3. Thuốc thử được chọn để phân biệt các chất trên là:
A. dung dịch H2SO4, giấy quỳ tím. B. H2O, giấy quỳ tím.
C. dung dịch NaOH, giấy quỳ tím. D. dung dịch HCl, giấy quỳ.
20. Dãy chất nào sau đây gồm toàn muối:
A. KCl, HNO3, CuCl2, NaHCO3 B. NaNO3, Al2(SO4)3, NaOH, H2S
C. ZnCl2, Mg(NO3)2, KCl, Na2S D. Cu(NO3)2, PbCl2, FeS2, AgCl.
21. Dãy chất nào sau đây gồm toàn muối không tan trong nước:
A. Na2SO3, Al2(SO4)3, KHSO4, Na2S B. KCl, Ba(NO3)2 , CuCl2, Ca(HCO3)2
C. ZnCl2, Mg(NO3)2, KCl, K2S D. BaSO4, AgCl, CaCO3, Ca3(PO4)2.
22. Cho biết phát biểu nào dưới đây là đúng:
A. Gốc cacbonat (CO3) và sunfat (SO4) hoá trị I B. Gốc photphat (PO4) hoá trị II
C. Gốc Clorua (Cl) và Nitrat (NO3) hoá trị III D. Nhóm hiđroxit (OH) hoá trị I
23. Từ công thức hoá học Fe2O3 và H2 SO4, công thức tạo bởi Fe và SO4 là:
A. FeSO4 B. Fe2 (SO4)3 C. Fe (SO4)3 D. Fe3(SO4)2
24. Cho các phương trình phản ứng sau:
1. Zn + 2HCl ® ZnCl2 + H2
2. 2H2O ![]() 2H2 + O2
2H2 + O2
3. 2 Al + 3H2SO4 ® Al2( SO4 )3 + 3H2
4. 2Mg + O2 ![]() 2MgO
2MgO
5. 2 KClO3 ![]() 2KCl + 3O2
2KCl + 3O2
6. H2 + CuO ![]() Cu + H2O
Cu + H2O
7. 2H2 + O2 ![]() 2 H2O
2 H2O
A. Phản ứng hoá hợp là:
a. 1, 3 b. 2, 5 c. 4,7 d. 3, 6
B. Phản ứng phân huỷ là:
a. 5, 6 b. 2 , 5 c. 4, 5 d. 2, 7
C. Phản ứng thế là:
a. 1, 3, 6 b. 1, 3, 7 c. 3, 5, 6 d. 4, 6, 7.
25. Cặp chất nào sau đây dùng để điều chế oxi trong phòng thí nghiệm:
A. H2O, KClO3 B. KMnO4, H2O C. KClO3, KMnO4 D. HCl, Zn
26. Cho các khí: CO, N2, O2, Cl2, H2 .Các khí nhẹ hơn không khí là:
A. N2 , H2 , CO B. N2, O2, Cl2 C. CO, Cl2 D. Cl2,O2
27. Dãy gồm các chất khí nặng hơn không khí :
A. CO2 , H2 B. CO, CO2 C. N2, H2 D.SO2, O2
28. Ứng dụng của hiđro là:
A. Dùng làm nguyên liệu cho động cơ xe lửa
B. Dùng làm chất khử để điều chế một số kim loại từ oxit của chúng
C. Dùng để bơm vào khinh khí cầu
D. Tất cả các ứng dụng trên
29. Cách nào dưới đây thường dùng để điều chế hiđro trong phòng thí nghiệm:
A. Cho Zn tác dụng với dd HCl B. Điện phân nước
C. Cho Na tác dụng với nước D. Cho Cu tác dụng với dd H2SO4 đặc nóng
30. Tính chất hoá học của oxi là:
A. Tác dụng với kim loại B. Tác dụng với phi kim
C. Tác dụng với hợp chất D. Cả 3 tính chất trên
31. Sự oxi hóa là:
A. Sự tác dụng của oxi với 1 kim loại. B. Sự tác dụng của oxi với 1 phi kim.
C. Sự tác dụng của oxi với 1 chất. D. Sự tác dụng của oxi với 1 nguyên tố hoá học.
32. Sự oxi hóa chậm là:
A. Sự oxi hóa mà không tỏa nhiệt. B. Sự oxi hóa mà không phát sáng.
C. Sự oxi hóa toả nhiệt mà không phát sáng. D. Sự tự bốc cháy.
33. Biến đổi hoá học nào sau đây thuộc phản ứng oxi hoá - khử ?
A. Nung nóng canxi cacbonat (CaCO3) để sản xuất canxi oxit (CaO)
B. Lưu huỳnh (S) cháy trong khí oxi (O2).
C. Canxi oxit (CaO) tác dụng với nước (H2O) thành canxi hiđroxit [Ca(OH)2 ]
D. Cacbon đioxit (CO2) tác dụng với nước (H2O) tạo axit cacbonic (H2CO3)
34. Nước là hợp chất mà phân tử được tạo bởi:
A. một nguyên tử H và một nguyên tử O B. hai nguyên tử H và một nguyên tử O
C. hai nguyên tử H và hai nguyên tử O D. một nguyên tử H và hai nguyên tử O.
35. Để tổng hợp nước người ta đã đốt cháy hoàn toàn 4,48 lít khí hiđro ( đktc) trong oxi. Thể tích khí oxi cần dùng là:
A. 2,24 lit B. 4,48 lit C. 44,8 lit D. 22,4 lit
36. Cho H2O tác dụng vừa đủ với Na. Sản phẩm tạo ra là:
A. Na2O B. NaOH và H2 C. NaOH D. Không có phản ứng.
37. Dung dịch là hỗn hợp:
A. Của chất rắn trong chất lỏng B. Của chất khí trong chất lỏng
C. Đồng nhất của chất rắn và dung môi D. Đồng nhất của dung môi và chất tan.
38. Nồng độ phần trăm của dung dịch là:
A. Số gam chất tan trong 100g dung môi B. Số gam chất tan trong 100g dung dịch
B. Số gam chất tan trong 1 lít dung dịch D. Số mol chất tan trong 1 lít dung dịch.
39. Dung dịch muối ăn 8 % là:
Dung dịch có 8 phần khối lượng muối ăn và 100 phần khối lượng nước.
Dung dịch có 8 phần khối lượng muối ăn và 92 ml nước .
Dung dịch có 8 phần khối lượng muối ăn và 92 phần khối lượng nước.
Dung dịch có 8 phần khối lượng nước và 92 phần khối lượng muối ăn.
40. Nồng độ mol/lít của dung dịch là:
A. Số gam chất tan trong 1 lít dung dịch B. Số gam chất tan trong 1lít dung môi
B. Số mol chất tan trong 1lít dung dịch D. Số mol chất tan trong 1lít dung môi.
41. Độ tan của một chất trong nước ở một nhiệt độ xác định là:
A. Số gam chất đó có thể tan trong 100g dung dịch
B. Số gam chất đó có thể tan trong 100g nước
C. Số gam chất đó có thể tan trong 100g dung môi để tạo thành dung dịch bão hoà
D. Số gam chất đó có thể tan trong 100g nước để tạo thành dung dịch bão hoà
42. Khi hoà tan 100ml rượu êtylic vào 50ml nước thì:
A. Rượu là chất tan và nước là dung môi B. Nước là chất tan và rượu là dung môi
C. Nước và rượu đều là chất tan D. Nước và rượu đều là dung môi
43. Khi tăng nhiệt độ và giảm áp suất thì độ tan của chất khí trong nước thay đổi như thế nào?
A. Tăng B. Giảm C. Có thể tăng hoặc giảm D. Không thay đổi
44. Khi tăng nhiệt độ thì độ tan của chất rắn trong nước thay đổi như thé nào?
A. Đều tăng B. Đều giảm C. Phần lớn tăng D. Phần lớn giảm
45. Muốn tăng tốc độ hoà tan của chất rắn vào chất lỏng, ta thường:
A. tăng nhiệt độ của chất lỏng B. nghiền nhỏ chất rắn
C. khuấy trộn D. A, B, C đều đúng.
46. Với một lượng chất tan xác định khi tăng thể tích dung môi thì:
A. C% tăng,CM tăng B. C% giảm ,CM giảm
C. C% tăng,CM giảm D. C% giảm,CM tăng
47. Để tính nồng độ mol của dung dịch NaOH, người ta làm thế nào?
A.Tính số gam NaOH có trong 100g dung dịch B.Tính số gam NaOH có trong 1000g dung dịch
C.Tính số gam NaOH có trong 1 lít dung dịch D. Tính số mol NaOH có trong 1 lít dung dịch
48. Để tính nồng độ phần trăm của dung dịch HCl, người ta làm thế nào?
A.Tính số gam HCl có trong 100g dung dịch B.Tính số gam HCl có trong 1lít dung dịch
C.Tính số gam HCl có trong 1000g dung dịch D.Tính số mol HCl có trong 1lít dung dịch
49. Trong thí nghiệm cho từ từ 2 muỗng đường vào nước. Dung dịch đường này có thể hòa tan thêm đường, A. Dung dịch đường bão hòa B. Dung dịch đường chưa bão hòa
C. Dung dịch đồng nhất D. Cả A, B, C đều đúng
50. Trong phòng thí nghiệm, muốn chuyển đổi dung dịch NaCl bão hòa thành một dung dịch chưa bão hòa, ta cần:
A. Cho thêm nước B. Cho thêm muối C. Đun nóng dung dịch muối D. Cả A,C đúng.
ĐỀ THAM KHẢO
ĐỀ SỐ 1:
I. LÝ THUẾT:(7 điểm)
Câu 1(1.5điểm) Trình bày tính chất hóa học của nước ? Viết các phương trình hóa học minh họa? Câu 2 (1.0điểm) Hãy nhận biết các chất sau bị mất nhãn: Natri hiđroxit NaOH, axit clohiđric HCl, nước H2O?
Câu 3 (2.0điểm) Hãy gọi tên và phân loại các chất có công thức hóa học sau:
MgCl2 , Fe(OH)3, SO3 , H2SO4.
Câu 4 (2.5điểm) Cho các phương trình hóa học sau
a) ? + 2O2 ![]() Fe3O4
Fe3O4
b) H2 + CuO ![]() Cu + ?
Cu + ?
c) ?H2O ![]() ? + O2
? + O2
d) ?Al + ?HCl à 2AlCl3 + ?
a/ Hãy hoàn thành và phân loại các phản ứng trên?
b/ Phản ứng nào dùng để điều chế hiđro trong phòng thí nghiệm?
II.BÀI TOÁN: (3điểm)
Cho 3,25 gam Kẽm tác dụng hết với dung dịch axit Clohiđric tạo ra Kẽm clorua ZnCl2 và khí hiđro.
a/ Viết phương trình hóa học của phản ứng?
b/ Tính thể tích dung dịch axit clohiđric 0.5M đã phản ứng ?
c/ Cho một hỗn hợp gồm nhôm và sắt tác dụng hết với dung dịch H2SO4 thấy thoát ra khí Hiđro đúng bằng lượng Hiđro thu được ở phản ứng trên. Tính thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp, biết số mol của hai kim loại này trong hỗn hợp bằng nhau ?
( Cho O = 16; Al = 27; Fe = 56; Zn = 65)
---------------------------HẾT---------------------------
ĐỀ SỐ 2:
Câu 1 :( 1 đ)
a) Oxit là gì ?
b) Trong các oxit sau: CaO, CO2 , MgO, SO2 , P2O5, Fe3O4 .
- Oxit nào thuộc oxit axit.
- Oxit nào thuộc oxit bazơ.
Câu 2 (2đ)
Viết các PTHH theo sơ đồ biến hóa sau (ghi điều kiện phản ứng nếu có).
Cu -> CuO -> H2O -> H2SO4 -> H2.
Câu 3 : ( 3 đ)
a. Cho biết các chất dưới đây thuộc loại hợp chất nào ? Viết công thức các chất đó: Natrihiđrôxit; Axit photphoric; Natri Clorua ;
b. Cho các chất sau: K; BaO; SO2 đều tác dụng được với nước.
Viết phương trình phản ứng hóa học xảy ra?
c. Bằng phương pháp hóa học hãy nhận biết các lọ dung dịch mất nhãn sau : NaCl; NaOH; H2SO4
Câu 4 : (2đ)
Trong phòng thí nghiệm oxit sắt từ (Fe3O4) được điều chế bằng cách dùng oxi để oxi hóa sắt ở nhiệt độ cao.
Tính khối lượng sắt và thể tích khí oxi ( ở đktc) cần thiết để điều chế được 3,48 gam oxit sắt từ.
Để có được lượng oxi trên cần phải phân hủy bao nhiêu gam kaliclorat?
Câu 5: (1,5đ)
Trong 200 ml dung dịch có hòa tan 16 gam CuSO4. Hãy tính nồng độ mol của dung dịch CuSO4?
Dung dịch H2SO4 có nồng độ 14 %. Hãy tính khối lượng H2SO4 có trong 150 gam dung dịch?
Câu 6: (0,5 đ )
Đốt cháy hoàn toàn 7,2 g kim loại R có hóa trị II thu được 12 g oxit. Xác định tên nguyên tố R trên.
Em tách ra mỗi bài đăng 1 lượt nha!
Đúng 0
Bình luận (0)
Nêu tính chất hoá học của bazơ tan , viết phương trình minh hoạ
Nêu tính chất hoá học của bazơ không tan , viết phương trình minh hoạ
Từ hỗn hợp chứa CaCO3 và MgCO3 hãy trình bày cách điều chế muối MgCl2 và CaCl2 riêng
biệt, chỉ dùng thêm nước và 1 hoá chất khác (các dụng cụ thí nghiệm có đủ). Viết các phương trình hoá học minh hoạ.
Đem nhiệt phân hỗn hợp muối thu được CO2, MgO, CaO
MgCO3 -> (t°) MgO + CO2
CaCO3 -> (t°) CaO + CO2
Thả hỗn hợp vào nước và thổi CO2 vào MgO không tan, CaO tan ta lọc lấy MgO
CaO + H2O -> Ca(OH)2
Ca(OH)2 + CO2 -> CaCO3 + H2O
CaCO3 + H2O + CO2 -> Ca(HCO3)2
Ta đem dd còn lại đi cô cạn ta được CaCO3
Ca(HCO3)2 -> (t°) CaCO3 + H2O + CO2
Đem CaCO3 đi nhiệt phân ta thu được CaO:
CaCO3 -> (t°) CaO + CO2
Đem CaO và MgO tác dụng lần lượt với dd HCl dư rồi lọc lấy MgCl2 và CaCl2 riêng biệt:
CaO + HCl -> CaCl2 + H2O
MgO + HCl -> MgCl2 + H2O
Đúng 1
Bình luận (0)
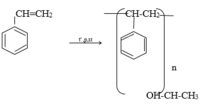
So sánh tính chất hoá học của etylbenzen với stiren, viết phương trình hoá học của phản ứng để minh hoạ.
a. Giống nhau: đều phản ứng thế
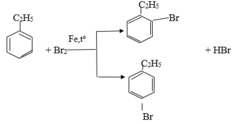
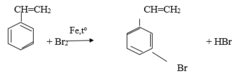
b. Khác nhau:
Etylbenzen có tính chất giống ankan
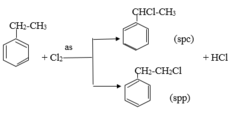
Stiren có tính chất giống anken
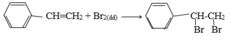
Đúng 0
Bình luận (0)
Sắt có những tính chất hoá học nào ? Viết các phương trình hoá học minh hoạ.
1. Tác dụng với phi kim
a) Tác dụng với oxi.
3Fe + 2O2 \(\rightarrow\) Fe3O4 (oxit sắt từ, sắt có hóa trị II và III)
b) Tác dụng với phi kim khác.
2Fe + 3Cl2 \(\rightarrow\) 2FeCl3
2. Tác dụng với dung dịch axit:
Sắt tác dụng với HCl, H2SO4 loãng tạo thành muối sắt (II) và giải phóng Hg.
Fe + 2HCl \(\rightarrow\) FeCl2, + H2
Chú ỷ: Sắt không tác dụng với HNO3, H2S04đặc, nguội.
3. Tác dụng với dung dịch muối của kim loại yếu hơn sắt.
Fe + CuSO4 -> FeSO4 + Cu
Đúng 0
Bình luận (0)
1. Tác dụng với phi kim
a) Tác dụng với oxi.
3Fe + 2O2 → Fe3O4 (oxit sắt từ, sắt có hóa trị II và III)
b) Tác dụng với phi kim khác.
2Fe + 3Cl2 → 2FeCl3
2. Tác dụng với dung dịch axit: Sắt tác dụng với HCl, H2SO4 loãng tạo thành muối sắt (II) và giải phóng Hg.
Fe + 2HCl → FeCl2, + H2
*Chú ý: Sắt không tác dụng với HN03, H2S04đặc, nguội.
3. Tác dụng với dung dịch muối của kim loại yếu hơn sắt.
Fe + CuSO4 -> FeSO4 + Cu
Đúng 0
Bình luận (0)
Nêu những tính chất hoá học giống nhau và khác nhau giữa silic và cacbon. Viết các phương trình hoá học để minh hoạ.
- C và Si đều thể hiện tính khử hoặc tính oxi hóa trong các phản ứng hóa học
+ Đều có tính oxi hóa: ( tác dụng được với một số kim loại)
\(C+Mg\underrightarrow{^{to}}Mg_2C\\ Si+Mg\underrightarrow{^{to}}Mg_2Si\)
+ Đều có tính khử : ( tác dụng với một số phi kim)
\(C+O_2\underrightarrow{to}CO_2\\
Si+O_2\underrightarrow{to}SiO_2\)
- Khác nhau:
+ Si tác dụng mạnh được với dung dịch kiềm giải phóng khí H2 còn C thì không:
\(Si+2NaOH+H_2O\rightarrow Na_2SiO_3+2H_2\uparrow\)
+ C khử được một số oxit kim loại còn Si thì không khử được:
\(C+2FeO\underrightarrow{^{to}}2Fe+CO_2\uparrow\)
Đúng 0
Bình luận (0)
Viết phương trình hoá học của phản ứng giữa SO2 và dung dịch NaOH minh hoạ cho tính chất hoá học của sulfur dioxide.
\(SO_2+2NaOH\rightarrow Na_2SO_4+H_2O\\ SO_2+NaOH\rightarrow NaHSO_3\)
Đúng 0
Bình luận (0)
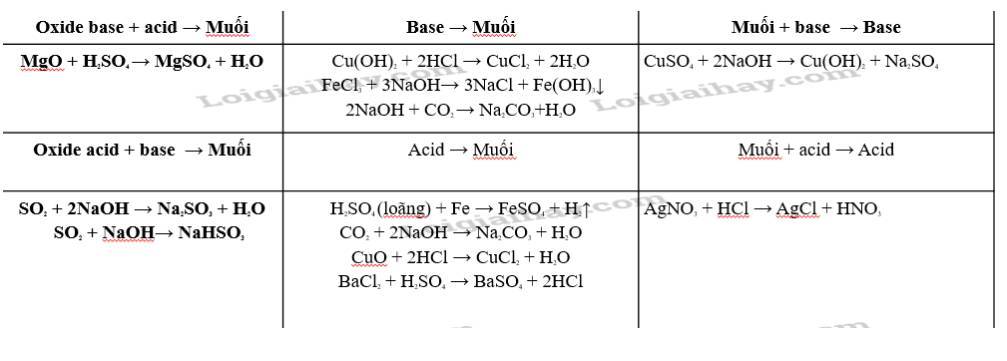
Tính chất hoá học của các hợp chất vô cơ được tóm tắt bằng sơ đồ dưới đây:
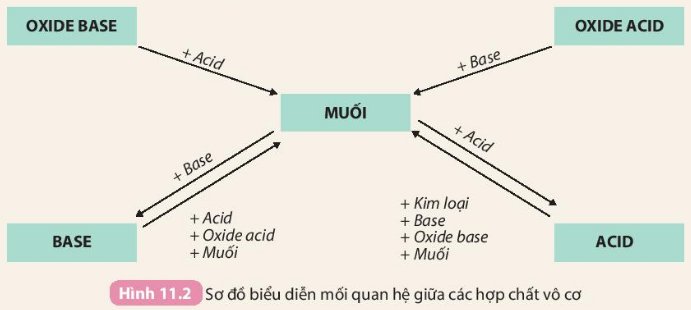
Dựa vào sơ đồ Hình 11.2 và cho biết tính chất của oxide, acid, base. Viết phương trình hoá học minh hoạ.
Hãy chỉ ra những tính chất hoá học chung và khác biệt giữa axit nitric và axit sunfuaric. Viết các phương trình hoá học để minh hoạ?
- Những tính chất khác biệt:
+ Với axit H2SO4 loãng có tính axit, còn H2SO4 đặc mới có tính oxi hoá mạnh, còn axit HNO3 dù là axit đặc hay loãng đề có tính oxi hoá mạnh khi tác dụng với các chất có tính khử.
+ H2SO4 loãng không tác dụng được với các kim loại đứng sau hiđro trong dãy hoạt động hoá học như axit HNO3.
Fe + H2SO4 (loãng) → FeSO4 + H2↑
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
- Những tính chất chung:
∗ Với axit H2SO4 loãng và HNO3 đều có tính axit mạnh
+ Thí dụ:
Đổi màu chất chỉ thị: Quỳ tím chuyển thành màu hồng
Tác dụng với bazơ, oxit bazơ không có tính khử (các nguyên tố có số oxi hoá cao nhất):
2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3+ 6H2O
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
2HNO3 + CaCO3 → Ca(NO3)2 + H2O + CO2↑
H2SO4 + Na2SO3 → Na2SO4 + H2O + SO2↑
∗ Với axit H2SO4(đặc) và axit HNO3 đều có tính oxi hoá mạnh
+ Thí dụ:
Tác dụng được với hầu hết các kim loại (kể cả kim loại đứng sau hiđro trong dãy hoạt động hoá học) và đưa kim loại lên số oxi hoá cao nhất.
Fe + 4HNO3 → Fe(NO3)3 + NO↑ + 2H2O
Cu + 2H2SO4(đặc) → CuSO4 + SO2↑ + 2H2O
Tác dụng với một số phi kim (đưa phi kim lên số oxi hoá cao nhất)
C + 2H2SO4(đặc) → CO2↑ + 2SO2↑ + 2H2O
S + 2HNO3 → H2SO4 + 2NO↑
Tác dụng với hợp chất( có tính khử)
3FeO + 10HNO3 → 3Fe(NO3)3 + NO↑ + 5H2O
2FeO + 4H2SO4(đặc) → Fe2(SO4)3 + SO2↑ + 4H2O
Cả hai axit khi làm đặc nguội đều làm Fe và Al bị thụ động hoá (có thể dùng bình làm bằng nhôm và sắt để đựng axit nitric và axit sunfuaric đặc)
Đúng 0
Bình luận (0)