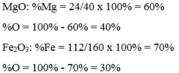xác định thành phần phần trăm theo khối lượng các nguyên tố trong hợp chất sất(III) oxit FE2O3
H24
Những câu hỏi liên quan
Tính thành phần phần trăm theo khối lƣợng của các nguyên tố trong hợp chất sau: a) Sắt(III) oxit: Fe2O3 b) Nhôm sunfat : Al2(SO4)3
a) \(\left\{{}\begin{matrix}\%Fe=\dfrac{56.2}{160}.100\%=70\%\\\%O=100\%-70\%=30\%\end{matrix}\right.\)
b) \(\left\{{}\begin{matrix}\%Al=\dfrac{27.2}{342}.100\%=15,79\%\\\%S=\dfrac{32.3}{342}.100\%=28,07\%\\\%O=\dfrac{16.12}{342}.100\%=56,14\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Xác định thành phần trăm theo khối lượng của các nguyên tố có trong hợp chất AgNO3
\(M_{AgNO_3}=108+14+16.3=170\left(DvC\right)\)
\(\%Ag=\dfrac{108}{170}.100\%=63,5\%\\ \%N=\dfrac{14}{170}.100\%=8,2\%\\ \%O=100\%-63,5\%-8,2\%=28,3\%\)
Đúng 3
Bình luận (0)
%Ag=108\170 .100=63,53 %
%N =14\170 .100=8,23%
%O =16.3\170.100=28,24%
Đúng 3
Bình luận (2)
Tính thành phần % về khối lượng của nguyên tố oxi có trong hợp các chất: khí cacbon dioxit (CO2) và nhôm oxit (AL2O3). Từ đó hãy xác định trong hợp chất nào có nhiều oxi nhất (chiếm thành phần % theo khối lượng nguyên tố oxi cao nhất.)
Trong $CO_2$ : $\%O = \dfrac{16.2}{44}.100\% = 72,73\%$
Trong $Al_2O_3$ : $\%O = \dfrac{16.3}{102}.100\% = 47,06\%$
Suy ra: $\%O : CO_2 > Al_2O_3$
Đúng 2
Bình luận (0)
Xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.Hợp chấtkhối lượng mình mol( M )Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chấtKhối lượng của mỗi nguyên tố có trong 1 mol hợp chấtThành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chấtKMnO4 -Nêu các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất ....
Đọc tiếp
Xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.
| Hợp chất | khối lượng mình mol( M ) | Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất | Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất | Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất |
| KMnO4 |
-Nêu các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất .
-Viết công thức tính thành phần phần trăm theo khối lượng của 1 nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.
Khối lượng mol :
MKMnO4 = 39 + 55 + 64 = 158 (g/mol)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất :
nK = 1 mol
nMn = 1 mol
nO = 4 mol
Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất :
mK = 39.1 = 39 (g)
mMn = 55.1 = 55 (g)
mO = 16.4 = 64 (g)
Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất :
\(\%m_K=\frac{m_K}{M_{KMnO_4}}.100\%=\frac{39}{158}.100\%=24,7\%\)
\(\%m_{Mn}=\frac{m_{Mn}}{M_{KMnO_4}}.100\%=\frac{55}{158}.100\%=34,8\%\)
\(\%m_O=\frac{m_O}{m_{KMnO_4}}.100\%=\frac{64}{158}.100\%=40,5\%\)
Đúng 0
Bình luận (5)
Các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất :
B1 : Tính khối lượng mol (M) của hợp chất.
B2 : Tính số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Tính khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B4 : Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.
Đúng 0
Bình luận (0)
Công thức tính thành phần phần trăm theo khối lượng của 1 nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất :
\(\%m_A=\frac{m_A}{M_{h\text{/}c}}.100\%\)
Đúng 0
Bình luận (7)
X là nguyên tố phi kim có hoá trị III trong hợp chất với khí hiđro. Biết thành phần phần trăm khối lượng của hiđro trong hợp chất là 17,65%. Xác định nguyên tố X.
Công thức hoá học của hợp chất có dạng XH 3 .
17,65% ứng với (3 x 1)đvC
(100 - 17,65)% ứng với 82,35x3/17,65 = 14(đvC)
Nguyên tử X có nguyên tử khối là 14, vậy nguyên tố X là nitơ (N).
Đúng 0
Bình luận (0)
CTHH của hợp chất Y có dạng là NaxNyOz. Thành phần phần trăm theo khối lượng các nguyên tố Y như sau: 27,06% Na; 16,47% N và 56,47% O. xác định CTHH của Y, biết khối lượng mol của Y là 85g/mol
nêu các bước giải bài toán xác định CTHH của hợp chất khi biết thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất
B1 : Tìm khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B2 : Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Lập CTHH.
Đúng 0
Bình luận (1)
còn xác định công thức hóa hc của Y nữa mà bn
Đúng 0
Bình luận (4)
Bước 1: Tìm khối lượng mol của nguyên tố có trong 1 mol hợp chất.
Bước 2: Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
Bước 3: Lập CTHH của hợp chất.
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Câu 4 . Xác định phần trăm về khối lượng các nguyên tố có trong hợp chất Fe2O3, SO2, KHCO3
\(M_{Fe_2O_3}=56.2+16.3=160\left(DvC\right)\)
\(\%Fe=\dfrac{56.2}{160}.100\%=70\%\\ \%O=100\%-70\%=30\%\)
\(M_{SO_2}=32+16.2=64\left(DvC\right)\)
\(\%S=\dfrac{32}{64}.100\%=50\%\\ \%O=100\%-50\%=50\%\)
\(M_{KHCO_3}=39+1+12+16.3=100\left(DvC\right)\)
\(\%K=\dfrac{39}{100}.100\%=39\%\\ \%H=\dfrac{1}{100}.100\%=1\%\\ \%C=\dfrac{12}{100}.100\%=12\%\\ \%O=100\%-39\%-1\%-12\%=48\%\)
Đúng 1
Bình luận (1)
Khối lượng của hợp chất Fe2O3 là:
M\(Fe_2O_3\)= 56 . 2 + 16 . 3 = 160
%mFe = \(\dfrac{112.100\%}{160}=70\%\)
%mO = 100% - 70% = 30%
__________________________________________________________________
%mS = \(\dfrac{32.100\%}{64}=50\%\)
%mO = 100 % - 50% = 50%
__________________________________________________________________
%mK = \(\dfrac{39.100\%}{100}=39\%\)
%mH = \(\dfrac{1.100\%}{100}=1\%\)
%mC = \(\dfrac{12.100\%}{100}=12\%\)
%mO = 100% - 39% - 1% - 12% = 48%
Đúng 1
Bình luận (1)
Canxi oxit (CaO) được dùng trong ngành công nghiệp luyện kim, khử chua đất trồng trọt, xử lý nước thải , khử độc môi trường... Hãy xác định thành phần phần trăm (theo khối lượng) của các nguyên tố trong hợp chất đó.
%MCa=\(\dfrac{40}{56}.100=71,42\%\)
%MO=28,58%
Đúng 1
Bình luận (0)
Tính thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong các hợp chất sau: MgO và F e 2 O 3 .