Hai ngtu H trong phân tử H2 làm thế nào để đạt đc cấu hình bền vững
Cl Cl2
O O2
N N2
Chỉ cần giải thick đề thoi ko cần giải, mình ko hiểu đề lắm
Hai ngtu H trong phân tử H2 làm thế nào để đạt đc cấu hình bền vững
...............Cl .....................Cl2
................O...................... O2
................N........................N2
Chỉ cần giải thick đề thoi ko cần giải, mình ko hiểu đề lắm
Mỗi nguyên tử H có 1 e độc thân nên nếu chúng tồn tại 1 mình sẽ không bền vững-->2 nguyên tử H sẽ góp chung với nhau 1 electron độc thân tạo thành cấu hình bền vững hơn
Tương tự với Cl2
Tương tự với Oxi, mỗi nguyên tử có 2 e độc thân-->2 nguyên tử Oxi sẽ góp chung với nhau electron tạo thành cấu hình bền vũng hơn
Mỗi nguyên tử Nito có 3 e độc thân, 2 nguyên tử Nito sẽ liên kết với nhau tạo thành N2 bền vững hơn
N≡N O=O Cl-Cl H-H
những đặc điểm nào về cấu trúc làm cho phân tử ADN có tính bền vững tương đối? tại sao nói tính bền vững trong cấu trúc của adn chỉ có tính chất tương đối?
Những đặc điểm nào về cấu trúc làm cho phân tử ADN có tính bền vững tương đối?
- Những đặ điểm :
+ Trên mỗi mạch đơn, các nucleotit liên kết hóa học vs nhau một cách bền vững
+ Trên mạch kép, các cặp Nu giữa 2 mạch đơn liên kết vs nhau bằng liên kết Hidro. Liên kết Hidro là 1 liên kết kém bền nhưng có số lượng lớn
=> Đảm bảo cho cấu trúc không gian của ADN đc ổn định
Tại sao nói tính bền vững trong cấu trúc của adn chỉ có tính chất tương đối?
- Vì 2 mạch của ADN vẫn phải tách ra để thực hiện quá trình tự sao, tổng hợp mARN (sao mã)
- Vik liên kết H kém bền nên dễ dàng bị đứt -> 2 mạch ADN tách nhau ra thực hiện quá trình như trên
Từ C đến Pb khả năng thu thêm electron để đạt được cấu hình electron bền vững của khí hiếm biến đổi như thế nào?
A. tăng dần
B. giảm dần
C. không đổi
D. không xác định
Từ C đến Pb khả năng thu thêm electron để đạt được cấu hình electron bền vững của khí hiếm biến đổi như thế nào?
A. tăng dần
B. giảm dần
C. không đổi
D. không xác định
Câu 1: Hóa trị của Fe trong hai hợp chất FeCl3, FeCl2 là:
A. I
B. III, II
C. I, III
D. I, II
Câu 2: Cho các kí hiệu và các công thức hóa học: Cl, H, O, C, CO2, Cl2, H2, O2. Dãy gồm các đơn chất là:
A. Cl, H, O, C
B. CO2, Cl2, H2, O2
C. C, Cl2, H2, O2
D. CO2, Cl, H, O2
Câu 3: Các nguyên tử của cùng một nguyên tố hóa học có cùng
A. khối lượng
B. số proton
C. số nơtron
D. cả A, B, C
Câu 4: Công thức hóa học dung để biểu diễn:
A. hợp chất
B. chất
C. đơn chất
D. hỗn hợp
Câu 5: Một kim loại M tạo muối sunfat M2(SO4)3. Muối nitrat của kim loại M là:
A. M(NO3)3
B. M2(NO3)2
C. MNO3
D. M2NO3
Câu 6: Trong nguyên tử luôn có:
A. số proton bằng số nơtron
B. số proton bằng số electron
C. số nowtron bằng số electron
D. số proton bằng số electron bằng số nơtron
II. TỰ LUẬN
Câu 1: Cân bằng các phương trình phản ứng hóa học sau:
Al + S −to→ Al2S3
NaOH + FeCl3 → Fe(OH)3 +NaCl
K + H2O → KOH + H2
Fe + Cl2 −to→ FeCl3
Câu 2: Lập công thức hóa học của các hợp chất hai nguyên tố sau: Ca và O; Al và Cl.
Câu 3: Tính khối lượng mol của các chất sau: H2O, Al2O3, Mg3(PO4)2, Ca(OH)2.
Câu 4: Tính thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong các hợp chất sau: MgO và Fe2O3.
Câu 5:
Tính khối lượng của 4,48 lít khí SO3 (ở đktc).
Tính thể tích ở đktc của 6,4 gam khí CH4.
(Cho biết H=1, O=16, Al=27, Ca=40, P=31, Mg=24, S=32, C=12, Fe=56).
giải thik cho em nhé
Câu 1: Hóa trị của Fe trong hai hợp chất FeCl3, FeCl2 là:
A. I
B. III, II
C. I, III
D. I, II
Câu 2: Cho các kí hiệu và các công thức hóa học: Cl, H, O, C, CO2, Cl2, H2, O2. Dãy gồm các đơn chất là:
A. Cl, H, O, C
B. CO2, Cl2, H2, O2
C. C, Cl2, H2, O2
D. CO2, Cl, H, O2
Câu 3: Các nguyên tử của cùng một nguyên tố hóa học có cùng
A. khối lượng
B. số proton
C. số nơtron
D. cả A, B, C
Câu 4: Công thức hóa học dung để biểu diễn:
A. hợp chất
B. chất
C. đơn chất
D. hỗn hợp
Câu 5: Một kim loại M tạo muối sunfat M2(SO4)3. Muối nitrat của kim loại M là:
A. M(NO3)3
B. M2(NO3)2
C. MNO3
D. M2NO3
Câu 6: Trong nguyên tử luôn có:
A. số proton bằng số nơtron
B. số proton bằng số electron
C. số nowtron bằng số electron
D. số proton bằng số electron bằng số nơtron
Câu 1 :
\(2Al+3S\underrightarrow{^{^{t^0}}}Al_2S_3\)
\(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}FeCl_3\)
Câu 2 : Cái này có sẵn dạng trình bày trong SGk, anh chỉ ghi CT thoi nhé !
\(CaO,AlCl_3,\)
Câu 3 :
\(M_{H_2O}=2+16=18\left(\dfrac{g}{mol}\right)\)
\(M_{Al_2O_3}=24\cdot2+16\cdot3=102\left(\dfrac{g}{mol}\right)\)
\(M_{Mg_3\left(PO_4\right)_2}=24\cdot3+\left(31+64\right)\cdot2=262\left(\dfrac{g}{mol}\right)\)
\(M_{Ca\left(OH\right)_2}=40+17\cdot2=74\left(\dfrac{g}{mol}\right)\)
Câu 4 :
\(MgO:\)
\(M_{MgO}=24+16=40\left(\dfrac{g}{mol}\right)\)
\(\%Mg=\dfrac{24}{40}\cdot100\%=60\%\)
\(\%O=100-60=40\%\)
\(Fe_2O_3:\)
\(M_{Fe_2O_3}=56\cdot2+16\cdot3=160\left(\dfrac{g}{mol}\right)\)
\(\%Fe=\dfrac{2\cdot56}{160}\cdot100\%=70\%\)
\(\)\(\%O=100-70=30\%\)
Câu 5 :
\(n_{SO_3}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(m_{SO_3}=0.2\cdot80=16\left(g\right)\)
\(n_{CH_4}=\dfrac{6.4}{16}=0.4\left(mol\right)\)
\(V_{CH_4}=0.4\cdot22.4=8.96\left(l\right)\)
Khả năng nhận thêm electron để đạt cấu hình bền vững của khí hiếm của các nguyên tố theo chiều từ C đến Pb thay đổi như thế nào ?
A. tăng dần.
B. giảm dần.
C. không đổi.
D. không có quy luật chung.
Từ C đến Pb, khả năng nhận e để đạt cấu hình bền vững của khí hiếm giảm dần, do đó tính phi kim giảm dần
Đáp án B
Khả năng nhận thêm electron để đạt cấu hình bền vững của khí hiếm của các nguyên tố theo chiều từ C đến Pb thay đổi như thế nào ?
A. tăng dần
B. giảm dần
C. không đổi
D. không có quy luật chung
Nếu phân tử ADN có cấu trúc quá bền vững cũng như trong quá trình truyền đạt thông tin di truyền không xảy ra sai sót gì thì thế giới sinh vật có thể vật đa dạng như ngày nay không?
Nếu phân tử ADN quá bền vững thì trong giảm phân rất khó xảy ra sự trao đổi chéo giữa các nhiễm sắc tử không chị em, khó xảy ra sự hoán vị gen tương ứng, rất khó tạo ra các biến dị tổ hợp để cung cấp nguyên liệu phong phú cho chọn lọc tự nhiên.
Nếu quá trình truyền đạt thông tin di truyền không xảy ra sai sót gì thì không tạo ra được các đột biến cung cấp nguyên liệu cho chọn lọc tự nhiên.
Do vậy, sinh giới không thể đa dạng như ngày nay.
Từ Hình 8.2, cho biết mỗi nguyên tử nitrogen đã đạt được cấu hình electron bền vững của nguyên tử khí hiếm nào.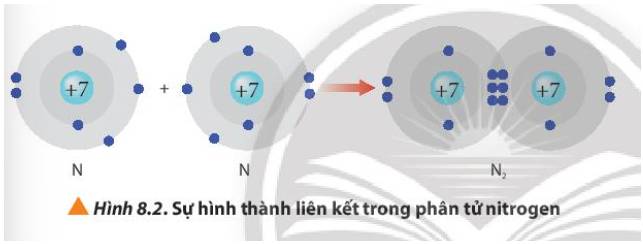
Sau khi tham gia liên kết, nguyên tử nitrogen 8 electron ở lớp ngoài cùng và có 2 lớp electron
=> Đạt được cấu hình electron bền vững của nguyên tử khí hiếm Neon