Cho 11,2 gam kim loại M tác dụng HNO3 thu được 13,44 lít khí NO. Tìm tên kim loại
NH
Những câu hỏi liên quan
Cho 11,2 gam hỗn hợp Cu và kim loại M tác dụng với dung dịch HCl dư thu được 3,136 lít (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch HNO3 loãng thu được 3,92 lít khí NO (đktc, sản phẩm khử duy nhất). Kim loại M là :
A. Mg B. Fe C. Mg hoặc Fe D. Mg hoặc Zn
Gọi số mol Cu, M là a, b (mol)
=> 64a + b.MM = 11,2 (1)
\(n_{NO}=\dfrac{3,92}{22,4}=0,175\left(mol\right)\)
Cu0 - 2e --> Cu+2
a--->2a
M0 - ne --> M+n
b--->bn
N+5 + 3e --> N+2
0,525<-0,175
Bảo toàn e: 2a + bn = 0,525 (2)
(1)(2) => 32bn - bMM = 5,6 (3)
\(n_{H_2}=\dfrac{3,136}{22,4}=0,14\left(mol\right)\)
PTHH: 2M + 2xHCl --> 2MClx + xH2
\(\dfrac{0,28}{x}\)<---------------------0,14
=> \(\dfrac{0,28}{x}=b\) (4)
(3)(4) => MM = 32n - 20x (g/mol)
Và \(0< x\le n\)
TH1: x = n = 1 => MM = 12 (Loại)
TH2: x = n = 2 => MM = 24 (Mg)
TH3: x = n = 3 => MM = 36 (Loại)
TH4: x = 1; n = 2 => MM = 44 (Loại)
TH5: x = 1; n = 3 => MM = 76 (Loại)
TH6: x = 2; n = 3 => MM = 56 (Fe)
Vậy M có thể là Mg hoặc Fe
=> C
Đúng 1
Bình luận (0)
hòa tan hoàn toàn 11,2 gam kim loại M vào dung dịch HNO3 thu được 4,48 lít khí NO . xác định kim lọai M
Cho m gam bột kim loại kẽm hòa tan hết trong dung dịch HNO3, thu được 13,44 lít hỗn hợp ba khí là NO2, NO và N2O. Dẫn lượng khí trên qua dung dịch xút dư, có 11,2 lít hỗn hợp khí thoát ra. Cho lượng khí này trộn với không khí dư (coi không khí chỉ gồm oxi và nitơ) để phản ứng xảy ra hoàn toàn, sau đó cho hấp thụ lượng khí màu nâu thu được vào dung dịch KOH dư, thu được dung dịch D. Dung dịch D làm mất màu vừa đủ 100 ml dung dịch KMnO4 0,4M trong môi trường H2SO4 có dư. Thể tích các khí đo ở đktc...
Đọc tiếp
Cho m gam bột kim loại kẽm hòa tan hết trong dung dịch HNO3, thu được 13,44 lít hỗn hợp ba khí là NO2, NO và N2O. Dẫn lượng khí trên qua dung dịch xút dư, có 11,2 lít hỗn hợp khí thoát ra. Cho lượng khí này trộn với không khí dư (coi không khí chỉ gồm oxi và nitơ) để phản ứng xảy ra hoàn toàn, sau đó cho hấp thụ lượng khí màu nâu thu được vào dung dịch KOH dư, thu được dung dịch D. Dung dịch D làm mất màu vừa đủ 100 ml dung dịch KMnO4 0,4M trong môi trường H2SO4 có dư. Thể tích các khí đo ở đktc. Các phản ứng xảy ra hoàn toàn.
a. Viết phản ứng giữa kẽm với dung dịch HNO3 có hiện diện 3 khí trong phản ứng theo dữ kiện trên.
b. Tính m.
a) \(n_{NO_2}=\dfrac{13,44-11,2}{22,4}=0,1\left(mol\right)\)
Gọi số mol NO là a
\(n_{KMnO_4}=0,1.0,4=0,04\left(mol\right)\)
PTHH: 2NO + O2 --> 2NO2
a------------->a
N+4 -1e--> N+5
a--->a
Mn+7 +5e--> Mn+2
0,04->0,2
Bảo toàn e: a = 0,2 (mol)
=> \(n_{N_2O}=\dfrac{11,2}{22,4}-0,2=0,3\left(mol\right)\)
=> \(n_{NO_2}:n_{NO}:n_{N_2O}=0,1:0,2:0,3=1:2:3\)
31Zn + 80HNO3 --> 31Zn(NO3)2 + 2NO2 + 4NO + 6N2O + 40H2O
b) nZn = 1,55 (mol)
=> mZn = 1,55.65 = 100,75(g)
Đúng 1
Bình luận (0)
Hỗn hợp X gồm Zn và kim loại M. Cho 12,1 gam X tác dụng với dung dịch NaOH dư thu được 2,24 lít khí (đktc) và a gam chất rắn. Mặt khác cho 12,1 gam X tan hoàn toàn trong dung dịch HNO3 đặc, nóng, dư, thu được 11,2 lít khí NO2 (là sản phẩm khử duy nhất, đktc). Tính chất của kim loại M là A. tan được trong dung dịch hỗn hợp Ca(OH)2 và KOH dư. B. không tan được trong dung dịch H2SO4 đặc, nguội. C. tác dụng với clo và dung dịch HCl cho ra cùng một muối. D. tan được trong dung dịch Fe(NO3)2.
Đọc tiếp
Hỗn hợp X gồm Zn và kim loại M. Cho 12,1 gam X tác dụng với dung dịch NaOH dư thu được 2,24 lít khí (đktc) và a gam chất rắn. Mặt khác cho 12,1 gam X tan hoàn toàn trong dung dịch HNO3 đặc, nóng, dư, thu được 11,2 lít khí NO2 (là sản phẩm khử duy nhất, đktc). Tính chất của kim loại M là
A. tan được trong dung dịch hỗn hợp Ca(OH)2 và KOH dư.
B. không tan được trong dung dịch H2SO4 đặc, nguội.
C. tác dụng với clo và dung dịch HCl cho ra cùng một muối.
D. tan được trong dung dịch Fe(NO3)2.
Chọn B.
![]() Þ M không tác dụng được với NaOH.
Þ M không tác dụng được với NaOH.
Từ đó suy ra: ![]()
![]() (với n là hoá trị của M)
(với n là hoá trị của M)
Mà ![]() Từ (1), (2) suy ra M = 56 (Fe)
Từ (1), (2) suy ra M = 56 (Fe)
Vậy tính chất của M là không tan được trong dung dịch H2SO4 đặc, nguội.
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Fe và kim loại M có hóa trị không đổi. Cho 15,2 gam X tác dụng với dung dịch HC1 dư, thấy thoát ra 2,24 lít khí H2 (đktc). Nếu cho lượng X như trên tác dụng với dung dịch HNO3 dư, thu được 4,48 lít khí NO (đktc). Kim loại M là A. Ag. B. Cu. C. Al. D. Mg.
Đọc tiếp
Hỗn hợp X gồm Fe và kim loại M có hóa trị không đổi. Cho 15,2 gam X tác dụng với dung dịch HC1 dư, thấy thoát ra 2,24 lít khí H2 (đktc). Nếu cho lượng X như trên tác dụng với dung dịch HNO3 dư, thu được 4,48 lít khí NO (đktc). Kim loại M là
A. Ag.
B. Cu.
C. Al.
D. Mg.
Đáp án B
n H 2 = 0 , 1 ; n NO = 0 , 4 . Gọi n là hóa trị của M.
Căn cứ vào 4 đáp án ta có 2 trường hợp:
+) M là kim loại đứng trước H trong dãy hoạt động hóa học. Khi đó cả M và Fe có phản ứng với dung dịch HCl. Vì hóa trị của M không đổi nên sự chênh lệch về số electron trao đổi trong hai lần thí nghiệm là do sắt có hai mức hóa trị là II và III.
Áp dụng định luật bảo toàn mol electron:
- Khi hòa tan hỗn hợp vào dung dịch HCl, ta có: 2 n Fe + n . n M = 2 n H 2
- Khi hòa tan hỗn hợp vào dung dịch HNO3, ta có: 3 n Fe + n . n M = 3 n NO
Trừ hai vế của hai phương trình cho nhau, ta được:
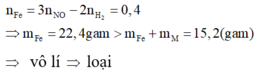
+) M là kim loại đứng sau H và trước Pt trong dãy hoạt động hóa học. Khi đó M không phản ứng được với dung dịch HCl và phản ứng được với dung dịch HNO3. Áp dụng định luật bảo toàn mol electron:
- Khi hòa tan hỗn hợp vào dung dịch HCl, ta có:

Đúng 0
Bình luận (0)
Cho 19,2g kim loại M tác dụng với dung dịch HNO3 loãng dư thu được 4,48 lít khí duy nhất NO (đktc). Kim loại M là
A. Mg.
B. Cu.
C. Fe.
D. Zn.
Gọi n là hóa trị của M
\(M\rightarrow M^{2+}+ne\\ N^{5+}+3e\rightarrow N^{2+}\\ BTe:n_M.n=n_{NO}.3\\ \Rightarrow\dfrac{19,2}{M}.n=0,2.3=0,6\\ \Rightarrow M=32n\\ Chạynghiệm\Rightarrow n=2,M=64\left(tm\right)\)
=> Chọn B
Đúng 3
Bình luận (0)
Cho 11,2 gam kim loại M tác dụng HNO3 thu được 13,44 lít khí NO. Tìm tên kim loại
Cho 11,2 gam hỗn hợp gồm Cu và kim loại M tác dụng hết với HCl dư thu được 3,136 lít khí (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch H2SO4 đặc nóng dư, thu được 5,88 lít khí SO2 (đktc sản phẩm khử duy nhất). Xác định kim loại M và tính % khối lượng Cu trong hỗn hợp
Cho 11,2 gam hỗn hợp gồm Cu và kim loại M tác dụng hết với HCl dư thu được 3,136 lít khí (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch H2SO4 đặc nóng dư, thu được 5,88 lít khí SO2 (đktc sản phẩm khử duy nhất). Xác định kim loại M và tính % khối lượng Cu trong hỗn hợp






