viết cấu hình electron từ 1 đến 30
ZZ
Những câu hỏi liên quan
Viết cấu hình electron nguyên tử các nguyên tố có số electron từ 1 đến 10
Viết cấu hình electron của các nguyên tố có số hiệu nguyên tử từ 1 đến 20.
Z = 1: 1s1
Z = 2: 1s2
Z = 3: 1s22s1
Z = 4: 1s22s2
Z = 5: 1s22s22p1
Z = 6: 1s22s22p2
Z = 7: 1s22s22p3
Z = 8: 1s22s22p4
Z = 9: 1s22s22p5
Z = 10: 1s22s22p6
Z = 11: 1s22s22p63s1
Z = 12: 1s22s22p63s2
Z = 13: 1s22s22p63s23p1
Z = 14: 1s22s22p63s23p2
Z = 15: 1s22s22p63s23p3
Z = 16: 1s22s22p63s23p4
Z = 17: 1s22s22p63s23p5
Z = 18: 1s22s22p63s23p6
Z = 19: 1s22s22p63s23p64s1
Z = 20: 1s22s22p63s23p64s2
Đúng 0
Bình luận (0)
1. Viết cấu hình electron nguyên tử của các nguyên tố (có số hiệu nguyên tử từ 1 đến 20).
\(Z=1\Rightarrow1s^1\)
\(Z=2\Rightarrow1s^2\)
\(Z=3\Rightarrow1s^22s^1\)
\(Z=4\Rightarrow2s^22s^2\)
\(Z=5\Rightarrow1s^22s^22p^1\)
\(Z=6\Rightarrow1s^22s^22p^2\)
\(Z=7\Rightarrow1s^22s^22p^3\)
\(Z=8\Rightarrow1s^22s^22p^4\)
\(Z=8\Rightarrow1s^22s^22p^4\)
\(Z=9\Rightarrow1s^22s^22p^5\)
\(Z=10\Rightarrow1s^22s^22p^6\)
\(Z=11\Rightarrow1s^22s^22p^63s^1\)
Đúng 1
Bình luận (1)
Cấu hình electron của ion được thiết lập bằng cách thêm hoặc bớt electron, bắt đầu từ phân lớp ngoài cùng của cấu hình electron nguyên tử tương ứng. a. Viết cấu hình electron của Na+ và Cl-. b. Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp nào của Cl? AO đó là AO trống, chứa 1 hay 2 electron?
Cấu hình electron của ion được thiết lập bằng cách thêm hoặc bớt electron, bắt đầu từ phân lớp ngoài cùng của cấu hình electron nguyên tử tương ứng.
a) Viết cấu hình electron của Na+ và Cl-.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp nào của Cl? AO đó là AO trống, chứa 1 hay 2 electron?
a) Na (Z = 11) 1s22s22p63s1 ⇒ Na+: 1s22s22p6.
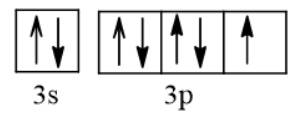
Cl (Z = 17) 1s22s22p63s23p5 ⇒ Cl-: 1s22s22p63s23p6.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp p của Cl. AO đó là AO chứa 1 electron.
Đúng 0
Bình luận (0)
Từ cấu hình e của ion viết cấu hình e của nguyên tử
a. Ion A+, B2+, D3+, X-, Y2-, Z3- đều có cấu hình electron là: 1s22s22p6. Viết cấu hình của A,
B, D, X, Y, Z.
b. Ion A+, B2+, X-, Y2-, Z3- đều có cấu hình electron là: 1s22s22p63s23p6. Viết cấu hình của
A, B, X, Y, Z
Tổng số hạt proton, notron và electron trong nguyên tử của một nguyên tố là 13.
Viết cấu hình electron nguyên tử của nguyên tố đó.
(Cho biết: các nguyên tố có số hiệu nguyên từ từ 2 đến 82 trong bảng tuần hoàn thì)
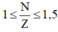
Z = 4 nên có cấu hình electron : 1s22s2.
Đúng 0
Bình luận (0)
Viết cấu hình electron các nguyên tử có Z=1 đến 20, và Z=23,24,25,26,29. Cho biết số E lớp ngoài cùng của mỗi cấu hình. Giúp em với ạ. Em cảm ơn.
Tổng số hạt proton, notron và electron trong nguyên tử của một nguyên tố là 58
a, Xác định nguyên tử khối
b, Viết cấu hình electron nguyên tử của một nguyên tố đó
( Cho biết : Các nguyên tố có số hiệu nguyên tử từ 2 đến 82 trong bảng tuần hoàn thì 1 ≤ N/Z ≤ 1,5 )




