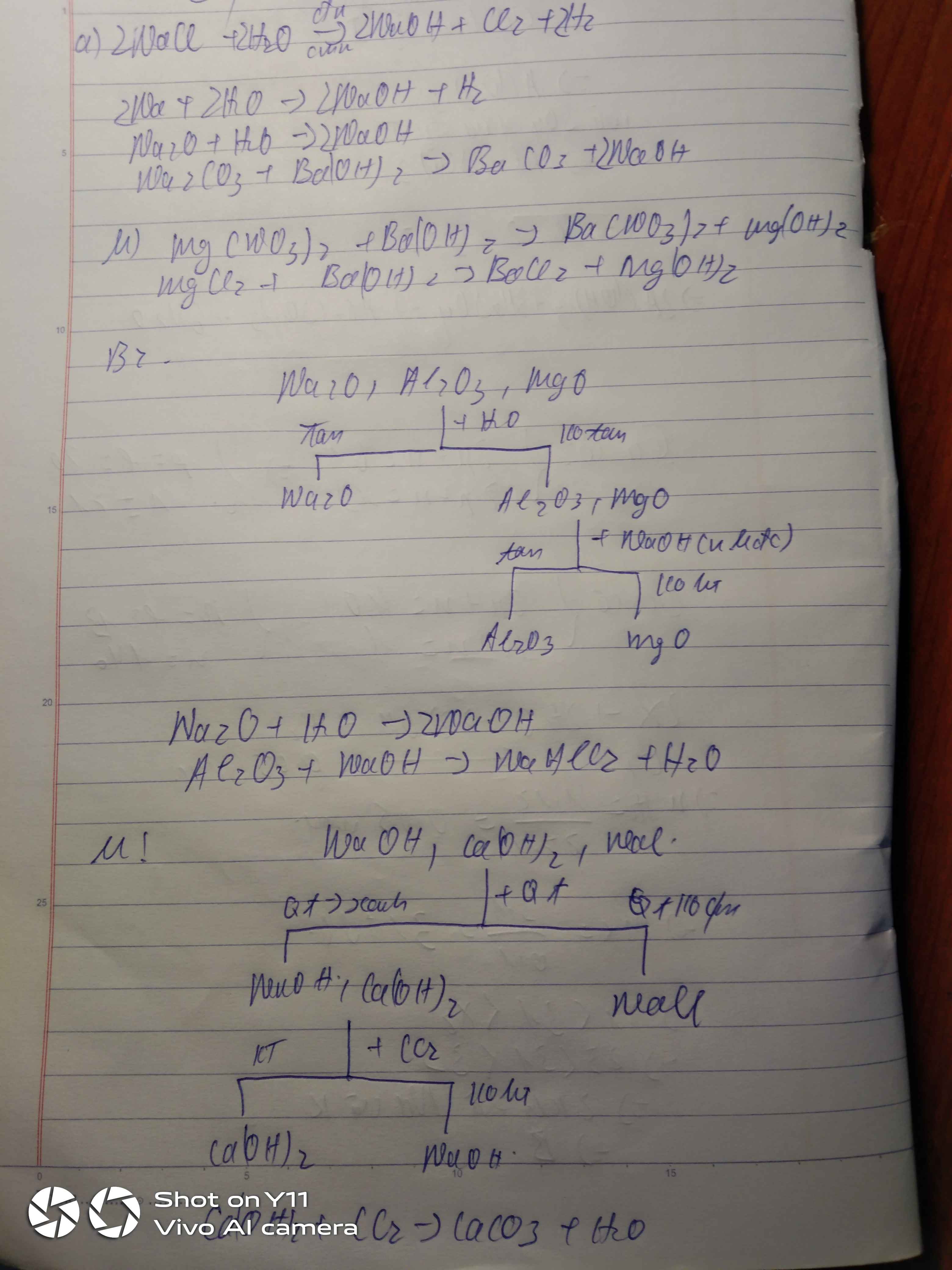Chỉ dùng 2 hóa chất nhận biết 6 chất bột sau: Mg(OH)2, Zn(OH)2, Fe(OH)3, BaCl2, Na2CO3, NaOH
PN
Những câu hỏi liên quan
Phân biệt 6 chất dạng bột : Mg(OH)2 , Zn(OH)2 , Fe(OH)2 , BaCl2 , Na2CO3 , NaOH . Chỉ dùng 1 hoá chất
Chỉ dùng thêm nước và khí CO2, hãy nhận biết các chất rắn đựng trong các lọ riêng biệt sau: Mg(OH)2, Al(OH)3, BaCl2, Na2CO3, NaOH, FeCl2
- Đổ nước vào từng chất sau đó khuấy đều
+) Không tan, tạo kết tủa trắng: Mg(OH)2
+) Không tan, tạo kết tủa keo: Al(OH)3
+) Tan, tạo dd lục nhạt: FeCl2
+) Tan: Các dd còn lại
- Đổ dd FeCl2 vào các dd còn lại
+) Tạo kết tủa trắng: Na2CO3
PTHH: \(FeCl_2+Na_2CO_3\rightarrow2NaCl+FeCO_3\downarrow\)
+) Tạo kết tủa trắng xanh, sau 1 thời gian kết tủa chuyển nâu đỏ: NaOH
PTHH: \(FeCl_2+2NaOH\rightarrow2NaCl+Fe\left(OH\right)_2\downarrow\)
\(4Fe\left(OH\right)_2+O_2+2H_2O\rightarrow4Fe\left(OH\right)_3\)
+) Không hiện tượng: BaCl2
Đúng 0
Bình luận (0)
Nhóm các chất nào sau đây tác dụng với H2SO4 loãng chỉ xảy ra phản ứng trao đổi.
A. Fe , CuO , Cu(OH)2 , BaCl2. B. FeO , Cu(OH)2 , BaCl2 , Na2CO3.
C. Fe2O3 , Cu(OH)2 , Zn , Na2CO3. D. Fe(OH)2 , Mg , CuO , KHCO3.
Nhóm các chất nào sau đây tác dụng với H2SO4 loãng chỉ xảy ra phản ứng trao đổi.
A. Fe , CuO , Cu(OH)2 , BaCl2. B. FeO , Cu(OH)2 , BaCl2 , Na2CO3.
C. Fe2O3 , Cu(OH)2 , Zn , Na2CO3. D. Fe(OH)2 , Mg , CuO , KHCO3.
Đúng 2
Bình luận (0)
Chỉ dùng dd H2SO4 loãng, nhận biết các chất rắn sau:
Cu(OH)2, Ba(OH)2 ,Na2CO3
Hãy nêu phương pháp hóa học để nhận biết bột các kim loại sau:
Al, Fe, Cu.
a)
- Cho các chất rắn tác dụng với dd H2SO4 loãng:
+ Tạo ra dd có màu xanh: Cu(OH)2
\(Cu\left(OH\right)_2+H_2SO_4\rightarrow CuSO_4+2H_2O\)
+ Kết tủa trắng: Ba(OH)2
\(Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4\downarrow+2H_2O\)
+ Có khí thoát ra: Na2CO3
\(Na_2CO_3+H_2SO_4\rightarrow Na_2SO_4+CO_2+H_2O\)
b)
- Hòa tan các kim loại vào dd NaOH dư
+ Kim loại tan: Al
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
+ Kim loại không tan: Fe, Cu
- Hòa tam 2 kim loại còn lại vào dd HCl
+ Kim loại tan: Fe
Fe + 2HCl --> FeCl2 + H2
+ Kim loại không tan: Cu
Đúng 1
Bình luận (0)
Câu 1)
Trích mẫu thử: Cho dung dịch \(H_2SO_4\) vào 3 mẫu thử mẫu nào có kết tủa trắng là \(Ba\left(OH\right)_2\)
Phương trình:
\(Ba\left(OH\right)_2+H_2SO_4\Rightarrow BaSO_4+2H_2O\)
Còn lại: \(Cu\left(OH\right)_2;Na_2CO_3\)
Cho \(Ba\left(OH\right)_2\) vào 2 mẫu thử còn lại: Mẫu nào sinh ra kết tủa trắng là \(Na_2CO_3\)
Phương trình:
\(Na_2CO_3+Ba\left(OH\right)_2\Rightarrow BaCO_3+2NaOH\)
Còn lại là \(Cu\left(OH\right)_2\)
Câu 2)
Lấy mỗi kim loại 1 ít, lần lượt cho vào dd axit loãng HCl vào từng kim loại
Kim loại nào không tan là \(Cu\)
Kim loại nào tan có hiện tượng sủi bọt khí không màu không mùi là \(Al,Fe\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
Cho dd \(NaOH\) vào 2 kim loại còn loại còn lại \(Al,Fe\)
Kim loại nào có hiện tượng sủi bọt khí không màu không mùi là \(Al\) , không có hiện tượng gì là \(Fe\)
\(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
Đúng 0
Bình luận (0)
Bài 1: Nhận biết các dung dịch muối sau chỉ bằng dung dịch H2SO4; NaCl; BaCl2; Ba(HSO3)2; Na2CO3; K2SO3; Na2S. Bài 2: Cho các chất sau: Cu; Ag2O; MgO; Mg(OH)2; Al2O3; Al(OH)3; AlCl3; NaHCO3; CaCO3; Fe(OH)3; CuCl2; Ba(NO3)2; K2SO4; Ca(HCO3)2; FeS; Fe2O3; Fe; NaNO3. Chất nào tác dụng với dung dịch H2SO4 loãng (viết pthh nếu có)
Bài 1: Nhận biết các dung dịch muối sau chỉ bằng dung dịch H2SO4:
H2SO4 + NaCl: Không có phản ứng xảy ra với H2SO4. Dung dịch vẫn trong suốt và không có hiện tượng gì xảy ra.
H2SO4 + BaCl2: Sẽ có kết tủa trắng BaSO4 (sulfat bari) kết tủa xuất hiện. Phản ứng cụ thể là:
H2SO4 + BaCl2 -> BaSO4↓ + 2HCl
H2SO4 + Ba(HSO3)2: Không có phản ứng xảy ra với H2SO4. Dung dịch vẫn trong suốt và không có hiện tượng gì xảy ra.
H2SO4 + Na2CO3: Sẽ có sủi bọt khí CO2 thoát ra và dung dịch trở nên mờ. Phản ứng cụ thể là:
H2SO4 + Na2CO3 -> Na2SO4 + H2O + CO2↑
H2SO4 + K2SO3: Sẽ có sủi bọt khí SO2 thoát ra và dung dịch trở nên mờ. Phản ứng cụ thể là:
H2SO4 + K2SO3 -> K2SO4 + H2O + SO2↑
H2SO4 + Na2S: Sẽ có sủi bọt khí H2S (hydro sulfide) thoát ra và dung dịch trở nên mờ. Phản ứng cụ thể là:
H2SO4 + Na2S -> Na2SO4 + H2S↑
Bài 2: Chất nào tác dụng với dung dịch H2SO4 loãng:
Chất tác động với dung dịch H2SO4 loãng để tạo khí hiđro (H2) sẽ là các chất kim loại. Cụ thể, các chất sau sẽ tác động:
Cu (đồng): Phản ứng sẽ tạo khí hiđro (H2) và ion đồng II (Cu^2+):
Cu + H2SO4 -> CuSO4 + H2↑
MgO (oxit magiê): Phản ứng sẽ tạo magiê sulfat (MgSO4):
MgO + H2SO4 -> MgSO4 + H2O
Mg(OH)2 (hydroxide magiê): Phản ứng sẽ tạo magiê sulfat (MgSO4) và nước:
Mg(OH)2 + H2SO4 -> MgSO4 + 2H2O
Al (nhôm): Phản ứng sẽ tạo khí hiđro (H2) và ion nhôm III (Al^3+):
2Al + 6H2SO4 -> 2Al2(SO4)3 + 6H2↑
Vậy, các chất Cu, MgO, Mg(OH)2, và Al tác động với dung dịch H2SO4 loãng để tạo khí hiđro (H2).
Đúng 0
Bình luận (0)
Cho các chất hóa học sau:
CaO, HCl, K2SO4, Na(OH), FeSO4, Fe(OH)3, MgO, Mg(OH)2, MgCl2, BaCl2, HNO3, KNO3, K2O, Zn(OH)2, ZnO, H2SO4, BaSO4, Al2(SO4)3, Al(OH)3
a) Hãy phân biệt các hóa chất trên
b) Gọi tên các hóa chất đó
2. Viết phương trình của các tính chất hóa học: Oxit, Axit, Bazo, muối
3. Cho 8gam dung dịch NạO phản ứng hoàn toàn với CO2, phản ứng tạo ra muối Na2CO3
a) Viết phương trình phản ứng
b) Tính thể tích CO2( ở điều kiện tiêu chuẩn)
c) Tính khối lượng muối Na2CO3
Giúp mik với ạ, mi...
Đọc tiếp
Cho các chất hóa học sau: CaO, HCl, K2SO4, Na(OH), FeSO4, Fe(OH)3, MgO, Mg(OH)2, MgCl2, BaCl2, HNO3, KNO3, K2O, Zn(OH)2, ZnO, H2SO4, BaSO4, Al2(SO4)3, Al(OH)3 a) Hãy phân biệt các hóa chất trên b) Gọi tên các hóa chất đó 2. Viết phương trình của các tính chất hóa học: Oxit, Axit, Bazo, muối 3. Cho 8gam dung dịch NạO phản ứng hoàn toàn với CO2, phản ứng tạo ra muối Na2CO3 a) Viết phương trình phản ứng b) Tính thể tích CO2( ở điều kiện tiêu chuẩn) c) Tính khối lượng muối Na2CO3 Giúp mik với ạ, mik cần gấp lắm ạ
Bài 1. Nêu các phản ứng điều chếa) NaOH từ các hoá chất: Na, Na2O, Na2CO3, Ba(OH)2, NaCl, H2Ob) Mg(OH)2 từ các hoá chất: Mg, Mg(NO3)2, MgCl2, HCl, Ba(OH)2 Bài 2. Phân biệt nhận biết chấta) Chỉ dùng H2O hãy trình bày cách phân biệt 3 chất rắn: Na2O, Al2O3, MgOb) 3 dd trong suốt có trong 3 lọ riêng biệt: NaOH, Ca(OH)2, NaClc) Chỉ dùng quỳ tím hãy phân biệt 4 dd trong suốt: Ba(OH)2, NaOH, NaCl, Na2SO4 Bài 3. Cho 6,2 gam Na2O vào ước dư để thu được 200 ml dd A.a) Xác đinh nồng độ mol của dd A...
Đọc tiếp
Bài 1. Nêu các phản ứng điều chế
a) NaOH từ các hoá chất: Na, Na2O, Na2CO3, Ba(OH)2, NaCl, H2O
b) Mg(OH)2 từ các hoá chất: Mg, Mg(NO3)2, MgCl2, HCl, Ba(OH)2
Bài 2. Phân biệt nhận biết chất
a) Chỉ dùng H2O hãy trình bày cách phân biệt 3 chất rắn: Na2O, Al2O3, MgO
b) 3 dd trong suốt có trong 3 lọ riêng biệt: NaOH, Ca(OH)2, NaCl
c) Chỉ dùng quỳ tím hãy phân biệt 4 dd trong suốt: Ba(OH)2, NaOH, NaCl, Na2SO4
Bài 3. Cho 6,2 gam Na2O vào ước dư để thu được 200 ml dd A.
a) Xác đinh nồng độ mol của dd A.
b) Cần lấy bao nhiêu ml dd H2SO41M để trung hoà vừa hết dd A?
c) Cần lấy bao nhiêu gam dd HCl 7,3% để trung hoà vừa hết dd A?
Bài 1. Nêu các phản ứng điều chếa) NaOH từ các hoá chất: Na, Na2O, Na2CO3, Ba(OH)2, NaCl, H2Ob) Mg(OH)2 từ các hoá chất: Mg, Mg(NO3)2, MgCl2, HCl, Ba(OH)2 Bài 2. Phân biệt nhận biết chấta) Chỉ dùng H2O hãy trình bày cách phân biệt 3 chất rắn: Na2O, Al2O3, MgOb) 3 dd trong suốt có trong 3 lọ riêng biệt: NaOH, Ca(OH)2, NaClc) Chỉ dùng quỳ tím hãy phân biệt 4 dd trong suốt: Ba(OH)2, NaOH, NaCl, Na2SO4 Bài 3. Cho 6,2 gam Na2O vào ước dư để thu được 200 ml dd A.a) Xác đinh nồng độ mol của dd A...
Đọc tiếp
Bài 1. Nêu các phản ứng điều chế
a) NaOH từ các hoá chất: Na, Na2O, Na2CO3, Ba(OH)2, NaCl, H2O
b) Mg(OH)2 từ các hoá chất: Mg, Mg(NO3)2, MgCl2, HCl, Ba(OH)2
Bài 2. Phân biệt nhận biết chất
a) Chỉ dùng H2O hãy trình bày cách phân biệt 3 chất rắn: Na2O, Al2O3, MgO
b) 3 dd trong suốt có trong 3 lọ riêng biệt: NaOH, Ca(OH)2, NaCl
c) Chỉ dùng quỳ tím hãy phân biệt 4 dd trong suốt: Ba(OH)2, NaOH, NaCl, Na2SO4
Bài 3. Cho 6,2 gam Na2O vào ước dư để thu được 200 ml dd A.
a) Xác đinh nồng độ mol của dd A.
b) Cần lấy bao nhiêu ml dd H2SO41M để trung hoà vừa hết dd A?
c) Cần lấy bao nhiêu gam dd HCl 7,3% để trung hoà vừa hết dd A?
Chất nào sau đây là chất kiềm?
A. NaOH, KOH, Ba(OH)2.
B. Ca(OH)2, Fe(OH)2, KOH.
C. Cu(OH)2, Zn(OH)2, Fe(OH)3.
D. Mg(OH)2, NaOH, Al(OH)3.
Chọn câu A nha em, vì kiềm thường sẽ nói là những bazo , những chất có tan trong nước.
B loại Fe(OH)2, C loại tất cả , D loại Mg(OH)2 và Al(OH)3
Đúng 3
Bình luận (0)
Chất bào sau đây là chất kiềm ?
A NaOH , KOH , Ba(OH)2
B Ca(OH)2 , Fe(OH)2 , KOH
C Cu(OH)2 , Zn(OH)2 , Fe(OH)3
D Mg(OH)2 , NaOH , Al(OH)3
Chúc bạn học tốt
Đúng 2
Bình luận (0)