Nêu phương pháp nhận biết 4 dung dịch sau: Mg(NO3)2, Cu(NO3)2, HNO3 và Fe(NO3)3
MT
Những câu hỏi liên quan
hòa tan hoàn toàn 3,37g hỗn hợp Cu,Fe,Mg,Al trong dung dịch HNO3 dư thu được m gam hỗn hợp các muối sau Cu(NO3)2,Fe(NO3)3,Mg(NO3)2,Al(NO3)3 và 616 ml khí N2O là sản phẩm khử duy nhất của N(+5).tìm giá trị m
nN2O = \(\dfrac{0,616}{22,4}\)= 0,0275 mol
2N+5 + 8e --> N2+1
0,22<------- 0,0275
nNO3- tạo muối = ne trao đổi = 0,22 mol
=> mNO3- tạo muối = 0,22.62 = 13,64 gam
mMuối = mKL + mNO3- = 3,37 + 13,64 = 17,01 gam
Đúng 2
Bình luận (0)
Cho hỗn hợp gồm Fe và Mg vào dung dịch AgNO3, khi cá phản ứng xảy ra hoàn toàn thu được dung dịch X (gồm ba muối) và chất rắn Y là một kim loại. Có các nhận định sau: (a) Dung dịch X chứa: Fe(NO3)3, Mg(NO3)2 và Fe(NO3)2. (b) Dung dịch X chứa: Fe(NO3)3, AgNO3 và Fe(NO3)2. (c) Dung dịch X chứa: AgNO3, Mg(NO3)2 và Fe(NO3)2. (d) Dung dịch X chứa: Fe(NO3)3, Mg(NO3)2 và AgNO3. Số nhận định đúng là A. 3. B. 4. C. 1. D. 2.
Đọc tiếp
Cho hỗn hợp gồm Fe và Mg vào dung dịch AgNO3, khi cá phản ứng xảy ra hoàn toàn thu được dung dịch X (gồm ba muối) và chất rắn Y là một kim loại. Có các nhận định sau:
(a) Dung dịch X chứa: Fe(NO3)3, Mg(NO3)2 và Fe(NO3)2.
(b) Dung dịch X chứa: Fe(NO3)3, AgNO3 và Fe(NO3)2.
(c) Dung dịch X chứa: AgNO3, Mg(NO3)2 và Fe(NO3)2.
(d) Dung dịch X chứa: Fe(NO3)3, Mg(NO3)2 và AgNO3.
Số nhận định đúng là
A. 3.
B. 4.
C. 1.
D. 2.
Đáp án D
Phương pháp: Dựa vào dãy điện hóa (quy tắc α)
Hướng dẫn giải:
Kim loại thu được là Ag. Do thu được 1 KL nên Fe, Mg hết.
Thứ tự các kim loại phản ứng với AgNO 3 : Mg, Fe
TH1:
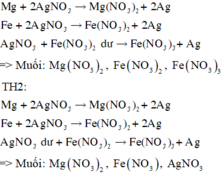
Đúng 0
Bình luận (0)
Làm sạch chất có lẫn tạp chất bằng phương pháp hóa học
a. Dung dịch AlCl3 có lẫn tạp chất CuCl2.
b. Bột Ag có lẫn bột Mg và Cu.
c. Bột Fe có lẫn bột Al
d. Cu có lân Fe và Al
e. Dung dịch Al(NO3)3 có lẫn tạp chất Cu(NO3)2.và Fe(NO3)2
a) Cho Al tác dụng với dd, lọc bỏ rắn không tan thu được dd AlCl3
2Al + 3CuCl2 --> 2AlCl3 + 3Cu
b) Đốt cháy hỗn hợp trong O2 dư, hòa tan sản phẩm thu được vào dd HCl, lọc lấy phần rắn không tan là Ag
2Mg + O2 --to--> 2MgO
2Cu + O2 --to--> 2CuO
MgO + 2HCl --> MgCl2 + H2O
CuO + 2HCl --> CuCl2 + H2O
c) Hòa tan hỗn hợp rắn vào dd NaOH, lọc lấy phần rắn không tan là Fe
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
d) Hòa tan hỗn hợp rắn vào dd HCl, lọc lấy phần rắn không tan là Cu
Fe + 2HCl --> FeCl2 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
e) Cho Al tác dụng với dd, lọc bỏ phần rắn không tan thu được dung dịch Al(NO3)3
2Al + 3Cu(NO3)2 --> 2Al(NO3)3 + 3Cu
2Al + 3Fe(NO3)2 --> 2Al(NO3)3 + 3Fe
Đúng 1
Bình luận (0)
Cu + H2SO4 đ -> CuSO4 + SO2 + H2O
Fe + H2SO4 đ -> Fe2(SO4)3 + SO2 + H2O
Al + H2SO4 đ -> Al2(SO4)3 + SO2 + H2O
Cu + HNO3 -> Cu(NO3)2 + NO2 + H2O
Cu + HNO3 -> Cu(NO3)2 + NO + H2O
Cu + HNO3 -> Cu(NO3)2 + N2O + H2O
Cu + HNO3 -> Cu(NO3)2 + N2 + H2O
Mg + HNO3 -> Mg(NO3)2 + N2H4O3 + H2O
Fe + HNO3 -> Fe(NO3)3 + NO2 + H2O
Fe + HNO3 -> Fe(NO3)3 + NO + H2O
Cu + 2H2SO4 đ -> CuSO4 + SO2 + 2H2O
2Fe + 6H2SO4 đ -> Fe2(SO4)3 + 3SO2 + 6H2O
2Al + 6H2SO4 đ -> Al2(SO4)3 + 3SO2 + 6H2O
Cu + 4HNO3 -> Cu(NO3)2 + 2NO2 + 2H2O
3Cu + 8HNO3 -> 3Cu(NO3)2 + 2NO + 4H2O
4Cu + 10HNO3 -> 4Cu(NO3)2 + N2O + 5H2O
5Cu + 12HNO3 -> 5Cu(NO3)2 + N2 + 6H2O
4Mg + 10HNO3 -> 4Mg(NO3)2 + N2H4O3 + 3H2O
Fe + 6HNO3 -> Fe(NO3)3 + 3NO2 + 3H2O
Fe + 4HNO3 -> Fe(NO3)3 + NO + 2H2O
Đúng 0
Bình luận (0)
Giải:
Cu + 2H2SO4 đ -> CuSO4 + SO2 + 2H2O
2Fe + 6H2SO4 đ -> Fe2(SO4)3 + 3SO2 + 6H2O
2Al + 6H2SO4 đ -> Al2(SO4)3 + 3SO2 + 6H2O
Cu + 4HNO3 -> Cu(NO3)2 + 2NO2 + 2H2O
3Cu + 8HNO3 -> 3Cu(NO3)2 + 2NO + 4H2O
4Cu + 10HNO3 -> 4Cu(NO3)2 + N2O + 5H2O
5Cu + 12HNO3 -> 5Cu(NO3)2 + N2 + 6H2O
4Mg + 10HNO3 -> 4Mg(NO3)2 + N2H4O3 + 3H2O
Fe + 6HNO3 -> Fe(NO3)3 + 3NO2 + 3H2O
Fe + 4HNO3 -> Fe(NO3)3 + NO + 2H2O
Bạn đếm lại nha, mình cân bằng chưa kịp đếm.
Đúng 0
Bình luận (0)
Cu + 2H2SO4 đ -> CuSO4 + SO2 + 2H2O
2Fe + 6H2SO4 đ -> Fe2(SO4)3 + 3SO2 + 6H2O
2Al + 6H2SO4 đ -> Al2(SO4)3 + 3SO2 + 6H2O
Cu + 4HNO3 -> Cu(NO3)2 + 2NO2 + 2H2O
3Cu + 8HNO3 -> 3Cu(NO3)2 + 2NO + 4H2O
4Cu + 10HNO3 -> 4Cu(NO3)2 + N2O + 5H2O
5Cu + 12HNO3 -> 5Cu(NO3)2 + N2 + 6H2O
4Mg + 10HNO3 -> 4Mg(NO3)2 + N2H4O3 + 3H2O
Fe + 6HNO3 -> Fe(NO3)3 + 3NO2 + 3H2O
Fe + 4HNO3 -> Fe(NO3)3 + NO + 2H2O
Đúng 0
Bình luận (0)
Câu 3: Bằng phương pháp hoá học hãy nhận biết các lọ không nhãn chứa các dung dịch hoá chất sau: Al(NO3)3 , Zn(NO3)2 , NaNO3 , Mg(NO3)2 . Viết các phương trình phản ứng
- Cho các dd tác dụng với dd NaOH dư:
+ Xuất hiện kết tủa trắng, không tan: Mg(NO3)2
\(Mg\left(NO_3\right)_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaNO_3\)
+ Xuất hiện kết tủa trắng, lượng kết tủa tăng dần đến cực đại rồi tan trong dd: Al(NO3)3, Zn(NO3)2 (1)
\(Al\left(NO_3\right)_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaNO_3\)
\(Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+2H_2O\)
\(Zn\left(NO_3\right)_2+2NaOH\rightarrow Zn\left(OH\right)_2\downarrow+2NaNO_3\)
\(Zn\left(OH\right)_2+2NaOH\rightarrow Na_2ZnO_2+2H_2O\)
+ Không hiện tượng: NaNO3
- Cho các dd ở (1) tác dụng với dd NH3 dư:
+ Xuất hiện kết tủa trắng, không tan: Al(NO3)3
\(Al\left(NO_3\right)_3+3NH_3+3H_2O\rightarrow Al\left(OH\right)_3\downarrow+3NH_4NO_3\)
+ Xuất hiện kết tủa trắng, sau đó kết tủa tan dần trong dd: Zn(NO3)2
\(Zn\left(NO_3\right)_2+2NH_3+2H_2O\rightarrow Zn\left(OH\right)_2\downarrow+2NH_4NO_3\)
\(Zn\left(OH\right)_2+NH_3\rightarrow\left[Zn\left(NH_3\right)_4\right]\left(OH\right)_2\)
Đúng 1
Bình luận (0)
Cho Cu tác dụng với các dung dịch sau: HNO3, HCl, AgNO3, Fe(NO3)2,Fe(NO3)3, Na2S. Số dung dịch Cu phản ứng được là:
A. 2
B. 3
C. 4
D. 5
Đáp án: B
3Cu + 8HNO3→ 3Cu(NO3)2 +2NO +4H2O
Cu + 2AgNO3→ Cu(NO3)2 + 2Ag
Cu + 2Fe(NO3)3 → 2Fe(NO3)2+Cu(NO3)2
Đúng 0
Bình luận (0)
Thuốc thử duy nhất dùng để nhận biết NH4NO3, NaNO3, Al(NO3)3, Mg(NO3)2, Fe(NO3)2, Fe(NO3)3, và Cu(NO3)2 là: A.NaAlO2 B.Na2CO3 C.NaCl D.NaOH
Đọc tiếp
Thuốc thử duy nhất dùng để nhận biết NH4NO3, NaNO3, Al(NO3)3, Mg(NO3)2, Fe(NO3)2, Fe(NO3)3, và Cu(NO3)2 là:
A.NaAlO2
B.Na2CO3
C.NaCl
D.NaOH
Chọn D
Với NH4NO3 có khí mùi khai thoát ra
Với Al(NO3)3 có kết tủa sau đó tan
Với NaNO3 không có hiện tượng
Với Fe(NO3)3 có kết tủa màu đỏ nâu xuất hiện
Dùng NH3 để nhận ra Cu(NO3)2
Để kết tủa Fe(OH)2 ngoài không khí hoá nâu đỏ để nhận ra Fe(NO3)2
Đúng 0
Bình luận (0)
Câu 4: Hãy nhận biết các lọ hoá chất mất nhãn sau đây bằng phương pháp hoá học: NaCl, Mg(NO3)2 , Cu(NO3)2 , Al2(SO4)3
- Trích một ít các dd làm mẫu thử;
- Cho các dd tác dụng với dd NaOH dư:
+ Không hiện tượng: NaCl
+ Xuất hiện kết tủa xanh: Cu(NO3)2
\(Cu\left(NO_3\right)_2+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow+2NaNO_3\)
+ Xuất hiện kết tủa trắng, không tan: Mg(NO3)2
\(Mg\left(NO_3\right)_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaNO_3\)
+ Xuất hiện kết tủa trắng, lương kết tủa tăng dần đến cực đại rồi tan trong dd: Al2(SO4)3
\(Al_2\left(SO_4\right)_3+6NaOH\rightarrow2Al\left(OH\right)_3\downarrow+3Na_2SO_4\)
\(Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+2H_2O\)
Đúng 1
Bình luận (0)
chỉ dùng 1 thuốc thử nhận biết các dd đựng trong lọ riêng biệt sau: Cu(NO3)2 , Fe(NO3)2,Fe(NO3)3, NH4NO3, AgNO3, NaNO3, Al(NO3)3, Mg(NO3)2
Cho dung dịch NaOH lần lượt vào từng mẫu thử :
- Kết tủa xanh lam : Cu(OH)2
- Kết tủa trắng xanh sau đó hóa nâu đỏ trong không khí : Fe(NO3)2
- Kết tủa nâu đỏ : Fe(NO3)3
- Sủi bọt khí mùi khai : NH4NO3
- Kết tủa đen : AgNO3
- Kết tủa keo trắng , tan dần trong NaOH dư : Al(NO3)3
- Kết tủa trắng bền : Mg(NO3)2
- Không hiện tượng : NaNO3
PTHH em tự viết nhé !
Đúng 7
Bình luận (0)



