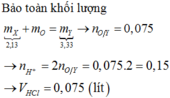Cho 5,26g hỗn hợp kim loại ở dạng bột là; Mg, Al, Cu cháy hoàn toàn trong khí õi, thu được 8,70g hỗn hợp oxit. Hỏi để hòa tan hết lượng hỗn hợp oxit đó cần dùng ít nhất bao nhiêu g axit HCl
LB
Những câu hỏi liên quan
Cho 12g hỗn hợp 2 kim loại dạng bột là Fe và Cu tác dụng với 200ml dung dịch H₂SO₄ 2M thì thu đc 2,24 lít khí hidro ở đktc, dung dịch B và m gam chất ko tan.
a) Tính khối lượng mỗi kim loại trong hỗn hợp và xác định m.
b) Tính nồng độ mol của các chất sau phản ứng.(Coi thể tích dung dịch thay đổi ko đáng kể)
a, \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
\(\Rightarrow m=m_{Cu}=12-5,6=6,4\left(g\right)\)
b, \(n_{FeSO_4}=n_{H_2SO_4\left(pư\right)}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,2.2-0,1=0,3\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{FeSO_4}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\\C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Cho 2,08g hỗn hợp hai dạng oxit dạng bột là \(CuO\) và \(Fe_2O_3\). Dùng V lít (đktc) khí CO để khử hoàn toàn hai oxit trên thành kim loại thì thu được 1,464g hỗn hợp hai kim loại
a) Viết PTPƯ xảy ra
b) Xác định V tối thiểu cần dùng
a)
$CuO + CO \xrightarrow{t^o} Cu + CO_2$
$Fe_2O_3 + 3CO \xrightarrow{t^o}2Fe + 3CO_2$
b)
Gọi $n_{CO_2} = n_{CO} = a(mol)$
Bảo toàn khối lượng :
$2,08 + 28a = 1,464 + 44a$
$\Rightarrow a = 0,0385(mol)$
$V = 0,0385.22,4 = 0,8624(lít)$
Đúng 3
Bình luận (1)
Cho 2,13 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 3,33 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là A. 57 ml B. 50 ml C. 75 ml D. 90 ml
Đọc tiếp
Cho 2,13 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 3,33 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là
A. 57 ml
B. 50 ml
C. 75 ml
D. 90 ml
Chọn đáp án C
n H C l = 2 n O o x i t = 2 3 , 33 - 2 , 13 16 = 0,15 (mol)
→ V d d H C l = 0 , 15 0 , 2 = 0,075 (lít)
Đúng 0
Bình luận (0)
Cho 4,26 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 6,66 gam. Thể tích dung dịch H2SO4 1M vừa đủ để phản ứng hết với Y là A. 75 ml B. 150 ml C. 55 ml D. 90 ml
Đọc tiếp
Cho 4,26 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 6,66 gam. Thể tích dung dịch H2SO4 1M vừa đủ để phản ứng hết với Y là
A. 75 ml
B. 150 ml
C. 55 ml
D. 90 ml
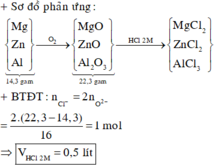
Cho 14,3 gam hỗn hợp X gồm ba kim loại Mg, Zn và Al ở dạng bột tác dụng hoàn toàn với oxi, thu được hỗn hợp Y gồm các oxit có khối lượng 22,3 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là A. 2,0 lít. B. 1,0 lít. C. 0,5 lít. D. 1,5 lít.
Đọc tiếp
Cho 14,3 gam hỗn hợp X gồm ba kim loại Mg, Zn và Al ở dạng bột tác dụng hoàn toàn với oxi, thu được hỗn hợp Y gồm các oxit có khối lượng 22,3 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là
A. 2,0 lít.
B. 1,0 lít.
C. 0,5 lít.
D. 1,5 lít.
Cho 2,13 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 3,33 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là A. 57 ml. B. 50 ml. C. 75 ml D. 90 ml
Đọc tiếp
Cho 2,13 gam hỗn hợp X gồm ba kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 3,33 gam. Thể tích dung dịch HCl 2M vừa đủ để phản ứng hết với Y là
A. 57 ml.
B. 50 ml.
C. 75 ml
D. 90 ml
Cho 2,13 gam hỗn hợp X gồm 3 kim loại Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khôi lượng 3,33 gam. Thể tích dung dịch HCL 2M vừa đủ để phản ứng hết với Y là
tham khảo
Bảo toàn khối lượng:
m kim loại+ mO2= moxit
=> mO2= 3.33-2.13=1.2g
=> nO2= 1.2/32=0.0375mol
=>nO=0.075mol
mà cứ 1O + 2H+ = 1H2O
=> 0.075mol 0.15mol
vậy nH+ cần dùng là 0.15mol
mà CM=n / V => V= n / CM = 0.15 / 2 = 0.075l =75ml
Đúng 1
Bình luận (0)
cho 2,08 g hỗn hợp hai ôxit dạng bột là CuO và sắt(3) ôxit .dùng khí CO để khử hoàn toàn hai ôxit thu được 1,4 g hỗn hợp hai kim loại. xác định thành phần phần trăm của mỗi ôxit ,mỗi kim loại trong hỗn hợp thu được.
bài này khó thật
cố gắng giúp mình nhé
a. PT : CuO+CO−−>Cu+CO2CuO+CO−−>Cu+CO2
Fe2O3+3CO−−>2Fe+3CO2Fe2O3+3CO−−>2Fe+3CO2
b. gọi a, b lần lượt là số mol CuOvàFe2O3phảnứngCuOvàFe2O3phảnứng
ta có hệ: 80a + 160b=2.08
64a+56*2b=1.464
=>a=....... b=......
=>V=............
Cho 5,12 gam hỗn hợp 2 kim loại ở dạng bột Mg và Cu tác dụng hoàn toàn với oxi thu được 7,2 g hỗn hợp oxit hỏi để hòa tan hết lượng hỗn hợp oxit đó cần dùng ít nhất bao nhiêu ml dung dịch H2 SO4 1,25M
- Gọi số mol Mg và Cu trong hỗn hợp là x và y mol .
\(PTKL:24x+64y=5,12\)
\(m_{oxit}=m_{MgO}+m_{CuO}=40x+80y=7,2\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,08\\y=0,05\end{matrix}\right.\) ( mol )
\(\Rightarrow n_{H2O}=n_{MgO}+n_{CuO}=0,13\left(mol\right)\)
\(BTNT\left(H\right):n_{H2SO4}=n_{H2O}=0,13\left(mol\right)\)
\(\Rightarrow V=0,104l=104ml\)
Đúng 1
Bình luận (2)