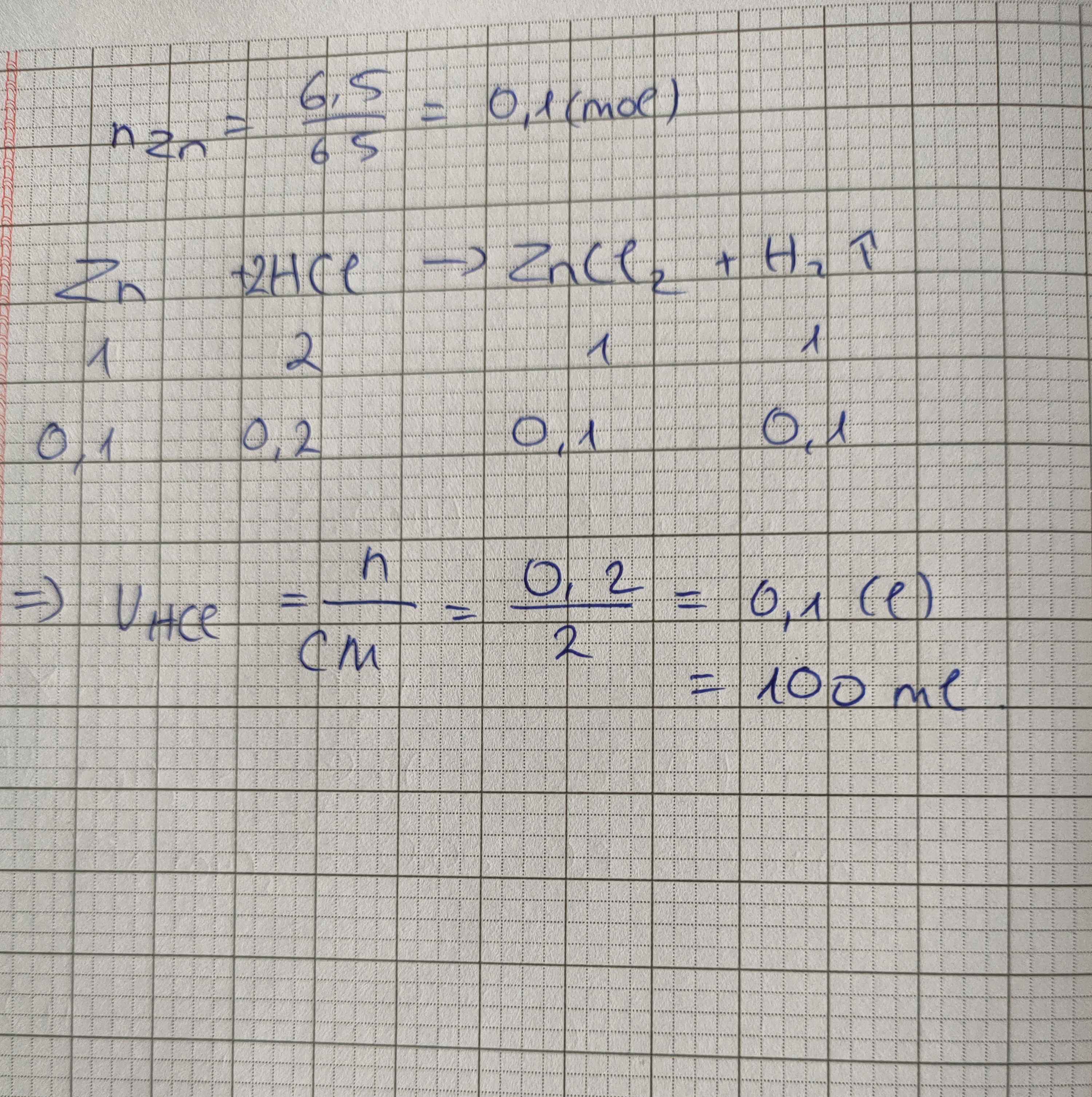Cần dùng bao nhiêu ml nước trộn vói bao nhiêu ml HCl để đc 500ml dung dịch HCl 1,4M
LN
Những câu hỏi liên quan
Câu 2: Trộn 200 ml dung dịch HCl 1M với 300 ml dung dịch HCl 1,5 M thu được dung dịch HCl có nồng độ mol/lit là bao nhiêu?
Câu 3: Cần thêm bao nhiêu ml H2O (D = 1 g/ml) vào 100 gam dung dịch NaOH 35% để thu được dung dịch NaOH 20%.
Câu 4: Cần pha bao nhiêu lít dung dịch HCl 2M với bao nhiêu lít dung dịch HCl 3M để thu được 4 lít dung dịch HCl 2,75M.
Câu 2 :
$n_{HCl} = 0,2.1 + 0,3.1,5 = 0,65(mol)$
$V_{dd} = 0,2 + 0,3 = 0,5(mol)$
$C_{M_{HCl}} = \dfrac{0,65}{0,5} =1,3M$
Câu 3 :
Gọi $m_{H_2O\ cần\ thêm} =a (gam)$
Sau khi thêm :
$m_{NaOH} = 100.35\% = 35(gam)$
$m_{dd} = 100 + a(gam)$
Suy ra: $\dfrac{35}{100 + a}.100\% = 20\%$
Suy ra: a = 75(gam)
Câu 4 :
Gọi $V_{dd\ HCl\ 2M} =a (lít) ; V_{dd\ HCl\ 3M} = b(lít)$
Ta có :
$a + b = 4$
$2a + 3b = 4.2,75$
Suy ra a = 1(lít) ; b = 3(lít)
Đúng 2
Bình luận (0)
Cần bao nhiêu ml dung dịch HCl 2M trộn với 180 ml dung dịch H2SO4 3M để được một dung dịch có nồng độ mol của H+ là 4,5M?
A. 108
B. 216
C. 324
D. 54
Đáp án A
Gọi thể tích dung dịch HCl cần dùng là V lít
Ta có nH+= 2V + 0,18.3.2= 2V + 1,08 (mol)
Vdung dịch= V + 0,18 (lít)
CM H+= nH+/ Vdung dịch= (2V+ 1,08)/ (V+ 0,18)= 4,5 (M)
Giải PT ra V= 0,108 lít
Đúng 0
Bình luận (0)
Để hoà tan hoàn toàn 500ml dung dịch gồm Naoh 0.5M và Ba(oh)2 0.2M thì cần dùng bao nhiêu ml dung dịch góm Hcl 0.6M và H2SO4 0.3 M
Để hoà tan hoàn toàn 500ml dung dịch gồm Naoh 0.5M và Ba(oh)2 0.2M thì cần dùng bao nhiêu ml dung dịch góm Hcl 0.6M và H2SO4 0.3 M
Bài 5.1. Tìm tỉ lệ thể tích của dung dịch HCl 18,25% (D 1,2g/ml) và thể tích của dung dịch HCl 13% (D 1,123g/ml) để pha thành dung dịch HCl 4,5M ?2. Cần trộn bao nhiêu gam tinh thể Na2CO3.6H2O vào 263,6 g dung dịch Na2CO3 bão hòa (ở nhiệt độ xác định) có độ tan bằng 31,8g để thu được dung dịch Na2CO3 34,13%.
Đọc tiếp
Bài 5.
1. Tìm tỉ lệ thể tích của dung dịch HCl 18,25% (D = 1,2g/ml) và thể tích của dung dịch HCl 13% (D = 1,123g/ml) để pha thành dung dịch HCl 4,5M ?
2. Cần trộn bao nhiêu gam tinh thể Na2CO3.6H2O vào 263,6 g dung dịch Na2CO3 bão hòa (ở nhiệt độ xác định) có độ tan bằng 31,8g để thu được dung dịch Na2CO3 34,13%.
1) Gọi dd HCl 18,25% là dd HCl (1)
Gọi dd HCl 13% là dd HCl (2)
Giả sử trộn a lít dd HCl (1) với b lít dd HCl (2) để thành dd HCl 4,5M
\(m_{dd.HCl.\left(1\right)}=1,2.1000a=1200a\left(g\right)\)
=> \(n_{HCl.trong.dd.\left(1\right)}=\dfrac{1200a.18,25\%}{36,5}=6a\left(mol\right)\)
\(m_{dd.HCl.\left(2\right)}=1,123.1000b=1123b\left(g\right)\)
=> \(n_{HCl.trong.dd.\left(2\right)}=\dfrac{1123b.13\%}{36,5}=4b\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=6a+4b\left(mol\right)\)
Vdd sau khi pha = a + b (l)
=> \(C_M=\dfrac{6a+4b}{a+b}=4,5M\)
=> 6a + 4b = 4,5a + 4,5b
=> 1,5a = 0,5b
=> a : b = 1 : 3
2)
Gọi khối lượng Na2CO3 trong dd bão hòa là a (g)
Có: \(S=\dfrac{a}{263,6-a}.100=31,8\left(g\right)\)
=> a = 63,6 (g)
=> nH2O(bđ) = 200 (g)
Giả sử số mol Na2CO3.6H2O là x (mol)
=> mNa2CO3(sau khi hòa tan) = 63,6 + 106x (g)
mdd(sau khi hòa tan) = 263,6 + 214x (g)
\(C\%_{dd.sau.khi.hòa.tan}=\dfrac{63,6+106x}{263,6+214x}.100\%=34,13\%\)
=> x = 0,8 (mol)
=> mNa2CO3.6H2O = 0,8.214 = 171,2 (g)
Đúng 2
Bình luận (0)
Câu1 Trộn 100 ml dung dịch chứa HCl 0,1M và H2SO4 0,05M với 150 ml dung dịch Ba(OH)2 có nồng độ 0,15 M thu được 250 ml dung dịch có pH= x và m gam kết tủa. Giá trị của x và m là Câu2 Cho 10ml dung dịch HNO3 có pH=4. Cần thêm bao nhiêu ml nước cất để thu được dung dịch có pH=6?A. 990 ml. Câu3 Một dung dịch chứa 0,01 mol Na+; 0,02 mol SO42-; 0,01 mol Cl- và x mol Cu2+. Giá trị của x là
Câu 3: Cần thêm bao nhiêu ml H2O (D = 1 g/ml) vào 100 gam dung dịch NaOH 35% để thu được dung dịch NaOH 20%. Câu 4: Cần pha bao nhiêu lít dung dịch HCl 2M với bao nhiêu lít dung dịch HCl 3M để thu được 4 lít dung dịch HCl 2,75M.
\(m_{NaOH\left(35\%\right)}=100.35\%=35\left(g\right)\)
\(m_{ddNaOH\left(20\%\right)}=\dfrac{35}{20}.100=175\left(g\right)\)
⇒ mnước thêm vào = 175-100 = 75(g)
Vnước thêm vào = 75.1 = 75 (ml)
Đúng 1
Bình luận (1)
Câu 4:
\(n_{HCl}=4.2,75=11\left(mol\right)\)
Ta có: \(V_{ddHCl\left(2M\right)}=\dfrac{n_{HCl\left(1\right)}}{2}\left(l\right);V_{ddHCl\left(3M\right)}=\dfrac{n_{HCl\left(2\right)}}{3}\left(l\right)\)
\(\Rightarrow V_{ddHCl\left(2M\right)}+V_{ddHCl\left(3M\right)}=\dfrac{n_{HCl\left(1\right)}}{2}+\dfrac{n_{HCl\left(2\right)}}{3}\)
\(\Leftrightarrow4=\dfrac{3n_{HCl\left(1\right)}+2n_{HCl\left(2\right)}}{6}\Leftrightarrow3n_{HCl\left(1\right)}+2n_{HCl\left(2\right)}=24\)
Ta có: \(\left\{{}\begin{matrix}n_{HCl\left(1\right)}+n_{HCl\left(2\right)}=11\\3n_{HCl\left(1\right)}+2n_{HCl\left(2\right)}=24\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}n_{HCl\left(1\right)}=2\\n_{HCl\left(2\right)}=9\end{matrix}\right.\)
\(\Rightarrow V_{ddHCl\left(2M\right)}=\dfrac{2}{2}=1\left(l\right);V_{ddHCl\left(3M\right)}=\dfrac{9}{3}=3\left(l\right)\)
Đúng 1
Bình luận (0)
Câu 3:
\(m_{NaOH}=35.100\%=35\left(g\right)\\ m_{H_2O\left(thêm\right)}=a\left(g\right)\\ \Rightarrow\dfrac{35}{100+a}.100\%=20\%\\ \Leftrightarrow a=75\left(g\right)\\ \Rightarrow V_{H_2O\left(thêm\right)}=\dfrac{75}{1}=75\left(ml\right)\)
Câu 4:
\(Đặt:V_{ddHCl\left(pha.thêm2M\right)}=a\left(l\right)\\ V_{ddHCl\left(pha.thêm3M\right)}=b\left(l\right)\\ \Rightarrow\dfrac{2a+3b}{a+b}=2,75\left(1\right)\\ Mà:a+b=4\left(2\right)\\ Từ\left(1\right),\left(2\right)\Rightarrow\left\{{}\begin{matrix}a=1\left(l\right)\\b=3\left(l\right)\end{matrix}\right.\)
Vậy cần pha 1 lít dung dịch HCl 2M vào 3 lít dung dịch HCl 3M để thu được 4 lít dung dịch HCl 2,75M
Chúc em học tốt!
Đúng 1
Bình luận (0)
Hoà tan mẫu hợp kim Na - Ba vào nước được dung dịch A và có 13,44 lít H2 bay ra (đktc). Cần dùng bao nhiêu ml dung dịch HCl 1M để trung hoà hoàn toàn 1/10 dung dịch A (ml).
\(n_{H_2}=0,6\left(mol\right)\) \(\dfrac{1}{10}A\) sẽ cho ra \(0,06\left(mol\right)\) khí
Ta có nH+ cần dùng sẽ gấp đôi số mol khí (dùng bảo toàn e)
=> n HCl = 0,12 mol
=> V = 120 ml
Đúng 0
Bình luận (0)
để hòa tan 6,5 g kẽm cần dùng bao nhiêu ml dung dịch hcl 2m
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 ( mol )
\(V_{HCl}=\dfrac{0,2}{2}=0,1l\)
Đúng 3
Bình luận (0)
Xem thêm câu trả lời