Quặng sắt ở nước ta chiếm từ đến % kim loại sắt
DB
Những câu hỏi liên quan
Quặng sắt là các loại đá và khoáng vật mà từ đó sắt kim loại có thể được chiết ra. Quặng sắt thường giàu các sắt oxit và có màu sắc từ xám sẫm, vàng tươi, tía sẫm tới nâu đỏ. Quặng hematite là loại quặng sắt chính có trong các mỏ quặng của nước Brasil. Tỉ lệ sắt trong quặng hematite được biểu diễn ở Hình 37. Trong 8 kg quặng hematite có bao nhiêu ki-lô-gam sắt?
Đọc tiếp
Quặng sắt là các loại đá và khoáng vật mà từ đó sắt kim loại có thể được chiết ra. Quặng sắt thường giàu các sắt oxit và có màu sắc từ xám sẫm, vàng tươi, tía sẫm tới nâu đỏ. Quặng hematite là loại quặng sắt chính có trong các mỏ quặng của nước Brasil. Tỉ lệ sắt trong quặng hematite được biểu diễn ở Hình 37. Trong 8 kg quặng hematite có bao nhiêu ki-lô-gam sắt?
Trong 8 kg quặng hematite có số ki-lô-gam sắt là:
\(\dfrac{{8.69,9}}{{100}} = 5,592\)(ki-lô-gam)
Đúng 0
Bình luận (0)
Những nhận định sau về kim loại sắt:(1) Kim loại sắt có tính khử trung bình. (2) Ion
F
e
2
+
bền hơn
F
e
3
+
. (3) Fe bị thụ động trong
H
2
S
O
4
đặc nguội. (4) Quặng manhetit là quặng có hàm lượng sắt cao nhất. (5) Trái đất tự quay và sắt là n...
Đọc tiếp
Những nhận định sau về kim loại sắt:
(1) Kim loại sắt có tính khử trung bình.
(2) Ion F e 2 + bền hơn F e 3 + .
(3) Fe bị thụ động trong H 2 S O 4 đặc nguội.
(4) Quặng manhetit là quặng có hàm lượng sắt cao nhất.
(5) Trái đất tự quay và sắt là nguyên nhân làm Trái Đất có từ tính.
(6) Kim loại sắt có thể khử được ion F e 3 + .
Số nhận định đúng là:
A. 3
B. 4
C. 5
D. 6
Trong các kim loại quặng sắt, quặng có hàm lượng sắt cao nhất là
A. Hematit nâu
B. Manhetit
C. Xiđerit
D. Hematit đỏ
Trong các kim loại quặng sắt, quặng có hàm lượng sắt cao nhất là
A. manhetit
B. hematit đỏ
C. xiđerit
D. hematit nâu
Đáp án A
Quặng manhetit chứa Fe3O4 là quặng giàu sắt nhất, nhưng hiếm có trong tự nhiên.
Đúng 0
Bình luận (0)
Trong các kim loại quặng sắt, quặng có hàm lượng sắt cao nhất là
A. manhetit
B. hematit đỏ
C. xiđerit
D. hematit nâu
Đáp án A
Quặng manhetit chứa Fe3O4 là quặng giàu sắt nhất, nhưng hiếm có trong tự nhiên
Đúng 0
Bình luận (0)
người ta điều chế sắt từ oxit sắt từ Fe3O4 theo sơ đồ CO+Fe3O4 - - - -> Fe+CO2 a, nếu dùng 1 tấn quặng chứa 90% là Fe3O4 thì lượng sắt kim loại thu được là bao nhiêu kg? b, muốn được 1 tấn sắt thì phải dùng bao nhiêu tấn quặng nói trên?
1 tấn=100000kg
\(m_{Fe_3O_4}=1000000.90\%=900000\left(g\right)\)
\(\rightarrow n_{Fe_3O_4}=\dfrac{900000}{232}=\dfrac{112500}{29}\left(mol\right)\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(\dfrac{112500}{29}\) \(\dfrac{337500}{87}\) (mol)
\(\rightarrow m_{Fe}=\dfrac{337500}{87}.56\approx217241,38\left(g\right)\approx217,24\left(kg\right)\)
b.
\(n_{Fe}=\dfrac{1000000}{56}=\dfrac{125000}{7}\left(mol\right)\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(\dfrac{375000}{7}\) \(\dfrac{125000}{7}\) (mol)
\(\rightarrow m_q=\dfrac{375000}{7}.232.100:90=13809523\left(g\right)=13809,5\left(kg\right)\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
Đúng 0
Bình luận (0)
Người ta trộn hai loại quặng sắt với nhau, một loại chứa 72% sắt, loại thứ hai chứa 58% sắt được một loại quặng chứa 62% sắt. Nếu tăng khối lượng của mỗi loại quặng thêm 15 tấn thì được một loại quặng chứa 63,25% sắt. Tìm khối lượng quặng của mỗi loại đã trộn.
Gọi khối lượng quặng loại thứ nhất là x ( tấn), loại thứ hai là y (tấn)
Điều kiện: x > 0; y > 0
Lượng sắt nguyên chất có trong mỗi loại quặng bằng lượng sắt có trong hỗn hợp ta có phương trình:
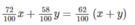
Thêm mỗi loại quặng 15 tấn ta được hỗn hợp chứa 63,25% sắt, ta có phương trình:
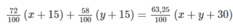
Ta có hệ phương trình:
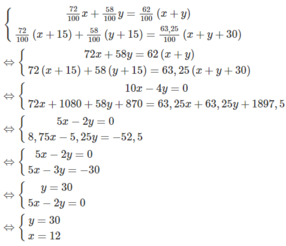
Cả hai giá trị x = 12; y = 30 thỏa mãn điều kiện bài toán.
Vậy loại quặng thứ nhất có 12 tấn, loại quặng thứ hai có 30 tấn.
Đúng 0
Bình luận (0)
Người ta trộn 2 loại quặng sắt vơi snhau. Mỗi loại chứa 72% sắt, loại thứ 2 chứa 58% sắt được 1 loiaj quặng chứa 62% sắt. Nếu tăng khối lượng mỗi loại quặng thêm 15 tấn thì được 1 loại quặng chứa 63,25% sắt. Tìm khối lượng quặng của mỗi loại đã trộn
Gọi khối lượng quặng loại thứ nhất là x tấn ,loại thứ 2 là y tấn ,x>0 ; y>0
ta có hệ phương trình :\(\hept{\frac{\frac{72}{100}x+\frac{58}{100}y=\frac{62}{100}\left(x+y\right)}{\frac{72}{100}\left(x+15\right)+\frac{58}{100}\left(y+15\right)=\frac{63,25}{100}\left(x+y+30\right)}}\)
hay : \(\hept{\begin{cases}5x-2y=0\\5\left(x+15\right)=3\left(y+15\right)\end{cases}}\)
giải hệ phương trình ta đc: (x;y) =(12;30)
vậy khối lượng loại thứ nhất là 12 tấn , loai thứ 2 là 30 tấn
người ta điều chế sắt từ oxit sắt từ Fe3O4 theo sơ đồ
CO+Fe3O4 - - - -> Fe+CO2
a, nếu dùng 1 tấn quặng chứa 90% là Fe3O4 thì lượng sắt kim loại thu được là bao nhiêu kg?
b, muốn được 1 tấn sắt thì phải dùng bao nhiêu tấn quặng nói trên?
a) PTHH:
Fe3O4 + 4CO =(nhiệt)=> 3Fe + 4CO2
1 (mol)------------------------3 (mol)
232(kg)----------------------168(kg)
900 (kg)----------------------x (kg)
Ta có: Khối lượng Fe3O4 có trong 1 tân quặng là: mFe3O4 = 1 x 90% = 0.9 (tấn ) = 900 (kg)
Lập các tỉ lệ số mol và khối lượng theo phương trình ( x là khối lượng kim loại sắt thu được )
=> x = \(\frac{900\times168}{232}\approx651,72\left(kg\right)\)
b)PTHH:
Fe3O4 + 4CO =(nhiệt)=> 3Fe + 4CO2
1 (mol)----------------------3(mol)
232 (tấn)---------------------168 (tấn)
y (tấn)--------------------------1 (tấn)
Lập các số mol và khối lượng trên phương trình ( y là khối lượng Fe3O4 cần dùng )
=> y = \(\frac{1\times232}{168}=1,4\left(t\text{ấn}\right)\)
=> Khối lượng quặng cần dùng: mquặng = \(1,4\div\frac{90}{100}=1,556\left(t\text{ấn}\right)\)
Đúng 0
Bình luận (1)




