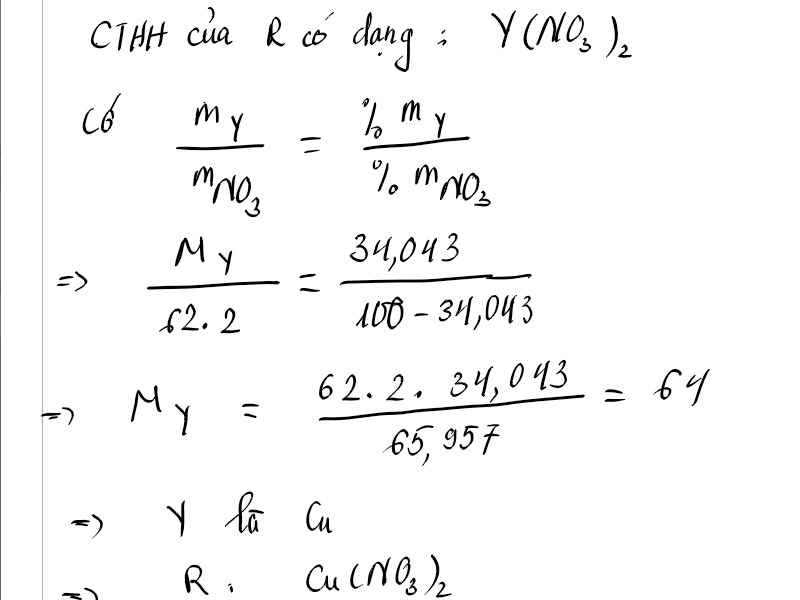tính thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất Ca(NO3)2
LG
Những câu hỏi liên quan
Tính thành phần trăm theo khối lượng của các nguyên tố trong các hợp chất sau: Ca(NO3)2
\(\%m_{Ca}=\dfrac{40}{164}.100=24,39\left(\%\right)\\ \%m_N=\dfrac{28}{164}.100=17,07\left(\%\right)\\ \%m_O=\dfrac{48.2}{164}.100=58,54\left(\%\right)\)
Đúng 2
Bình luận (0)
$M_{Ca(NO_3)_2} = 164$
$\%Ca = \dfrac{40}{164}.100\% = 24,39\%$
$\%N = \dfrac{14.2}{164}.100\% = 17,07\%$
$\%O = 100% -24,39\% -17,07\% = 58,54%%
Đúng 2
Bình luận (0)
1.Tính thành phần phần trăm (theo khối lượng) của các nguyên tố hóa học có mặt trong các hợp chất sau:a) Fe(NO3)2, Fe(NO3)2b) N2O, NO, NO22.Hãy tìm công thức hóa học của chất X có khối lượng mol MX 170 (g/mol), thành phần các nguyên tố theo khối lượng: 63,53% Ag; 8,23% N, còn lại O.3.Lập công thức hóa học của hợp chất A biết:- Phân khối của hợp chất là 160 đvC-Trong hợp chất có 70% theo khối lượng sắt, còn lại là oxi.
Đọc tiếp
1.Tính thành phần phần trăm (theo khối lượng) của các nguyên tố hóa học có mặt trong các hợp chất sau:
a) Fe(NO3)2, Fe(NO3)2
b) N2O, NO, NO2
2.Hãy tìm công thức hóa học của chất X có khối lượng mol MX = 170 (g/mol), thành phần các nguyên tố theo khối lượng: 63,53% Ag; 8,23% N, còn lại O.
3.Lập công thức hóa học của hợp chất A biết:
- Phân khối của hợp chất là 160 đvC
-Trong hợp chất có 70% theo khối lượng sắt, còn lại là oxi.
Câu 2:
Trong 1 mol X: \(\left\{{}\begin{matrix}n_{Ag}=\dfrac{170.63,53\%}{108}=1\left(mol\right)\\n_N=\dfrac{170.8,23\%}{14}=1\left(mol\right)\\n_O=\dfrac{170\left(100\%-63,53\%-8,23\%\right)}{16}=3\left(mol\right)\end{matrix}\right.\)
Vậy CTHH của X là \(AgNO_3\)
Đúng 2
Bình luận (0)
Câu 1:
\(a,\%_{Fe}=\dfrac{56}{180}\cdot100\%=31,11\%\\ \%_N=\dfrac{14\cdot2}{180}\cdot10\%=15,56\%\\ \%_O=100\%-31,11\%-15,56\%=53,33\%\\ b,\%_{N\left(N_2O\right)}=\dfrac{14\cdot2}{44}\cdot100\%=63,63\%\\ \%_{O\left(N_2O\right)}=100\%-63,63\%=36,37\%\\ \%_{N\left(NO\right)}=\dfrac{14}{30}\cdot100\%=46,67\%\\ \%_{O\left(NO\right)}=100\%-46,67\%=53,33\%\\ \%_{O\left(NO_2\right)}=\dfrac{16\cdot2}{46}\cdot100\%=69,57\%\\ \%_{N\left(NO_2\right)}=100\%-69,57\%=30,43\%\)
Đúng 2
Bình luận (0)
1. Tính thành phần phần trăm khối lượng của các nguyên tố trong hợp chất MgSO4; Al(NO3)3
\(M_{MgSO_4}=24+32+16.4=120\\ \%Mg=\dfrac{24}{120}.100=20\%\\ \%S=\dfrac{32}{120}.100=26,67\%\\ \%O=\dfrac{16.4}{120}.100=53,33\%\\ M_{Al\left(NO_3\right)_3}=27+62.3=213\\ \%Al=\dfrac{27}{213}.100=12,68\%\\ \%N=\dfrac{14.3}{213}.100=19,72\%\\ \%O=\dfrac{16.9}{213}.100=67,6\%\)
Đúng 0
Bình luận (0)
1. Tính thành phần phần trăm khối lượng của các nguyên tố trong hợp chất MgSO4; Al(NO3)3
\(MgSO_4=120\)
\(\%Mg=\dfrac{24}{120}.100\%=20\%\)
\(\%S=\dfrac{32}{120}.100\%\text{≈}26,67\%\)
\(\%O=100-\left(20+26,67\right)\text{≈}53,33\%\)
Đúng 1
Bình luận (0)
a) Hợp chất tạo bởi nguyên tố Y ( hóa trị a) và nhóm NO3 có thành phần khối lượng là 34,043% Y. Xác định khối lượng mol của Y theo a?
b) R kết hợp với nguyên tố Oxi tao hợp chất X. Tính phần trăm khối lượng nguyên tố R trong X ?
Đ
ặ
t
:
Y
(
N
O
3
)
2
V
ì
:
%
m
Y
=
34
,
043
%
⇔
M
Y
M
Y
+
124
=
34
,
043
%
⇔
M
Y
=
64
(
g
m
o
l
)
⇒
Y
:
Đ
ồ
n
g
(
C
u
=
64
)
⇒
C
T
H
H
:
C
u
(
N
O
3
)
2
Thu gọn
Đúng 0
Bình luận (0)
Câu 1: Tính phần trăm khối lượng của các nguyên tố trong hợp chất: Fe(NO3)3, K3PO4 , Ca(OH)2, P2O5, SiO2, Fe3O4.
\(Fe\left(NO_3\right)_3:\left\{{}\begin{matrix}\%_{Fe}=\dfrac{56}{242}\cdot100\%=23,14\%\%\\\%_N=\dfrac{14\cdot3}{242}\cdot100\%=17,36\%\\\%_O=\left(100-23,14-17,36\right)\%=59,5\%\end{matrix}\right.\)
\(K_3PO_4:\left\{{}\begin{matrix}\%_K=\dfrac{39\cdot3}{212}\cdot100\%=55,19\%\\\%_P=\dfrac{31}{212}\cdot100\%=14,62\%\\\%_O=\left(100-55,19-14,62\right)\%=30,19\%\end{matrix}\right.\)
\(Ca\left(OH\right)_2:\left\{{}\begin{matrix}\%_{Ca}=\dfrac{40}{74}\cdot100\%=54,05\%\\\%_O=\dfrac{16\cdot2}{74}\cdot100\%=43,24\%\\\%_H=\left(100-54,05-43,24\right)\%=2,71\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
\(P_2O_5:\left\{{}\begin{matrix}\%_P=\dfrac{31\cdot2}{142}\cdot100\%=43,66\%\\\%_O=100\%-43,66\%=56,34\%\end{matrix}\right.\\ SiO_2:\left\{{}\begin{matrix}\%_{Si}=\dfrac{28}{60}\cdot100\%=46,67\%\\\%_O=\left(100-46,67\right)\%=53,33\%\end{matrix}\right.\\ Fe_3O_4:\left\{{}\begin{matrix}\%_{Fe}=\dfrac{56\cdot3}{232}\cdot100\%=72,41\%\\\%_O=\left(100-72,41\right)\%=27,59\%\end{matrix}\right.\)
Đúng 2
Bình luận (1)
1. Tính thành phần phần trăm khối lượng của các nguyên tố trong hợp chất MgSO4; Al(NO3)3
giải giúp em đi ạ :((
\(\left\{{}\begin{matrix}\%Mg=\dfrac{24.1}{120}.100\%=20\%\\\%S=\dfrac{32.1}{120}.100\%=26,667\%\\\%O=\dfrac{16.4}{120}.100\%=53,333\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%Al=\dfrac{27.1}{213}.100\%=12,676\%\\\%N=\dfrac{14.3}{213}.100\%=19,718\%\\\%O=\dfrac{16.9}{213}.100\%=67,606\%\end{matrix}\right.\)
Đúng 3
Bình luận (2)
\(a.\%Mg=\dfrac{24\times100\%}{120}\)\(=20\%\)
\(\%S=\dfrac{32\times100\%}{120}\)\(=26,66\%\)\(\%\)
\(\%O=100\%-\left(20\%+26,66\%\right)\)\(=53,34\%\)
Đúng 1
Bình luận (0)
\(b.\%Al=\dfrac{27}{213}\)\(=12,67\%\)
\(\%N=\dfrac{42}{213}\)\(=19,71\%\)
\(\%O=100\%-12,67\%-19,71\%=67,62\%\)
Đúng 1
Bình luận (0)
Tính phần trăm nguyên tử (theo khối lượng) của các nguyên tố trong hợp chất Al(NO3)3. Biết Al=27; N=14; )=16
\(\%Al=\dfrac{27}{27+62.3}.100=12,68\%\)
\(\%N=\dfrac{14.3}{27+62.3}.100=19,72\%\)
\(\%O=\dfrac{16.9}{27+62.3}.100=67,6\%\)
Đúng 2
Bình luận (0)
Xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.Hợp chấtkhối lượng mình mol( M )Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chấtKhối lượng của mỗi nguyên tố có trong 1 mol hợp chấtThành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chấtKMnO4 -Nêu các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất ....
Đọc tiếp
Xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.
| Hợp chất | khối lượng mình mol( M ) | Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất | Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất | Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất |
| KMnO4 |
-Nêu các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất .
-Viết công thức tính thành phần phần trăm theo khối lượng của 1 nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.
Khối lượng mol :
MKMnO4 = 39 + 55 + 64 = 158 (g/mol)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất :
nK = 1 mol
nMn = 1 mol
nO = 4 mol
Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất :
mK = 39.1 = 39 (g)
mMn = 55.1 = 55 (g)
mO = 16.4 = 64 (g)
Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất :
\(\%m_K=\frac{m_K}{M_{KMnO_4}}.100\%=\frac{39}{158}.100\%=24,7\%\)
\(\%m_{Mn}=\frac{m_{Mn}}{M_{KMnO_4}}.100\%=\frac{55}{158}.100\%=34,8\%\)
\(\%m_O=\frac{m_O}{m_{KMnO_4}}.100\%=\frac{64}{158}.100\%=40,5\%\)
Đúng 0
Bình luận (5)
Các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất :
B1 : Tính khối lượng mol (M) của hợp chất.
B2 : Tính số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Tính khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B4 : Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.
Đúng 0
Bình luận (0)
Công thức tính thành phần phần trăm theo khối lượng của 1 nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất :
\(\%m_A=\frac{m_A}{M_{h\text{/}c}}.100\%\)
Đúng 0
Bình luận (7)