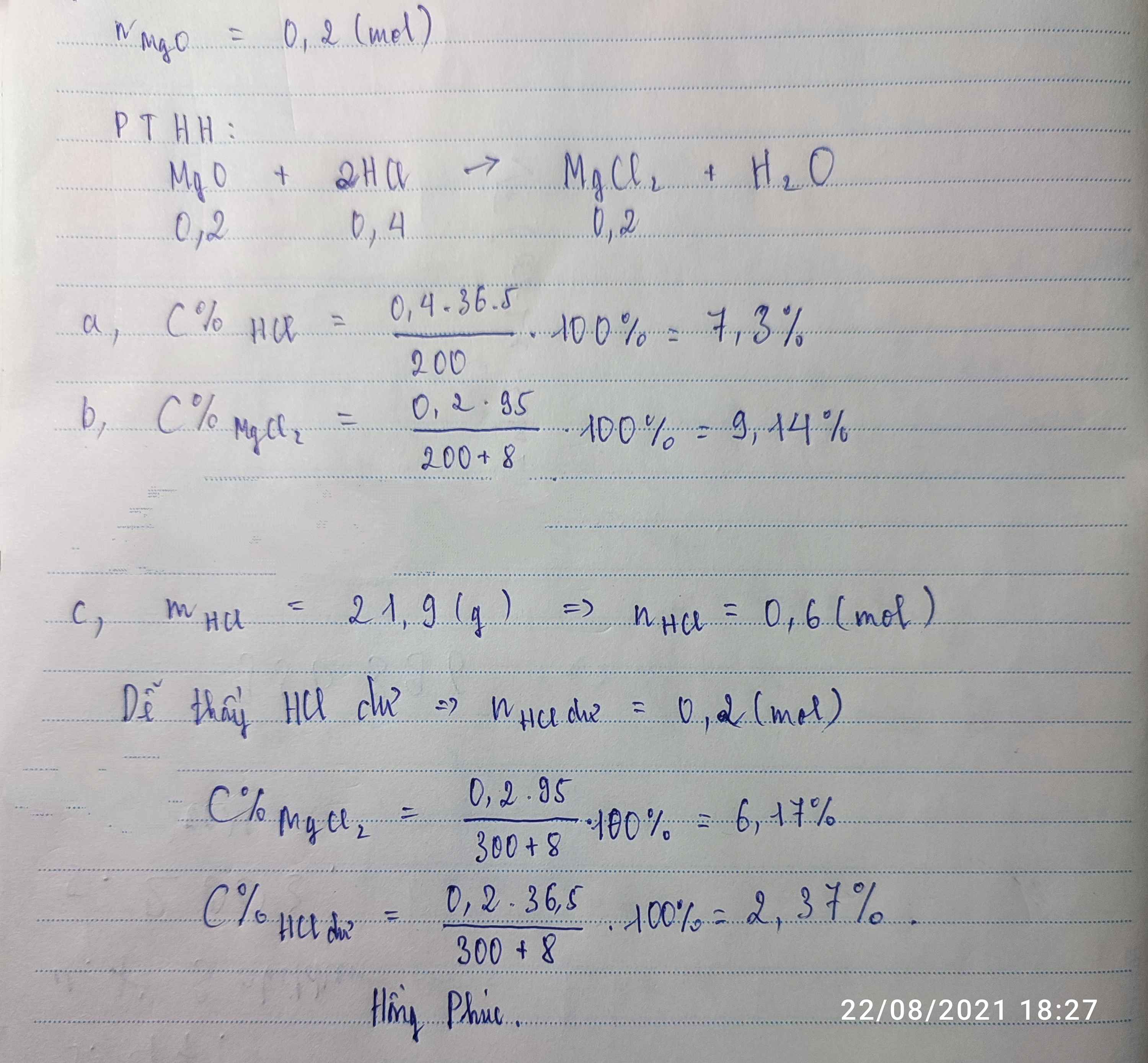hòa tan 5,6g Fe vào 300g đ HCl 3,65%. tính C% của dd sau pứ
H24
Những câu hỏi liên quan
hòa tan 5,6g Fe vào 300g hcl 3,65 %. tính C% dd mới
\(n_{Fe}=\dfrac{5.6}{56}=0.1\left(mol\right)\)
\(n_{HCl}=\dfrac{300\cdot3.65\%}{36.5}=0.3\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Lập tỉ lệ :
\(\dfrac{0.1}{1}< \dfrac{0.3}{2}\) => HCl dư
\(n_{FeCl_2}=n_{H_2}=0.1\left(mol\right)\)
\(n_{HCl\left(dư\right)}=0.3-0.1\cdot2=0.1\left(mol\right)\)
\(m_{dd}=5.6+300-0.1\cdot2=305.4\left(g\right)\)
\(C\%_{FeCl_2}=\dfrac{0.1\cdot127}{305.4}\cdot100\%=4.15\%\)
\(C\%_{HCl\left(dư\right)}=\dfrac{0.1\cdot36.5}{305.4}\cdot100\%=1.2\%\)
Đúng 4
Bình luận (0)
n(Fe)=0,1mol
m(HCl)=10,95g
n(Hcl)=0,3mol
Fe+2HCL-> FeCl2+H2
Ta có 0,1/1 < 0,3/2
Hcl dư
Fe+2HCl->FeCl2+H2
0,1 0,2 0,1 0,1
mdd =300+5,6-0,1.2=305,4g
C%(Fecl2)=0,1.127.100%/305,4 =4,16%
Đúng 3
Bình luận (0)
hòa tan 5,6g Fe vào 200g hcl 3,65 %. tính C% dd mới.
mọi người giúp em với ạ. Hóa 8,9 đó ạ!!hòa tan hoàn toàn mg vào đủ trong 200g dd HCl 3,65%.
a)Tính VH2 sinh ra.
b)Tính mMg tham gia PỨ
\(n_{HCl}=200.3,65\%=7,3g\)
\(m_{HCl}=\dfrac{7,3}{36,5}=0,2mol\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,1 0,2 0,1 ( mol )
\(m_{Mg}=0,1.24=2,4g\)
\(V_{H_2}=0,1.22,4=2,24l\)
Đúng 3
Bình luận (0)
\(m_{HCl}=200.3,65\%=7,3\left(g\right)\\
n_{HCl}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\\ pthh:Mg+2HCl\rightarrow MgCl_2+H_2\)
0,1 0,2 0,1
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\\
m_{Mg}=0,1.24=2,4\left(g\right)\)
Đúng 1
Bình luận (0)
Mg + 2HCl -- > MgCl2 + H2
mHCl = (200.3,65) / 100 = 7,3(g)
=> nHCl = 7,3 : 36,5 = 0,2 (mol)
=> nH2 = 0,1 (mol)
=> VH2 = 0,1 .22,4 = 2,24(l)
nMg = nHCl = 0,2(mol)
mMg = 0,1 . 24 = 2,4(g)
Đúng 0
Bình luận (1)
1. Dẫn 3.36lit CO2 vào 400ml Ca(OH)2 1M sau pứ thu đc muối CaCO3
a. viết pt pứ
b. Kluong chất rắn không tan
c. CM của chất có trong dd sau pứ(xem thế tích thay đổi không đáng kể)
2. Hòa tan hoàn toàn CaCO3 vào dd HCL 3,65% sau pứ thu đc 4.48 lít CO2
a. klg CaCO3
b. klg dd axit
c. % dd muối
d. Dẫn khí co2 vào dd Ba(OH)2 dư tính khlg chất không tan thu đc
giúp mìk vs nhe
bài 2 nCO2=\(\frac{4,48}{22,4}\)= ( chắc đề bạn ghi thiếu )
pt: CaCO3 + 2HCl --> CaCl2 + H2O + CO2
0,2mol 0,2mol 0,2mol 0,2mol
a, ta có : nCaCO3=nCO2=0,2 mol
=> mCaCO3=0,2.100=20(g)
b,nHCl=2nCO2=0,4 mol
=>mHCl=0.4.36,5=14,6(g)
=> mddHCl=\(\frac{14,6.100}{3,65}\)=400(g)
c,nCaCl2=nCO2=0,2mol
=> mCaCl2=0,2.111=22.2(g)
=> mCO2(thoát ra ) =0,2.44=8.8(g)
=>mddSPU=400+40-8,8=431.2g
=>C%CaCl2= \(\frac{22,2}{431,2}.100\)
=5,14%
d,pt :Ba(OH)2 +CO2 --> BaCO3(chat k tan trong H2O)+ H2O
0,2mol 0,2mol
mBa(OH)2=0,2.171=34,2g
het.....:v
Đúng 0
Bình luận (2)
1,
a, \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
b, \(n_{CO_2}=\frac{V}{22.4}=\frac{3.36}{22.4}=0.15\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=V\times C_M=0.4\times1=0.4\left(mol\right)\)
Ta có tỉ lệ \(n_{CO_2}< n_{Ca\left(OH\right)_2}\) nên ta tính theo số mol của CO2
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0.15 0.15 0.15 0.15 (mol)
Khối lượng Ca(OH)2 dư là \(m_{Ca\left(OH\right)_2du}=n_{du}\times M=\left(0.4-0.15\right)\times74=18.5\left(g\right)\)
c, \(C_{MCaCO_3}=\frac{n}{V}=\frac{0.15}{0.4}=\frac{3}{8}\left(M\right)\)
\(C_{MCa\left(OH\right)_2du}=\frac{n}{V}=\frac{0.4-0.15}{0.4}=\frac{5}{8}\left(M\right)\)
Đúng 0
Bình luận (4)
Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.
Đọc tiếp
Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.
a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.
c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.
a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.
c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.
Hòa tan 5,6g Fe bằng 50g dd HCL 18,25%. Sau phản ứng thu được dd X. Cho toàn bộ dd X ở trên tác dụng vừa đủ với 44,6g dd Na2Co3 thu được dd T. Tính C% các chất tan trong dd T
1.Hòa tan 4g ZnO vào 150g dd HCl 3,65%.Tính C% dd thu được sau phản ứng
2.Cho 15,3g oxit của kim loại hóa trị II vào nước thu đc dd bazo nồng độ 8,55%.Xác định công thức oxit trên
Hòa tan Mg vào ống đựng 7,3g dd HCl sau pứ thu được 2,24 lít H2 đktc a) tính KL Mg đã pứ b) HCl có dư không? Dự bao nhiêu?
Mik không tính ra được cậu có ghi đề sai không
Đúng 0
Bình luận (0)
a, \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Theo PT: \(n_{Mg}=n_{H_2}=0,1\left(mol\right)\Rightarrow m_{Mg}=0,1.24=2,4\left(g\right)\)
b, \(n_{HCl\left(pư\right)}=2n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{HCl\left(pư\right)}=0,2.36,5=7,3\left(g\right)\)
Vậy: HCl không dư.
Đúng 2
Bình luận (0)
ⁿHCl=7,3/36,5=0,2(mol)
Mg + 2HCl => MgCl₂ + H₂
1 2 1 1
0,1 < 0,2> 0,1 0,1
mMg=24.0,1=2,4(g)
lặp tỉ lệ
0,1/1 = 0,2/2
nên HCl không dư
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Hòa tan hoàn toàn 6,3175g hh muối gồm NaCl,KCl,MgCl2 vào nước rồi thêm vào đó 100ml dd AgNO3 1,2M sau pứ lọc tách kết tủa A thu đc dd B. Cho 2g Mg vào dd B pứ kết thúc đc kết tủa C và dd D. Cho kết tủa C tác dụng với dd HCl dư pứ sau pứ thấy klg C giảm đi 1,844g. Thêm NaOH dư vào dd D lọc kết tủa đem nung đến klg ko đổi thu đc 0,3g chất rắn E.a) Tính klg các kết tủa A và Cb) Tính % klg các muối có trong hh bđ
Đọc tiếp
Hòa tan hoàn toàn 6,3175g hh muối gồm NaCl,KCl,MgCl2 vào nước rồi thêm vào đó 100ml dd AgNO3 1,2M sau pứ lọc tách kết tủa A thu đc dd B. Cho 2g Mg vào dd B pứ kết thúc đc kết tủa C và dd D. Cho kết tủa C tác dụng với dd HCl dư pứ sau pứ thấy klg C giảm đi 1,844g. Thêm NaOH dư vào dd D lọc kết tủa đem nung đến klg ko đổi thu đc 0,3g chất rắn E.
a) Tính klg các kết tủa A và C
b) Tính % klg các muối có trong hh bđ