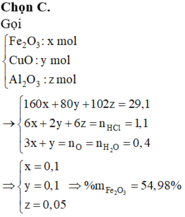Cần ít nhất bao nhiêu gam dung dịch H2SO4 20% để hòa tan hoàn toàn 16 gam Fe2O3
TN
Những câu hỏi liên quan
Cần ít nhất bao nhiêu gam dung dịch H2SO4 20% để hòa tan hoàn toàn 16 gam Fe2O3
\(Fe_2O_3+3H_2SO_4->Fe_2\left(SO_4\right)_3+3H_2O\\ m_{dd}=\dfrac{\dfrac{16}{160}\cdot3\cdot98}{0,2}=147g\)
Đúng 2
Bình luận (4)
Cần ít nhất bao nhiêu gam dung dịch H2SO4 20% để hòa tan hoàn toàn 16 gam Fe2O3
Ta có : số mol Fe2O3=16/160=0.1 mol
PTHH: Fe2O3+3H2SO4=>Fe2(SO4)3+3H2
0.1 0.3 mol
mdd H2SO4=0.3x98:20%=147g
Đúng 1
Bình luận (0)
Cần ít nhất bao nhiêu gam dung dịch H2SO4 20% để hòa tan hoàn toàn 16 gam Fe2O3
Để tính số gam dung dịch H2SO4 cần thiết để hoà tan hoàn toàn 16 gam Fe2O3, ta sử dụng phương trình phản ứng sau: Fe2O3 + 3H2SO4 -> Fe2(SO4)3 + 3H2O Theo phương trình trên, ta thấy 1 mol Fe2O3 tương ứng với 3 mol H2SO4. Ta cần tìm số mol H2SO4 cần thiết để hoà tan 16 gam Fe2O3. Khối lượng mol của Fe2O3 = 2 x khối lượng nguyên tử Fe + khối lượng nguyên tử O = 2 x 55.85 + 16 = 159.7 g/mol Số mol Fe2O3 = khối lượng Fe2O3 / khối lượng mol Fe2O3 = 16 / 159.7 ≈ 0.1 mol Số mol H2SO4 cần thiết = 3 x số mol Fe2O3 = 3 x 0.1 = 0.3 mol Dung dịch H2SO4 có nồng độ 20%, tức là có 20 gam H2SO4 trong 100 gam dung dịch. Vậy trong 1 gam dung dịch H2SO4 có 0.2 gam H2SO4. Số gam dung dịch H2SO4 cần thiết = số mol H2SO4 cần thiết x khối lượng mol H2SO4 x 100 / % nồng độ H2SO4 = 0.3 x 98 x 100 / 20 = 147 gam. Vậy cần ít nhất 147 gam dung dịch H2SO4 20% để hoà tan hoàn toàn 16 gam Fe2O3.
Đúng 0
Bình luận (0)
Thể tích dung dịch HNO3 1M (loãng) ít nhất cần dùng để hòa tan hoàn toàn một hốn hợp gồm 0,15 mol Fe và 0,15 mol Cu là (biết phản ứng tạo chất khử duy nhất là NO)
A. 1,0 lít
B. 0,6 lít
C. 0,8 lít
D. 1,2 lít
Đáp án C
Thể tích dung dịch HNO3 là ít nhất → dung dịch gồm Fe2+ và Cu2+

Số mol HNO3 cần dùng là: 0,6 + 0,2 = 0,8 mol
Thể tích dung dịch HNO3 1M cần dùng là:
![]()
Đúng 0
Bình luận (0)
Thể tích dung dịch HNO3 1M loãng ít nhất cần dùng để hòa tan hoàn toàn một hỗn hợp gồm 0,15 mol Fe và 0,15 mol Cu là: (Biết phản ứng tạo chất khử duy nhất là NO):
A. 1,0 lít
B. 0,6 lít
C. 0,8 lít
D. 1,2 lít
Đáp án C
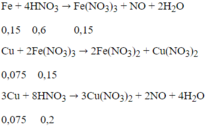
Số mol HNO3 cần dùng là: 0,6 + 0,2 = 0,8 mol
Thể tích dung dịch HNO3 1M cần dùng là:

Đúng 0
Bình luận (0)
Hỗn hợp X gồm Fe2O3, CuO và Al2O3. Để hòa tan vừa đủ 29,1 gam hỗn hợp X cần 2,2 lít dung dịch HCl 0,5M. Lấy 14,55 gam hỗn hợp X cho tác dụng hoàn toàn với H2 dư (nung nóng) thu được 3,6 gam H2O. Phần trăm khối lượng Fe2O3 trong X là A. 57,10%. B. 55,00%. C. 54,98%. D. 42,09%.
Đọc tiếp
Hỗn hợp X gồm Fe2O3, CuO và Al2O3. Để hòa tan vừa đủ 29,1 gam hỗn hợp X cần 2,2 lít dung dịch HCl 0,5M. Lấy 14,55 gam hỗn hợp X cho tác dụng hoàn toàn với H2 dư (nung nóng) thu được 3,6 gam H2O. Phần trăm khối lượng Fe2O3 trong X là
A. 57,10%.
B. 55,00%.
C. 54,98%.
D. 42,09%.
Khử hoàn toàn m gam oxit MxOy cần vừa đủ 17,92 lít khí CO (đktc), thu được a gam kim loại M. Hòa tan hết a gam M bằng dung dịch H2SO4 đặc nóng (dư), thu được 20,16 (lít) khí SO2 (sản phẩm khử duy nhất, ở đktc). Oxit MxOy là: A. Cr2O3 B. FeO C. Fe3O4 D. CrO
Đọc tiếp
Khử hoàn toàn m gam oxit MxOy cần vừa đủ 17,92 lít khí CO (đktc), thu được a gam kim loại M. Hòa tan hết a gam M bằng dung dịch H2SO4 đặc nóng (dư), thu được 20,16 (lít) khí SO2 (sản phẩm khử duy nhất, ở đktc). Oxit MxOy là:
A. Cr2O3
B. FeO
C. Fe3O4
D. CrO
Đáp án C
Ta có: nCO = 0,8 mol; = 0,9 mol
Gọi n là hóa trị của kim loại M (1 ≤ n ≤ 3)
Trong phản ứng giữa M với H2SO4 đặc nóng, M là chất khử nhường electron.
H2SO4 đặc là chất oxi hóa nhận electron:

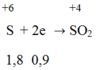
Trong phản ứng khử oxit kim loại bởi CO ta luôn có:
nO (trong oxit) = nCO = 0,8 mol
⇒Tỉ lệ:
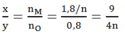
Dựa vào các đáp án ta thấy n = 2 hoặc n = 3

Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 33.4 gam hỗn hợp X gồm Al,Fe,Cu ngoài không khí thu được 41,4 gam hỗn hợp Y gồm 3 oxit . cho Y tác dụng hoàn toàn với dung dịch H2SO4 20% biết D=1,14 g/ml , thể tích tối thiểu của dung dịch H2SO4 20% để hoà tan hết hỗn hợp Y là bao nhiêu?
o mol o2 pu la :(41,4-33,4)/32=0,25 mol
o2 +4e ->2 o2-
2h+ +2e ->h2
=>so mol h+ la 4.0,25=1 mol
so mol h2so4 la 0,5 mol
=>v=(0,5.98.5)/1,14=215 ml
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Hòa tan hoàn toàn 20,88 gam một oxit sắt bằng dung dịch H2SO4 đặc, nóng thu được dung dịch X và 3,248 lít khí SO2 (sản phầm khử duy nhất, ở đktc). Cô cạn dung dịch X, thu được m gam muối sunfat khan. Giá trị của m là:
A. 52,2
B. 48,4
C. 54,0
D. 58,0
Đáp án D
Ta có: = 0,145 mol
Quy đổi 20,88 g oxit sắt FexOy thành 20,88 g Fe và O
Gọi nFe = x mol; nO = y mol
Quá trình nhường electron:
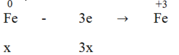
Quá trình nhận electron:
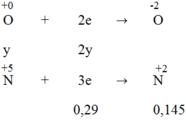
Áp dụng định luật bảo toàn electron, ta có:
3x = 2y + 0,29 → 3x - 2y = 0,29 (1)
Mặt khác: 56x + 16y = 20,88 (2)
Từ (1) và (2) → x = 0,29 và y = 0,29
Muối sinh ra là muối Fe2(SO4)3. Áp dụng ĐL bảo toàn nguyên tố ta có:
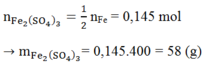
Đúng 0
Bình luận (0)