Viết công thức Lewis của các phân tử CS2, SCl2 và CCl4.
H24
Những câu hỏi liên quan
Viết công thức Lewis cho các phân tử H2O và CH4. Mỗi phân tử này có bao nhiêu cặp electron hóa trị riêng?
- Phân tử H2O:
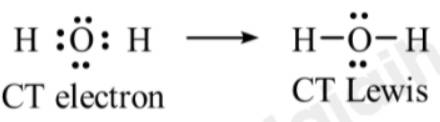
⟹ Phân tử H2O có 2 cặp electron hóa trị riêng.
- Phân tử CH4:
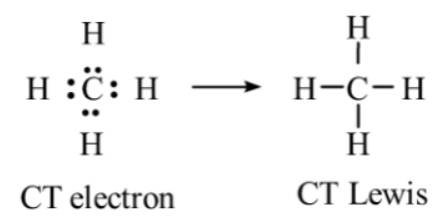
⟹ Phân tử CH4 không có cặp electron hóa trị riêng.
Đúng 0
Bình luận (0)
Hãy biểu diễn sự hình thành các cặp electron chung cho phân tử NH3. Từ đó, viết công thức Lewis của phân tử này.
Bước 1: Viết cấu hình electron của N (Z = 7) và H (Z = 1)
N (Z = 7): 1s22s22p3
H (Z = 1): 1s1
Bước 2: Biểu diễn sự hình thành các cặp electron chung cho NH3
H có 1e ở lớp electron ngoài cùng, N có 5e ở lớp electron ngoài cùng.
⟹ Mỗi nguyên tử góp chung 1e để đạt cấu hình khí hiếm bền vững.
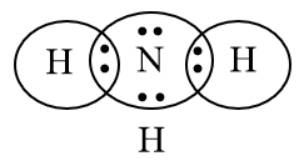
Bước 3: Công thức Lewis của NH3
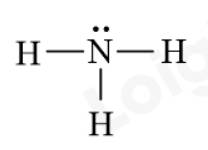
Đúng 0
Bình luận (0)
Để hình thành phân tử phosphorus trichloride (PCl3) thì mỗi nguyên tử chlorine và phosphorus đã góp chung bao nhiêu electron hóa trị? Viết công thức Lewis của phân tử.
- Trong phân tử phosphorus trichloride gồm 2 nguyên tố: P và Cl
+ Nguyên tử P có 5 electron ở lớp ngoài cùng => Góp chung 3 electron độc thân để hình thành 3 liên kết cộng hóa trị
+ Nguyên tử Cl có 7 electron ở lớp ngoài cùng => 3 nguyên tử Cl, mỗi nguyên tử góp chung 1 electron độc thân để hình thành 3 liên kết cộng hóa trị với P.
=> Khi đó, quanh P và Cl đều có 8 electron như khí hiếm Argon.
- Công thức Lewis của phân tử:

Đúng 0
Bình luận (0)
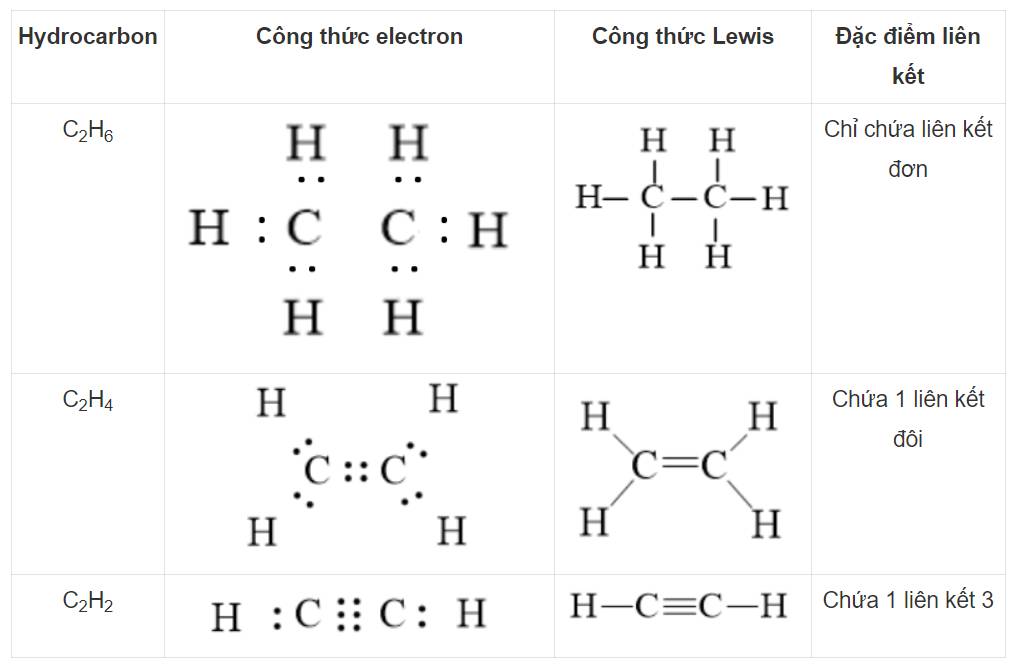
Em hãy viết công thức electron, công thức Lewis của các hydrocarbon sau: C2H6, C2H4, C2H2. Nhận xét sự khác nhau về đặc điểm liên kết trong phân tử của ba hydrocarbon trên.
0,7 g một anken có thể làm mất màu 16,0 g dung dịch brom (trong C C l 4 ) có nồng độ 12,5%.
1. Xác định công thức phân tử chất A.
2. Viết công thức cấu tạo của tất cả các đồng phân cấu tạo ứng với công thức phân tử tìm được. Ghi tên từng đồng phân.
1. C n H 2 n + B r 2 → C n H 2 n B r 2
Số mol anken = số mol
B
r
2
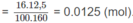
Khối lượng 1 mol anken 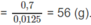
14n = 56 ⇒ n = 4 ⇒ C4H8.
2. Công thức cấu tạo
C H 2 = C H - C H 2 - C H 3 (but-1-en);
C H 3 - C H = C H - C H 3 (but-2-en)
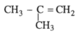 (2-metylpropen )
(2-metylpropen )
 (xiclobutan)
(xiclobutan)
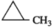 (metylxiclopropan)
(metylxiclopropan)
Đúng 0
Bình luận (0)
Mô tả sự hình thành phân tử N2 từ hai nguyên tử N. Phân tử N2 có bao nhiêu cặp electron dùng chung? Viết công thức Lewis của N2.
- Cấu hình electron của N (Z = 7): 1s22s22p3
- Để đạt cấu hình của khí hiếm gần nhất, mỗi nguyên tử N đều cần thêm 3 electron. Vì vậy mỗi nguyên tử N cùng góp 3 electron để tạo nên 3 cặp electron chung cho 2 nguyên tử N.
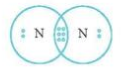
⟹ Số cặp electron dùng chung là 3.
⟹ Công thức Lewis của N2:
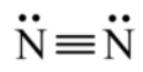
Đúng 0
Bình luận (0)
Viết công thức Lewis của CO2. Giữa nguyên tử carbon và mỗi nguyên tử oxygen có bao nhiêu cặp electron chung?
- Từ công thức electron của CO2:
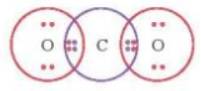
⟹ Mỗi nguyên tử O có 2 cặp electron dùng chung với nguyên tử C.
- Viết công thức Lewis của CO2: O = C = O
Đúng 0
Bình luận (0)
Tính hóa trị của mỗi nguyên tố trong công thức phân tử các hợp chất sau. Cho biết S hóa trị II: K 2 S ; MgS; C r 2 S 3 ; C S 2
-
K
2
S
: Ta có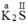
Theo quy tắc hóa trị: a.2 = II.1 → a = 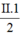 = I
= I
Vậy K có hóa trị I.
- MgS: Ta có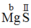
Theo quy tắc hóa trị: b.1 = II.1 → b = 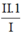 = II
= II
Vậy Mg có hóa trị II.
-
C
r
2
S
3
: Ta có 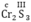
Theo quy tắc hóa trị: c.2 = II.3 → c = 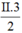 = III
= III
Vậy Cr có hóa trị III.
-
C
S
2
: Ta có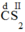
Theo quy tắc hóa trị: d.1 = II.2 → d = 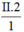 = IV
= IV
Vậy C có hóa trị IV.
Đúng 2
Bình luận (0)
Dẫn hỗn hợp gồm 2 chất X và Y có công thức phân tử C3H6 và C4H8 vào dung dịch brom trong dung môi CCl4 thấy dung dịch brom bị nhạt màu và không có khí thoát ra.Có bao nhiêu cặp X,Y thỏa mãn điều kiện đề cho,viết công thức cấu tạo của từng cặp.
Xem chi tiết
Theo độ âm điện, boron trifluoride là hợp chất ion, thực tế nó là hợp chất cộng hóa trị, với công thức Lewis như sau:
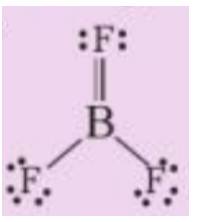
a) Viết phương trình hóa học tạo chất trên từ các đơn chất
b) Phân tử BF3 có bao nhiêu liên kết σ và bao nhiêu liên kết п?
a) Phương trình hóa học: 2B + 3F2 → 2BF3
b) Trong phân tử BF3 có 2 liên kết đơn, 1 liên kết đôi (gồm 1 liên kết σ và 1 liên kết п)
=> Trong phân tử BF3 có 3 liên kết σ và 1 liên kết п
Đúng 0
Bình luận (0)