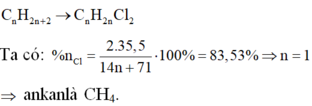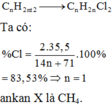Một loại nước clo chứa : Cl2 0,061M ; HCl 0,03M và HClO 0,03M. a) Viết phương trình phản ứng của Cl2 với H2O b) Thể tích khí clo (đktc) để thu được 5 lít nước clo trên ?
TA
Những câu hỏi liên quan
Trong 1 loại nước ta thấy nồng độ Cl2 là 0,061M còn nồng độ của HCl và HClO là 0,03 M . Hỏi phải hòa tan bao nhiêu lít khí Cl2 ( đktc) vào nước để thu đc 5 lít nc Clo như trên.
PTHH: \(H_2O+Cl_2\rightarrow HCl+HClO\\ 0,15:0,15\leftarrow0,15:0,15\)
\(n_{HCl}=n_{HClO}=0,03.5=0,15\left(mol\right)\)
\(n_{Cl_2trong5l}=0,061.5=0,305\left(mol\right)\)
\(V_{Cl_2candung}=\left(0,305+0,15\right).22,4=10,192\left(l\right)\)
Đốt cháy hết 12gam kim loại magie (Mg) trong bình chứa đầy khí clo CL2, thu được 47,5 gam magie clorua MgCL2 A)viết công thức của phản ứng xảy ra B)tính khối lượng khí clo đã phản ứng
P/ứng hóa học: \(Mg+Cl_2->MgCl_2\)
Công thức của p/ứng có phải CT về khối lượng không nhỉ? Mình chưa hiểu lắm. Nếu là CT về kh lượng thì:
\(m_{Mg}+m_{Cl_2}=m_{MgCl_2}\)
* Khối lượng khí clo đã p/ứ:
Theo ĐLBTKL:
\(m_{Mg}+m_{Cl_2}=m_{MgCl_2}\\ =>12g+m_{Cl_2}=47,5g\\ =>m_{Cl_2}=47,5g-12g=35,5g\)
Vậy có 35,5g khí Clo tham gia p/ứng.
Đúng 0
Bình luận (0)
14. Cho 25g nước Clo vào dd có chứa 2,5g KBr. Sau phản ứng , thấy KBr vẫn còn dư. Cô cạn dd thu đc 1,61g chất rắn khan. Xác định nồng độ % của nước Clo?
15 . Cho m gam Kmno4 tác dụng hết vs dd HCl đặc , dư thu đc 28,07g hỗn hợp 2 muối và V lít khí Cl2 ( đktc) . Cho toàn bộ lượng khí Cl2 sinh ra oxi hoá vừa đủ 7,5g hỗn hợp gồm Al và kim loại M có tỉ lệ số mol tương ứng là 1:2 . Xác định kim loại M?
Đọc tiếp
14. Cho 25g nước Clo vào dd có chứa 2,5g KBr. Sau phản ứng , thấy KBr vẫn còn dư. Cô cạn dd thu đc 1,61g chất rắn khan. Xác định nồng độ % của nước Clo?
15 . Cho m gam Kmno4 tác dụng hết vs dd HCl đặc , dư thu đc 28,07g hỗn hợp 2 muối và V lít khí Cl2 ( đktc) . Cho toàn bộ lượng khí Cl2 sinh ra oxi hoá vừa đủ 7,5g hỗn hợp gồm Al và kim loại M có tỉ lệ số mol tương ứng là 1:2 . Xác định kim loại M?
Bài 15. Lời giải:
16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 8H2O + 5Cl2
Theo PTHH : \(n_{KCl}=n_{MnCl_2}=x\)
Khối lượng muối = 28,07 ⇒ \(m_{KCl}+m_{MnCl_2}=28,7\)
⇒ x . 74,5 + x . 126 = 28,07
⇒ x = 0,14 mol
\(\Rightarrow n_{KCl}=n_{MnCl_2}=0,14mol\)
Theo PTHH ⇒ \(n_{Cl_2}=\frac{5}{2}n_{KCl}=\frac{5}{2}.0,14=0,35mol\)
Theo định luật bảo toàn e : \(x.n_M+3n_{Al}=2n_{Cl_2}=0,7mol\)
Có tỉ lệ mol Al : M = 1 : 2 \(\Rightarrow\) nAl = a thì nM = 2a
⇒ 2a.x + a.3 = 0,7 mol
Với x = 1 ⇒ a = 0,175 mol ⇒ m Al = 0,175.27 = 4,725 gam
⇒ mM = 7,5 – 4,725 = 2,775 gam
⇒ \(M_M=\frac{2,775}{0,175.2}=7,9\)(loại)
Với x = 2 ⇒ a = 0,1 mol ⇒ mAl = 27.0,1 = 2,7 gam ⇒ m M = 7,5 – 2,7 = 4,8 gam
\(\Rightarrow M_M=\frac{4,8}{0,1.2}=24\)(Mg, chọn)
Vậy kim loại cần tìm là Mg
Bài 14. Lời giải:
\(Cl_2+2NaBr\rightarrow2NaCl+Br_2\\ n_{Cl_2}=\frac{2,5-1,61}{44,5}=0,02\left(mol\right)\\ C\%_{Cl_2}=\frac{0,02.71}{25}.100\%=5,68\%\)
Test câu trả lời.
Cho khí clo vào nước được dung dịch có màu vàng nhạt.Trong nước clo có chứaA. Cl2,H2O B.HCl,HClO C. HCl,HClO, H2O D. HCl,HClO, H2O,Cl2
Xem chi tiết
Có thể tồn tại đồng thời những chất sau trong một bình chứa được không? Khí oxi O2 và khí clo Cl2
Khí oxi và khí clo có thể tồn tại trong một bình vì O2 không tác dụng trực tiếp với Cl2
Đúng 0
Bình luận (0)
Có thể tồn tại đồng thời những chất sau trong một bình chứa được không? Khí hiđro iotua HI và khí clo Cl2
Khí HI và Cl2 không tồn tại trong một bình vì Cl2 là chất oxi hóa mạnh và HI là chất khử mạnh
Đúng 0
Bình luận (0)
Một ankan phản ứng với Cl2 (theo tỉ lệ mol 1: 2) thu được sản phẩm chứa 83,53% clo về khối lượng. Công thức phân tử của ankan là: A. CH4 B. C2H6 C. C3H8 D. C4H10
Đọc tiếp
Một ankan phản ứng với Cl2 (theo tỉ lệ mol 1: 2) thu được sản phẩm chứa 83,53% clo về khối lượng. Công thức phân tử của ankan là:
A. CH4
B. C2H6
C. C3H8
D. C4H10
Khi hòa tan clo vào nước ta thu được nước clo có màu vàng nhạt. Khi đó một phần clo tác dụng với nước. Vậy nước clo có chứa những chất gì A. HCl, HClO B. Cl2, HCl, HClO C. H2O, Cl2, HCl, HClO D. Cl2, H2O
Đọc tiếp
Khi hòa tan clo vào nước ta thu được nước clo có màu vàng nhạt. Khi đó một phần clo tác dụng với nước. Vậy nước clo có chứa những chất gì
A. HCl, HClO
B. Cl2, HCl, HClO
C. H2O, Cl2, HCl, HClO
D. Cl2, H2O
Khi hòa tan Cl2 vào nước xảy ra phản ứng: Cl2 + H2O ⇋ HCl + HClO.
→ Thành phần của nước Cl2 là Cl2; HCl; HClO và H2O.
Để lâu này nước Cl2 bị mất màu do Cl+1 trong HCl có tính oxi hóa mạnh, làm mất màu nước Cl2.
Đúng 0
Bình luận (0)
Một ankan phản ứng với Cl2 (theo tỉ lệ số mol 1 : 2) thu được sản phẩm chứa 83,53 % clo về khối lượng. Công thức phân tử của ankan là: A. CH4. B. C2H6. C. C3H8. D. C4H10.
Đọc tiếp
Một ankan phản ứng với Cl2 (theo tỉ lệ số mol 1 : 2) thu được sản phẩm chứa 83,53 % clo về khối lượng. Công thức phân tử của ankan là:
A. CH4.
B. C2H6.
C. C3H8.
D. C4H10.