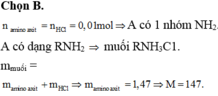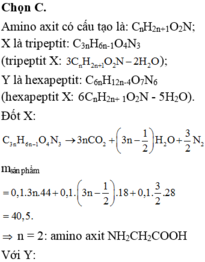tính số mol axit HCl có trong 40ml ddHCl 0.75M
BP
Những câu hỏi liên quan
Hòa tan 7,8 g hh gồm Mg , Al vào dd HCl dư. sau phản ứng thấy khối lượng ddHCl tăng 7g số mol axit HCl đã tham gia phản ứng là?
Khối lượng H2 thoát ra trong phản ứng chính bằng:
\(7,8-7=0,8\) gam
\(\Rightarrow n_{H_2}=0,4\) mol
Bảo toàn nguyên tố H: \(n_{HCl}=n_{H^+}=2n_{H_2}=0,8\) mol
Vậy số mol HCl tham gia phản ứng là 0,8 mol
Đúng 0
Bình luận (0)
1.để hòa tan 3,6g Mg phải dùng bao nhiêu ml hỗn hợp axit Hcl 1 M H2so4 0.75M
2.cho 111.6g hỗn họp Fe2o3 và FeO tỉ lệ mol 1:1 vào 300ml dd HCl 2M thu đc dd A
a. Tính Cm các chất có trog dd
b.tính Vdd NaOH 1.5M đủ tác dụng với dd A
1.để hòa tan 3,6g Mg phải dùng bao nhiêu ml hỗn hợp axit Hcl 1 M H2so4 0.75M
2.cho 111.6g hỗn họp Fe2o3 cvaf FeO tỉ lệ mol 1:1 vào 3000ml dd HCl 2M thu đc dd A
a. Tính Cm các chất có trog dd
b.tính Vdd NaOH 1.5M đủ tác dụng với dd A
Giúp mk với mk đang cần gấp cảm ơn nhìu
Để trung hòa 10ml dd hỗn hợp axit gồm h2so4 và hcl cần dùng 40ml dd NaOH 0,5M . Mặt khác lấy 100ml dd axit đem trung hòa một lượng xút vừa đủ rồi cô cạn thì thu được 13,2g muối khan. tính nồng độ mol/l của mỗi axit trong dd ban đầu.
Gọi x là nHCl, y là nH2SO4
nNaOH=0.5.0.04=0.02mol
=>nOH-=0.02mol
PT:
H(+)+OH(-)-->H2O
0.02<0.02
=>nH+ trong 10ml hh axit=0.02
=>nH+ trong 100ml hh axit=0.02.10=0.2mol
PT:
H(+)+OH(-)-->H2O
0.2->0.2
=>nNaOH=0.2mol
m muối=mNa(+)+mCl(-)+mSO4(2-)=23.0.2+35.5x...
< = > 35.5x+96y=8.6 (1)
Ta lại có: nH+=x+2y=0.2 (2)
Từ (1)(2)=>x=0.08, y=0.06.
Vậy [HCl]=0.08M, [H2SO4]=0.06M.
Giải rõ nhé!!!!!!!!!
Đúng 1
Bình luận (0)
Đặt x, y lần lượt là nồng độ mol/lit của axit H2SO4 và axit HCl
Viết PTHH.
Lập hệ phương trình:
2x + y = 0,02 (I)
142x + 58,5y = 1,32 (II)
Giải phương trình ta được:
Nồng độ của axit HCl là 0,8M và nồng độ của axit H2SO4 là 0,6M.
Đúng 0
Bình luận (1)
Để trung hòa 10ml dung dịch hỗn hợp axit gồm H2SO4 và HCl cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100ml dung dịch hỗn hợp axit trên đem trung hòa với một lượng dung dịch NaOH vừa đủ rồi cô cạn thì thu được 24,65g muối khan. Tính nồng độ mol/L của mỗi axit
trong dung dịch ban đầu nhé mn
Đúng 0
Bình luận (0)
Để trung hoà 10ml dd hỗn hợp axit gồm h2so4 và HCl cần dùng 40ml dd NaOH 0,5M. Mặt khác lấy 100ml dd axit đem trung hoà 1 lượng xút vừa đủ rồi cô cạn thì thu đc 13,2g muối than. Tính nồng độ mol/l của mỗi axit trg dd ban đầu.
Mn giúp mình với.
Hòa tan với một lượng xút chứ hk phải súp bạn ơi.
Gọi x là nHCl, y là nH2SO4
nNaOH=0.5.0.04=0.02mol
=>nOH-=0.02mol
PT:
H(+)+OH(-)-->H2O
0.02<0.02
=>nH+ trong 10ml hh axit=0.02
=>nH+ trong 100ml hh axit=0.02.10=0.2mol
PT:
H(+)+OH(-)-->H2O
0.2->0.2
=>nNaOH=0.2mol
m muối=mNa(+)+mCl(-)+mSO4(2-)=23.0.2+35.5x...
< = > 35.5x+96y=8.6 (1)
Ta lại có: nH+=x+2y=0.2 (2)
Từ (1)(2)=>x=0.08, y=0.06.
Vậy [HCl]=0.08M, [H2SO4]=0.06M.
Đúng 1
Bình luận (2)
Để trung hòa 10 ml dung dịch hỗn hợp axit gồm HCl và
H
2
S
O
4
cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100 ml dung dịch hỗn hợp axit trên đem trung hòa bằng một lượng NaOH vừa đủ rồi cô cạn thì thu được 13,2 gam muối khan. Nồng độ mol của mỗi axit trong dung dịch ban đầu lần lượt là A. 0,8M và 0,6M B. 1M và 0,5M C. 0,6M và 0,7M D. 0,2M và 0,9M
Đọc tiếp
Để trung hòa 10 ml dung dịch hỗn hợp axit gồm HCl và H 2 S O 4 cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100 ml dung dịch hỗn hợp axit trên đem trung hòa bằng một lượng NaOH vừa đủ rồi cô cạn thì thu được 13,2 gam muối khan. Nồng độ mol của mỗi axit trong dung dịch ban đầu lần lượt là
A. 0,8M và 0,6M
B. 1M và 0,5M
C. 0,6M và 0,7M
D. 0,2M và 0,9M
Chọn A
Gọi nồng độ mol ban đầu của HCl và H 2 S O 4 lần lượt là x và y (M)


Đúng 0
Bình luận (0)
Cho 0,01 mol
α
- amino axit a tác dụng vừa đủ với 40ml dung dịch HCl 0,25M. Cô cạn dung dịch sau phản ứng thu được 1,835 gam muối. Khối lượng phân tử của a là A. 140 B. 147. C. 150 D. 160.
Đọc tiếp
Cho 0,01 mol α - amino axit a tác dụng vừa đủ với 40ml dung dịch HCl 0,25M. Cô cạn dung dịch sau phản ứng thu được 1,835 gam muối. Khối lượng phân tử của a là
A. 140
B. 147.
C. 150
D. 160.
Cho 0,01 mol
α
- amino axit a tác dụng vừa đủ với 40ml dung dịch HCl 0,25M. Cô cạn dung dịch sau phản ứng thu được 1,835 gam muối. Khối lượng phân tử của a là: A. 140 B. 147 C. 150 D. 160.
Đọc tiếp
Cho 0,01 mol α - amino axit a tác dụng vừa đủ với 40ml dung dịch HCl 0,25M. Cô cạn dung dịch sau phản ứng thu được 1,835 gam muối. Khối lượng phân tử của a là:
A. 140
B. 147
C. 150
D. 160.