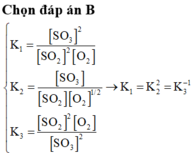Cho cân bằng:
2SO2 (k) + O2 (k) ⇄ 2SO3 (k) ; ∆ H < 0 xảy ra trong bình kín. Nhận xét nào sau đây là sai ?
A. Khi tăng nhiệt độ phản ứng thì tỉ khối của hỗn hợp khí so với H2 tăng.
B. Khi tăng áp suất chung của hệ phản ứng thì tỉ khối của hỗn hợp khí so với H2 tăng.
C. Khi tăng nồng độ SO2 thì tỉ khối của hỗn hợp khí so với H2 tăng.
D. Khi cho thêm xúc tác V2O5 thì tỉ khối của hỗn hợp khí so với H2 không đổi.