Hãy cho biết tính chất chung của các tinh thể nguyên tử.
NN
Những câu hỏi liên quan
Hãy cho biết các tính chất chung của các tinh thể phân tử.
Trong tinh thể phân tử, các phân tử vẫn tồn tại như những đơn vị độc lập và hút nhau bằng lực tương tác yếu giữa các phân tử Vì vậy, các tinh thể phân tử dễ nóng chảy, dễ bay hơi. Ngay ở nhiệt độ thường, các tinh thể phân tử như iot, băng phiến (naphtalen) đã từ từ hoá hơi, các phân tử tách rời khỏi mạng tinh thể và khuếch tán vào không khí nên ta dễ nhận ra mùi của chúng.
Các tinh thể cấu tạo từ các phân tử không phân cực như iot, băng phiến dễ hoà tan trong các dung môi không phân cực như benzen, toluen, hexan.
Đúng 0
Bình luận (0)
Hãy cho biết sự khác nhau về tính chất giữa tinh thể nguyên tử và tinh thể phân tử.
Liên kết giữa các nguyên tử trong tinh thể nguyên tử là liên kết cộng hoá trị rất mạnh. Vì vậy, các nguyên tử liên kết với nhau một cách chặt chẽ, do đó tinh thể nguyên tử rất bền, rất cứng, nhiệt độ nóng chảy và nhiệt độ sôi cao. Trong tinh thể phân tử, các phân tử vẫn tồn tại như những đơn vị độc lập và hút nhau bằng lực tương tác yếu giữa các phân tử. Vì vậy, các tinh thể phân tử dễ nóng chảy, dễ bay hơi. Các tinh thể nguyên tử rất khó hoà tan trong các dung môi khác nhau. Các tinh thể phân tử cấu tạo từ các phân tử không phân cực dễ hoà tan trong các dung môi không phân cực. Các tinh thể phân tử cấu tạo từ các phân tử phân cực dễ hoà tan trong các dung môi phân cực.
Đúng 0
Bình luận (0)
Cho các đặc điểm sau đâya, Số electron lớp ngoài cùng của nguyên tửb, Số oxi hoá của các nguyên tố trong hợp chấtc, cấu tạo mạng tinh thể của các đơn chấtd, bán kính nguyên tửCác đặc điểm là đặc điểm chung cho các kim loại nhóm IA? A. a, b, c B. b, c, d C. a, c D. b, c
Đọc tiếp
Cho các đặc điểm sau đây
a, Số electron lớp ngoài cùng của nguyên tử
b, Số oxi hoá của các nguyên tố trong hợp chất
c, cấu tạo mạng tinh thể của các đơn chất
d, bán kính nguyên tử
Các đặc điểm là đặc điểm chung cho các kim loại nhóm IA?
A. a, b, c
B. b, c, d
C. a, c
D. b, c
Điểm khác nhau là bán kính nguyên tử. Từ Li đến Cs, bán kính nguyên tử tăng dần.
Đáp án cần chọn: A
Đúng 0
Bình luận (0)
Hãy cho biết sự khác nhau về các cấu tử (các hạt tạo nên tinh thể) trong tinh thể ion, tinh thể nguyên tử, tinh thể phân tử.
Trong tinh thể ion, các cấu tử là các ion âm và dương. Trong tinh thể nguyên tử, các cấu tử là các nguyên tử. Trong tinh thể phân tử, các cấu từ là các phân tử.
Đúng 0
Bình luận (0)
Hãy cho biết sự khác nhau về liên kết hoá học trong các tinh thể ion, tinh thể nguyên tử và tinh thể phân tử.
Trong tinh thể ion, liên kết giữa các ion là liên kết ion.
Trong tinh thể nguyên tử, liên kết giữa các nguyên tử là liên kết cộng hoá trị.
Trong tinh thể phân tử, liên kết giữa các phân tử là tương tác yếu, được gọi là tương tác giữa các phân tử.
Đúng 0
Bình luận (0)
Tính bán kính gần đúng của nguyên tử canxi biết thể tích của 1 mol canxi tinh thể bằng 25,87 cm3.
(Cho biết: Trong tinh thể, các nguyên tử canxi chỉ chiếm 74% thể tích, còn lại là khe trống).
Thể tích của 1 nguyên tử Ca :
\(V_{\text{Nguyên tử Ca}}=\dfrac{25.87}{6\cdot10^{23}}\cdot\dfrac{74}{100}=3.19\cdot10^{-23}\left(cm^3\right)\)
\(\Rightarrow r=\sqrt[3]{\dfrac{3V}{4\pi}}=\sqrt[3]{\dfrac{3\cdot3.19\cdot10^{-23}}{4\pi}}=1.96\cdot10^{-8}\left(cm\right)\)
Đúng 1
Bình luận (0)
Tính bán kính gần đúng của nguyên tử canxi biết thể tích của 1 mol canxi tinh thể bằng 25,87 cm3.
(Cho biết: Trong tinh thể, các nguyên tử canxi chỉ chiếm 74% thể tích, còn lại là khe trống).
1 mol chứa khoảng 6,02.1023 nguyên tử nên thể tích của 1 nguyên tử canxi là
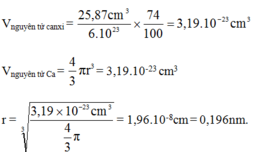
Đúng 0
Bình luận (0)
Hãy kể tên các loại tinh thể đã học và tính chất chung của từng loại.
Các loại tinh thể đã học:
Tinh thể nguyên tử: tính chất chung: bền vững, rất cứng, nhiệt độ nóng chảy và nhiệt độ sôi khá cao.
Tinh thể phân tử: tính chất chung: dễ nóng chảy, dễ bay hơi.
Tinh thể ion: tính chất chung: rất bền vững, các hợp chất ion đề khá rắn, khó bay hơi, khó nóng chảy.
Đúng 0
Bình luận (0)
Kali có cấu trúc mạng tinh thể và có khối lượng riêng là 0,86 gam/cm3 và có bán kính nguyên tử của kali là 2,31A0. Hãy cho biết % thể tích mà các nguyên tử Kali (giả thiết là hình cầu) đã chiếm trong mạng tinh thể. Cho biết K = 39 gam/mol.



