Khối lượng K H C O 3 thu được khí sục 6,72 lít khí C O 2 (đktc) vào 400ml dung dịch KOH 1M là (K=39, O=16, C=12, H=1)
A. 20g
B. 10g
C. 30g
D. 40g
Xác định khối lượng kết tủa thu được khi dẫn từ từ 6,72 lít khí CO2 (đktc) vào 400ml dung dịch Ca(OH)2 1M?
A. 30 gam
B. 40 gam
C. 35 gam
D. 45 gam
Đáp án A
nCO2= 6,72/22,4= 0,3 mol;
nCa(OH)2= 0,4.1= 0,4 mol
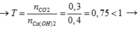
Sau phản ứng thu được muối trung hòa CaCO3
CO2 + Ca(OH)2 → CaCO3 + H2O
Ta có: 0,3 < 0,4 nên CO2 phản ứng hết, Ca(OH)2 còn dư
Ta có: nCaCO3= nCO2= 0,3 mol → mCaCO3= 0,3.100= 30,0 gam
Sục khí 6,72 lít CO2 (đktc) vào dung dịch có chứa 0,25 mol Ca(OH)2. Khối lượng kết tủa thu được là :
A. 10g.
B. 15g.
C. 20g.
D. 25g.
Đáp án C.
Số mol CO2 là: 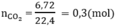
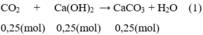
Theo pt (1): nCO2 = nCa(OH)2 = 0,25 mol
nCO2 (dư ) = 0,3 – 0,25 = 0,05 (mol)
Xảy ra phản ứng:
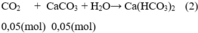
Theo pt(2): nCaCO3 pư = nCO2 = 0,05 mol
Như vậy CaCO3 không bị hòa tan là: 0,25 – 0,05 = 0,2(mol)
Khối lượng kết tủa thu được là m = 0,2. 100 = 20(g)
Sục 6,72 lít khí CO2 (đktc) vào 200 ml dung dịch Ba(OH)2 1M. Khối lượng kết tủa thu được sau phản ứng là bao nhiêu gam?
A. 19,7 gam.
B. 39,4 gam.
C. 59,1 gam.
D. 78,8 gam.
\(n_{CO_2}=0,3\left(mol\right);n_{OH^-}=0,4\left(mol\right)\)
Lập T : \(\dfrac{n_{OH^-}}{n_{CO_2}}=\dfrac{0,4}{0,3}=1,33\) => Tạo 2 muối BaCO3 và Ba(HCO3)2
Gọi BaCO3 (x_mol) , Ba(HCO3)2 (y_mol)
Ta có : \(\left\{{}\begin{matrix}x+y=0,2\left(BTNT:Ba\right)\\x+2y=0,3\left(BTNT:C\right)\end{matrix}\right.\)
=> x= 0,1 ;y=0,1
=> \(m_{BaCO_3}=0,1.197=19,7\left(g\right)\)
=> Chọn A
Sục 6,72 lít khí CO2 (đktc) vào 200 ml dung dịch Ba(OH)2 1M. Khối lượng kết tủa thu được sau phản ứng là bao nhiêu gam?
A. 19,7 gam.
B. 39,4 gam.
C. 59,1 gam.
D. 78,8 gam.
Hoà tan hoàn toàn 31,3 gam hỗn hợp gồm K và Ba vào nước, thu được dung dịch X và 5,6 lít khí H2 (đktc). Sục 8,96 lít khí CO2 (đktc) vào dung dịch X, thu được lượng kết tủa là
A. 49,25 gam
B. 39,40 gam
C. 78,80 gam
D. 19,70 gam
Hoà tan hoàn toàn 31,3 gam hỗn hợp gồm K và Ba vào nước, thu được dung dịch X và 5,6 lít khí H2 (đktc). Sục 8,96 lít khí CO2 (đktc) vào dung dịch X, thu được lượng kết tủa là
A. 49,25 gam.
B. 39,40 gam.
C. 78,80 gam.
D. 19,70 gam.
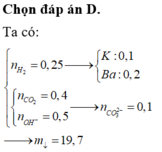
| CHÚ Ý |
| Với bài toán này tôi áp dụng công thức kinh nghiệm
|
Hoà tan hoàn toàn 31,3 gam hỗn hợp gồm K và Ba vào nước, thu được dung dịch X và 5,6 lít khí H2 (đktc). Sục 8,96 lít khí CO2 (đktc) vào dung dịch X, thu được lượng kết tủa là
A. 49,25 gam.
B. 39,40 gam.
C. 78,80 gam.
D. 19,70 gam.
Sục hoàn toàn 6,72 lít khí CO2 (đktc) vào 0,25 lít dung dịch Ca(OH)2 1M thu được bao nhiêu gam kết tủa?
A. 10 gam
B. 30 gam
C. 40 gam
D. 20 gam
Đáp án D
nCO2 = 6,72: 22,4 = 0,3 mol
nCa(OH)2 = 0,25.1 = 0,25 mol => nOH = 2nCa(OH)2 = 0,5 mol
Ta thấy: nCO2 < nOH < 2nCO2
=> phản ứng tạo hỗn hợp muối HCO3 và CO3
=> nCO3 = nOH – nCO2 = 0,5 – 0,3 = 0,2 mol < nCa2+
=> nCaCO3 = nCO3 = 0,2 mol
=> mkết tủa = 0,2. 100 = 20g
Hòa tan một mẫu hợp kim K-Ba có số mol bằng nhau vào nước được dung dịch X và 6,72 lít khí (đktc). Sục 0,025 mol khí CO2 vào dung dịch X thu được m gam kết tủa. Giá trị của m là:
A. 2,955
B. 4,334
C. 3,940
D. 4,925
Đáp án D
Ba+ 2H2O → Ba(OH)2+ H2
K + H2O → KOH + ½ H2
Đặt nBa = x mol; nK = x mol
n H 2 = x+ ½ x =6,72/22,4 =0,3 mol
→ x = 0,2 mol ; n O H - = 2. n H 2 = 0,6 mol
Ta thấy:
T = n O H - n C O 2 = 0 , 6 0 , 025 = 24 > 2
→ CO2 phản ứng với OH- theo PT sau:
CO2+ 2OH- → CO32-+ H2O
0,025 0,6 0,025 mol
Ba2+ + CO32- → BaCO3↓
0,2 0,025 mol 0,025 mol
m B a C O 3 = 0,025. 197 = 4,925 (gam)
Lấy 200ml dung dịch Ba(OH) 2 hấp thụ vừa đủ với 6,72 lít khí CO 2 (
đktc) tạo kết tủa trắng
a. Viết phương trình hóa học xảy ra.
b. Tính nồng độ mol của dung dịch Ba(OH) 2 đã dùng
c. Tính khối lượng kết tủa thu được.( Ba = 137, O =16, H =1, C = 12)
a, \(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Ba(OH)2 + CO2 → BaCO3 + H2O
Mol: 0,3 0,3 0,3
b, \(C_{M_{ddBa\left(OH\right)_2}}=\dfrac{0,3}{0,2}=1,5M\)
c, \(m_{BaCO_3}=0,3.197=59,1\left(g\right)\)